Nature:谜题破解!全面解析卵巢癌转移关键蛋白!
2019-05-31 Ruthy 转化医学网
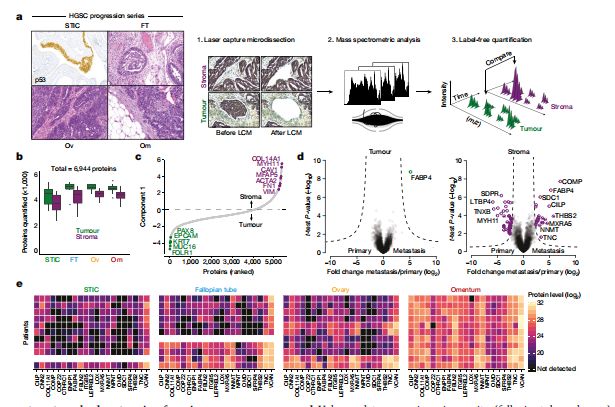
卵巢癌发病率居女性生殖系统恶性肿瘤第3位,死亡率居妇科恶性肿瘤之首。其中,高级别浆液性卵巢癌(HGSC)是卵巢上皮性癌中最常见的一种,大多数患者就诊时已属晚期,恶性程度较高,而难以避免的腹腔转移则是不良预后的罪魁祸首,如何控制转移成为了HGSC治疗的重要难点之一。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Nat#
40
#解析#
44
#关键蛋白#
41
#癌转移#
26