Lancet子刊:北京大学沈琳等多团队合作表明并非所有与高肿瘤突变负担的突变都能增强抗肿瘤免疫反应
2023-01-27 iNature iNature 发表于陕西省
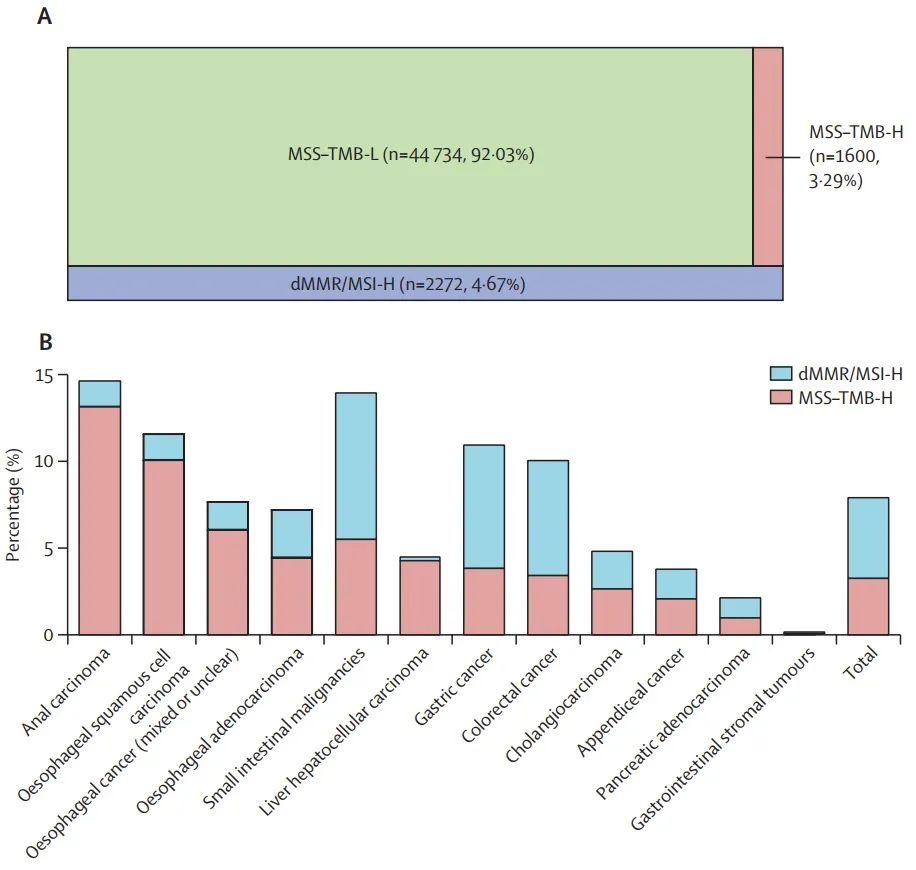
该研究旨在描述微卫星稳定型(microsatellite stable,MSS) TMB-H胃肠道肿瘤的分子特征。
与错配修复缺陷(mismatch-repair deficiency,dMMR)或高微卫星不稳定性(microsatellite instability-high,MSI-H)状态无关的高肿瘤突变负担(tumour mutational burden,TMB-H)的基因组特征尚未得到很好的研究。
2023年1月18日,北京大学沈琳团队及美国南加州大学Heinz-Josef Lenz团队(北京大学为第一单位)合作在 Lancet Oncology 杂志在线发表题为“Mutational analysis of microsatellite-stable gastrointestinal cancer with high tumour mutational burden: a retrospective cohort study”的研究论文,该研究旨在描述微卫星稳定型(microsatellite stable,MSS) TMB-H胃肠道肿瘤的分子特征。
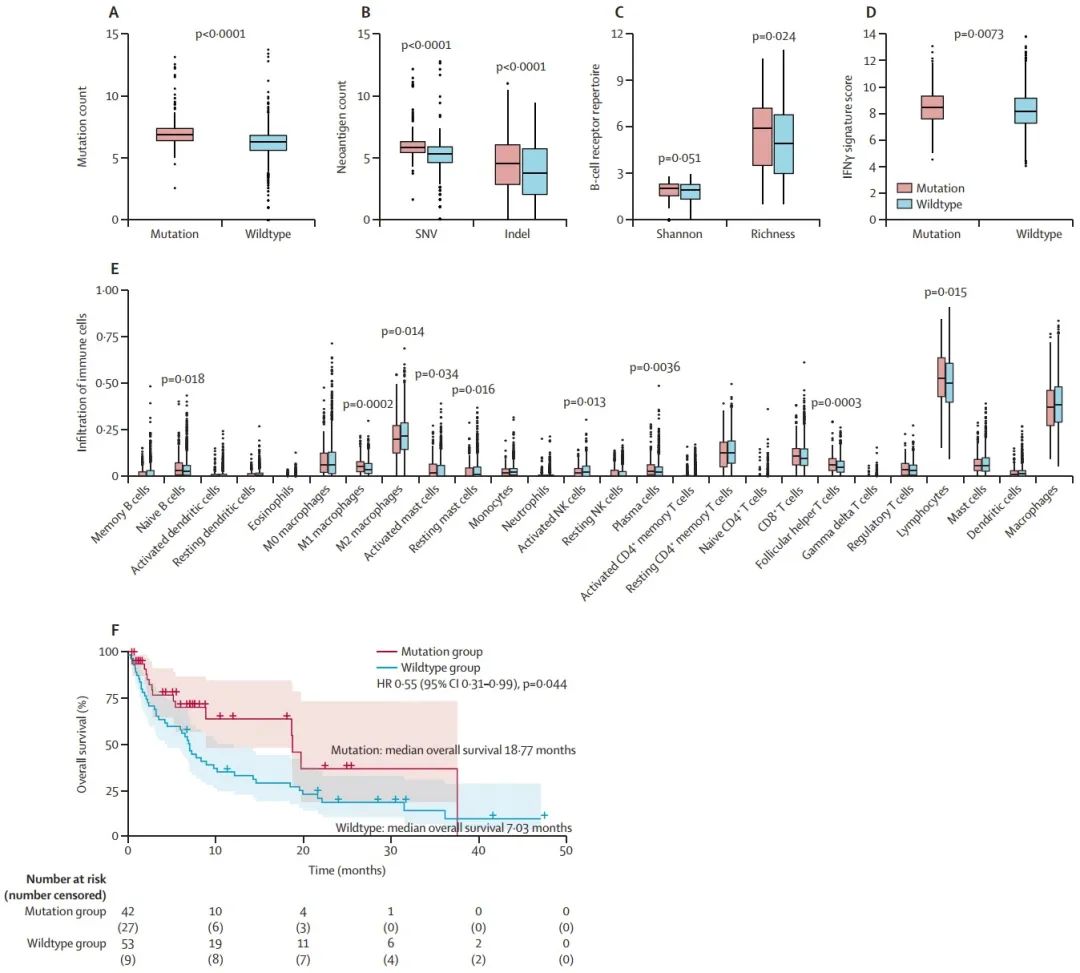
研究表明并非所有与TMB-H相关的突变都能增强抗肿瘤免疫反应。应该研究更多的复合生物标志物(如mTMB特征),以定制免疫检查点抑制剂的治疗。这些数据也为免疫检查点抑制剂和靶向周期蛋白D1或FGFs的药物的联合应用提供了新的见解。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







