罗氏诊断亮相第二届中国国际进口博览会,汇聚“全新、最多”,持续推动医疗创新
2019-11-05 MedSci MedSci
2019年11月5日,第二届中国国际进口博览会(以下简称“进博会”)已正式拉开帷幕。罗氏诊断及罗氏制药作为罗氏集团两个核心业务,再度联袂亮相本次盛会,在700平米的展台上,集中展出个体化医疗领域的创新产品及全面的解决方案。 罗氏诊断中国总经理姚国樑表示:“进博会是中国开放市场的一个重要举措,它不仅承载着全球企业对于中国市场的新期待,也为各行各业的发展带来新的契机。罗氏诊断与中国市场共同成长近2
2019年11月5日,第二届中国国际进口博览会(以下简称“进博会”)已正式拉开帷幕。罗氏诊断及罗氏制药作为罗氏集团两个核心业务,再度联袂亮相本次盛会,在700平米的展台上,集中展出个体化医疗领域的创新产品及全面的解决方案。
罗氏诊断中国总经理姚国樑表示:“进博会是中国开放市场的一个重要举措,它不仅承载着全球企业对于中国市场的新期待,也为各行各业的发展带来新的契机。罗氏诊断与中国市场共同成长近20年,中国已经成为罗氏在全球最重要的战略中心之一,我们非常重视进博会这一全球化的贸易交流平台,希望通过此次盛会,加速更多创新体外诊断技术在中国的落地,惠及更多中国患者,助力‘健康中国2030’战略。”

图为:罗氏诊断中国总经理姚国樑先生
罗氏携体外诊断最新技术参展 带来肿瘤诊疗新希望
体外诊断是通过对体液、血液、尿液、组织等人体样本进行检测,从而获取有关健康和疾病的客观信息,是影响临床治疗决策的关键。目前,体外诊断技术也正被广泛地运用于肿瘤的诊疗过程。尤其在个体化医疗时代,伴随诊断的重要性日益凸显。这一新的体外诊断理念能够帮助医生确认患者癌症的分子分型和选择针对性的治疗药物,实现“同癌异治”,让患者受益于疗效更佳的个体化医疗解决方案。
诊断和制药的综合优势使得罗氏在个体化医疗发展的浪潮中成为先驱者和领先者。本届进博会,罗氏诊断也带来了其肿瘤诊断领域的最新成果,其中就包括应用于免疫治疗和靶向治疗的伴随诊断产品,也期望通过这次展示可以让更多大众了解到前沿诊断技术的在肿瘤诊疗中的重要作用。

肿瘤免疫治疗自问世以来,受到了广泛的关注,尤其是这两年肿瘤免疫治疗药物在中国陆续获批上市,引发了社会热议。但事实上,精准检测才是实现精准医疗的第一步。罗氏诊断此次展出的VENTANA PD-L1(SP263)检测试剂盒,可用于检测肺癌和尿路上皮癌的PD-L1表达,关联主流的3种免疫治疗药物的用药检测,是目前国际上关联免疫治疗药物最多的伴随诊断产品,这款检测有望明年初在中国获批上市;VENTANA PD-L1(SP142)检测试剂盒,是全球首个获批的三阴性乳腺癌免疫治疗的伴随诊断检测产品。长期以来化疗几乎是转移性三阴性乳腺癌患者的唯一治疗方法。直到最近,罗氏诊断的PD-L1(SP142)伴随诊断和罗氏制药的Tecentriq免疫治疗药物的出现,让三阴性乳腺癌患者获得了新的希望。
肺癌是我国发病率和死亡率均高居首位的癌症。肺癌可分为小细胞肺癌和非小细胞肺癌,后者约占肺癌总数的80-85%,非小细胞肺癌又可分为肺腺癌、肺鳞癌和大细胞癌。中国肺癌人群中肺腺癌占50.1%,肺鳞癌占33.4%,其中约50%肺腺癌患者伴有EGFR突变。靶向治疗是目前EGFR突变患者最有效的治疗方法。今年,罗氏诊断新一代cobas EGFR V2检测试剂盒针对血浆样本的适应症正式在中国获批,这使得这款产品成为可以使用组织和血浆两种检测样本的肿瘤基因检测产品。针对血浆样本的检测为无法通过手术获得肿瘤组织样本的患者带来新的希望。该产品也是同时被中国国家药品监督管理局和美国FDA批准用于特罗凯®、泰瑞沙®及易瑞沙® 等 EGFR靶向药物的伴随诊断检测,这些药物均可用于EGFR突变阳性非小细胞肺癌的一线治疗。

最新肿瘤多学科会诊数字化方案 打开疾病管理新纪元
近年来,数字化是各行业关注的焦点。罗氏诊断也在积极探索数字化转型,研发更多可用于支持临床决策的数字化产品。在进博会上,罗氏也带来了最新推出的NAVIFY Tumor Board肿瘤多学科会诊平台,这是罗氏的第一款数字化产品,不仅能协助肿瘤多学科团队的医生完成患者所有相关临床数据的整理,还可通过强大的数据库,提供全球的临床指南、临床研究等资料并不断更新,成为参与肿瘤多学科会诊医生们的“智库”。
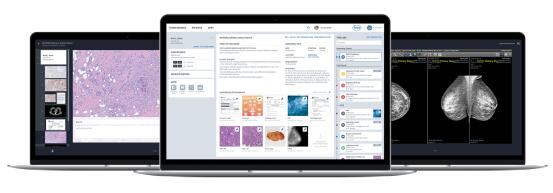
图:NAVIFY Tumor Board 2.0
智能化方案 打造“智慧”实验室
医疗服务需求的不断提升对检验流程与管理提出了更高的要求,实验室管理面临着多方压力与严峻挑战,自动化、系统化、精益化管理理念越来越受到关注。MyLab+智能化实验室管理方案就是罗氏诊断基于实验室需求,以自动化为基础结合精益管理,大数据、人工智能等“黑科技”,为实验室打造定制化智慧方案。对于临床医生和患者而言,MyLab+能帮助他们更快地拿到检验报告,特别是对如心梗等需要急救的疾病而言,越早拿到高准确度的检测结果就能挽救更多的生命。当然,肿瘤相关标志物的检测也涵盖在相关检测菜单中,这些检测结果均能帮助医生为患者进行诊断和治疗。

罗氏诊断进入中国发展的近20年中,公司始终将企业自身的成长与中国医疗改革发展紧密联系在一起,伴随着中国医疗行业及体外诊断领域的蓬勃发展,中国已经成为罗氏诊断全球第二大市场,也是罗氏持续性投入的关键市场之一。
罗氏诊断中国总经理姚国樑先生强调:“进博会的举办代表着中国持续开放市场,与世界共享未来的决心,也让我们跨国企业看到更多在中国发展的机遇。罗氏诊断对这片开放与不断发展的市场始终充满激情和信心。我们根植于此,将通过不断创新,丰富体外诊断解决方案,推动医疗事业的前进,为中国患者和中国医生解答更多有关疾病的疑问。”
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#医疗创新#
41
#创新#
38