综述:四代EGFR抑制剂
2022-10-20 精准药物 精准药物
三代EGFR-TKIs是NSCLC治疗的主力用药,但由于C797S突变及旁路信号激活等原因已有不少患者对奥希替尼等三代EGFR-TKIs产生耐药,这类患者疾病进展后治疗选择十分有限。
前言
三代EGFR-TKIs是NSCLC治疗的主力用药,但由于C797S突变及旁路信号激活等原因已有不少患者对奥希替尼等三代EGFR-TKIs产生耐药,这类患者疾病进展后治疗选择十分有限,亟需研发新一代药物来满足他们的治疗需求。
研发挑战 | 三代EGFR和ALK-TKI的耐药机制及处理方案
EGFR的激酶区共有3个结合位点,分别是ATP结合位点、变构结合位点以及失活位点,失活位点无法被小分子靶向,故已报导的EGFR-TKIs主要可分为三大类,其一为ATP竞争性的抑制剂,结合在ATP结合位点,已上市的EGFR-TKIs均属这一类别;其二为变构抑制剂,结合在变构口袋,已有临床前小分子披露;此外,也有同时结合ATP口袋及变构口袋的临床前小分子报导。
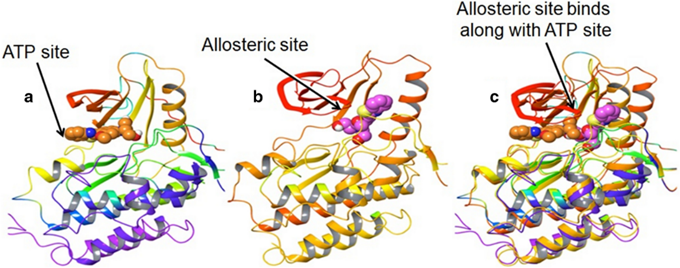
ATP竞争性抑制剂
该类抑制剂为四代EGFR-TKI开发的主流方向,与胞内ATP竞争结合EGFR,对小分子的激酶抑制活性要求较高。截至2022年9月,已有10个小分子进入临床,其中有6个来自中国医药企业,包括正大天晴、贝达、齐鲁、豪森等。
①BLU-945,由Blueprint公司经高通量筛选后优化得到,对双突变、三突变的EGFR均有效,在ex19del/T790M/C797S、L858R/T790M/C797S的BaF3细胞IC50分别为4.4和2.9 nM,细胞活性极佳,与此同时,其对wt EGFR的IC50为544 nM,选择性超过200倍。在针对奥希替尼耐药患者的I期剂量递增试验中,也观察到较高的安全性,与wt EGFR抑制相关的副反应极少,80%以上的患者实现了T790M和C797S 的ctDNA下降,缩瘤效果明显。

②BLU-701也是由Blueprint开发的四代EGFR抑制剂,和BLU-945互为补充,对BLU-945抑制活性不强的单突变及双突变EGFR有强活性,目前也处于I期临床研究中。
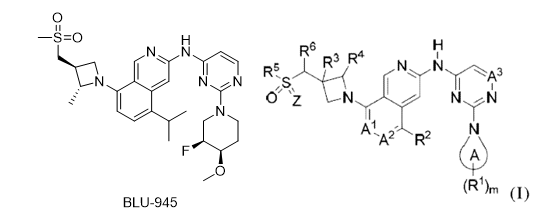
③JIN-A02由韩国J INTS BIO公司开发,对携带三突变或双突变的BaF3细胞IC50均在50 nM左右,此外,对ex19del/T790M/L718Q、L858R/T790M/L718Q等罕见突变也具有一定活性(60-100 nM),对wt EGFR的选择性接近15倍。在PDC模型中,50 mg/kg和60 mg/kg QD也可显著抑制小鼠肿瘤生长,TGI分别达到91.7%和95.7%。
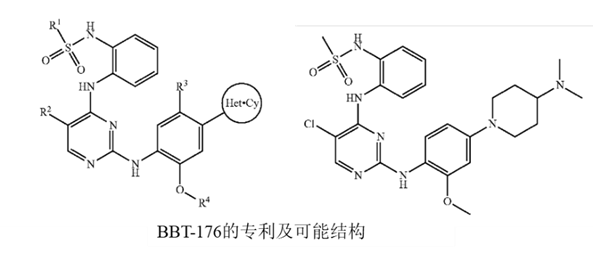
④BBT-176由韩国化学技术研究院在ALK抑制剂Brigatinib的基研上开发得到,后将全球权益授权Bridge Biotherapeutics公司,是全球第一个进入临床的四代EGFR-TKI,2021年4月便开始了剂量递增试验,已披露的数据显示其安全性较好,未报道剂量限制性毒性或因TRAE导致的停药,并已观察到初步疗效。
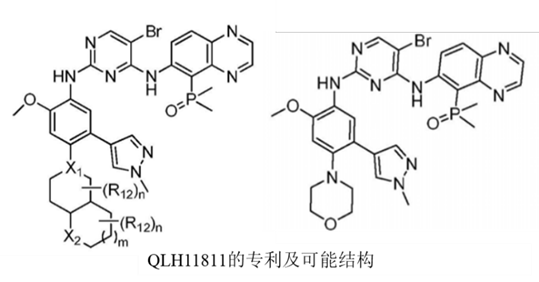
⑤国内EGFR四代抑制剂的玩家众多,竞争激烈,正大天晴(TQB3804)、贝达(BPI-361175)、齐鲁(QLH11811)、豪森(HS10375)、红云生物(H002)、成都地奥九泓(DAJH-1050766)均已推进到临床一期的剂量递增试验,查询专利发现,这些四代EGFR-TKI均是由Brigatinib改造得来,Brigatinib最早于2017年4月获FDA批准用于ALK突变阳性的NSCLC患者,后续研究发现该分子同时也能抑制C797S突变的EGFR,对三突变EGFR的BaF3细胞抑制活性达到了100 nM,而且又是上市药物,成药性非常好,相信这也是中韩药企纷纷选择Brigatinib作为先导化合物的原因。根据专利的披露,国内药企的分子酶抑制活性及细胞活性均可达到10 nM级,PK/PD也相当不错,仅在对野生型的选择性上略有差异。


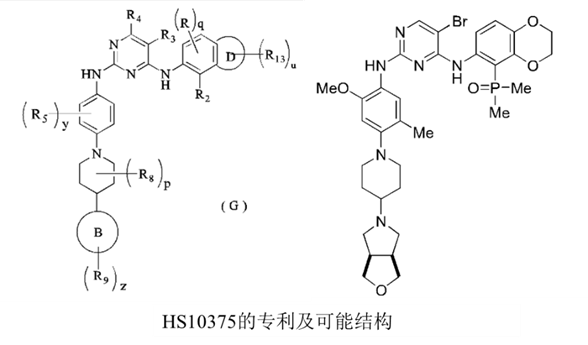
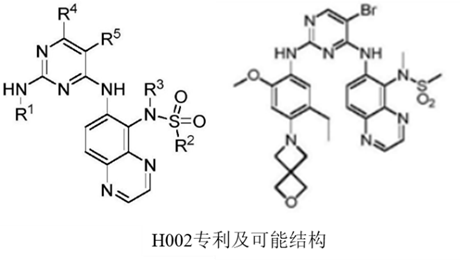
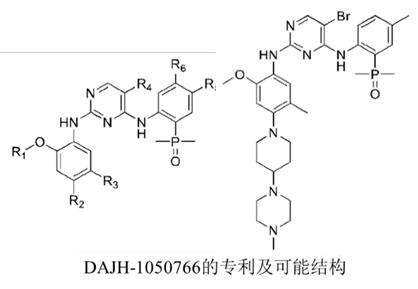
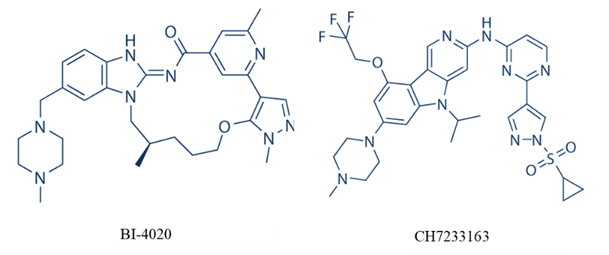
⑥除了临床中的化合物,临床前也有不少高活性、高结构新颖性的四代EGFR-TKI披露,比如勃林格殷格翰公司的BI-4020、中外制药的CH7233163,在19年及20年便已披露结构,但似乎并未往临床推进。
 变构抑制剂
变构抑制剂
结合EGFR的变构口袋,改变EGFR的构象使其活性被抑制。对野生型具有高选择性,目前仍处于临床前,且由于EGFR的二聚化导致其单药体内无效,但针对先导变构抑制剂的进一步的开发研究仍在继续,科学家们始终相信通过对结构进行优化可以实现单药有效。今年4月由Dana-Farber 癌症研究所研究人员发表在Nature Cancer上的论文迈出了关键的一步,其在JBJ-04-125-02基础上开发的变构抑制剂JBJ-09-063实现了体内单药有效。相信随着研究的深入,第一个进入临床的EGFR变构抑制剂也将很快到来。
 双位点抑制剂
双位点抑制剂
同时占据 ATP 结合位点和变构位点,研究还处于相对较早期,在研究论文中多有报导,主要是在EGFR-TKI或变构抑制剂的基础上,进行基于结构的合理设计来增加对另一结合口袋的亲和力,从文献数据来看,激酶抑制活性尚可,但可能是由于分子量较大,膜渗透性不佳,导致细胞活性较差,未来需要进一步优化精简其结构以提高活性。
总结
目前已有不少药企投入到四代EGFR-TKIs的开发中去,主要的开发路径有两种,一种是通过高通量筛选得到具有新颖结构的先导分子,再进一步的对活性和成药性进行优化得到临床候选化合物;另一种则是对已上市的Brigatinib进行改造,提高其抑制活性,并产生可专利的结构,国内已进入临床的分子均由该路径研发得到。
从专利来看,该赛道玩家众多,远不止已进入临床的10个小分子,竞争相当激烈。而如果新一代药物仅仅定位于三代TKIs耐药后的二线甚至三线治疗,那么市场天花板相对较低。
因此,最有市场潜力的四代TKI应当是对C797S突变EGFR有效的同时,也能显著抑制一代二代TKIs针对的单突变或双突变(L858R、del 19、T790M等),以方便在后续研究中提升其临床治疗地位,覆盖更多患者。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#EGFR抑制剂#
28