Nat Cancer:南开大学陈佺等团队合作发现通过LGR4靶向激活结直肠癌铁死亡克服获得性耐药
2024-02-03 iNature iNature 发表于陕西省
该研究发现通过LGR4靶向激活结直肠癌铁死亡能够克服获得性耐药。
获得性耐药是癌症治疗的主要挑战,也是癌症死亡的主要原因;然而,耐药机制是多种多样的,特异性靶向耐药癌细胞的策略仍然是一个未满足的临床问题。
2024年1月30日,南开大学陈佺、胡刚、中国科学院动物研究所杜蕾共同通讯在Nature Cancer在线发表题为“Targeted activation of ferroptosis in colorectal cancer via LGR4 targeting overcomes acquired drug resistance”的研究论文,该研究发现通过LGR4靶向激活结直肠癌铁死亡能够克服获得性耐药。该研究建立了一个结直肠癌衍生的类器官生物库,并通过重复低水平暴露化学药物诱导获得性耐药。化疗敏感性分析和转录组学分析研究显示,化疗耐药的癌源类器官表现出LGR4的表达升高和Wnt信号通路的激活。
该研究还制备了一种单克隆抗体(LGR4-mAb),它能有效抑制LGR4-Wnt信号传导,并发现LGR4-mAb能显著致敏药物诱导的铁死亡。从机制上讲,LGR4依赖性Wnt信号通过转录上调铁死亡的关键抑制剂SLC7A11,从而产生获得性耐药。该研究表明,LGR4-mAb与化疗药物联合使用时,靶向Wnt信号传导增强了铁死亡,显示了对抗难治性和复发性癌症的潜在机会。
另外,2024年1月29日,南开大学陈佺、李艳君、浙江大学王勇、中国科学技术大学熊伟及朱洪影共同通讯在Nature Chemical Biology 在线发表题为“PAFAH2 suppresses synchronized ferroptosis to ameliorate acute kidney injury”的研究论文,该研究发现血小板活化因子(PAF)和PAF样磷脂(PAF-LPLs)介导同步性铁死亡并导致AKI。铁死亡中PAF和PAF-LPLs的出现引起生物膜的不稳定,并提示邻近细胞的死亡。这种级联反应可以通过PAF乙酰水解酶(PAFAH2)或添加抗PAF抗体来抑制。基因敲除或药物抑制PAFAH2可增加PAF的产生,增强同步性铁死亡,加重缺血/再灌注(I/R)诱导的AKI。值得注意的是,静脉注射野生型PAFAH2蛋白,而不是其酶失活突变体,可以防止同步小管细胞死亡、肾单位损失和AKI。该研究提供了对同步铁死亡机制的深入了解,并提出了AKI预防性干预的可能性、。

在过去的十年中,在对抗癌症方面取得了非凡的突破,包括新的诊断和治疗策略。然而,癌症耐药和复发仍然是治疗失败和癌症相关死亡的主要原因。某些类型的癌细胞,如癌症干细胞(CSCs)或肿瘤启动细胞,以及所谓的持久性细胞,具有间充质样基因表达谱,获得了耐药性的所有特征,使它们在癌症治疗中处于独特的地位。几种信号通路,包括Wnt通路,决定肿瘤的发生,维持CSC性能和促进化学抗性典型的Wnt信号通过细胞表面受体(如LGR4/ LGR5)与可溶性配体(包括Wnt和R-spondin)结合而激活,从而促进癌蛋白β-catenin的核积累。
在细胞核中,β-连环蛋白与TCF/LEF转录因子复合物转录激活Wnt靶基因。特别是在结直肠癌(CRC)中,由于LGR4/LGR5及其可溶性配体的水平不同,Wnt -β-catenin通路的激活水平在不同的CRC之间是不同的。此外,APC和CTNNB1等基因的不同类型突变导致Wnt -β-catenin活性不同程度的变化。在许多癌症中,Wnt - β-连环蛋白活性与化疗耐药呈正相关。Wnt -β-catenin上调ABC转运蛋白的表达,该转运蛋白泵出有毒成分并促进CD44的表达,CD44被认为是CSCs的标记物和抗凋亡蛋白的调节因子。因此,靶向Wnt信号和CSCs是克服耐药性的一种有希望的策略;然而,在临床环境中尚未实现专门克服耐药性的治疗方法。
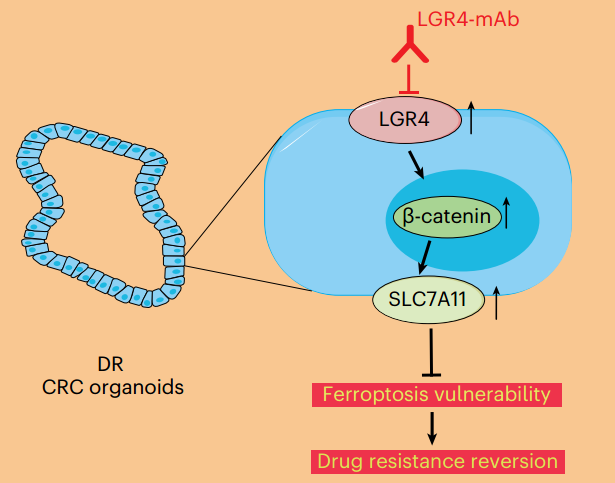
LGR4-mAb对DR CRC类器官致敏的示意图(图源自Nature Cancer )
铁死亡是一种特殊的、受调控的坏死细胞死亡形式,其特征是铁依赖性脂质过氧化和膜破裂。磷脂过氧化物酶谷胱甘肽过氧化物酶4 (GPX4)或胱氨酸/谷氨酸反转运蛋白SLC7A11的失活会导致细胞谷胱甘肽(GSH)的耗竭,导致脂质过氧化和随后的铁死亡。几种致瘤性信号通路,如p53、KRAS和Hippo通路,已被发现调节铁死亡。这些途径可能改变SLC7A11和GPX4的表达或脂质代谢,从而调节铁死亡的敏感性和耐药性。因此,这些研究提高了利用铁死亡易感性来对抗癌症的可能性。事实上,新出现的证据表明,包括索拉非尼和顺铂在内的几种化疗药物已被发现可促进癌细胞的铁死亡。将诱导铁死亡的药物如RSL3与化疗药物联合使用可实现协同抗癌活性。这似乎是一个很有希望的根除肿瘤的途径;然而,一个主要问题仍未解决,因为选择性靶向铁死亡途径而不影响正常细胞生长尚未实现。
R-spondin 与LGR5的结合驱动隐窝肠上皮的自我更新。它还支持不断扩大的小肠类器官,这些器官在结构、细胞类型组成和自我更新动态方面显示出原始组织的所有特征。体外实验显示,患者源性结直肠肿瘤类器官(PDOs)可以再现原始肿瘤的分子、遗传和病理特征,但对生态位因子的依赖性较弱或逐渐丧失。肿瘤类器官忠实地概括了临床患者的反应,并预测了化疗和放射敏感性。有证据表明LGR4也是一个真正的CSC标记物。由于LGR4-Wnt信号的激活和随后对铁死亡的抑制,PDOs获得了耐药性。该研究开发了一种选择性靶向LGR4的单克隆抗体,以减轻Wnt信号通路。该抗体和其他Wnt信号调节剂使具有获得性耐药性的PDO中的铁死亡敏感,从而提出了一种克服耐药性的新策略。
原文链接:
https://www.nature.com/articles/s43018-023-00715-8
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















用户帮助作,者审稿人主编副编辑编辑室管理员,生产经理,语言修订,排字员,出版商,联系统计员,
19
#直肠癌# #铁死亡# #获得性耐药#
30