【BCJ】复发/难治性慢性淋巴细胞白血病的治疗新进展
2024-03-04 聊聊血液 聊聊血液 发表于上海
本综述概述了治疗RR CLL患者的最佳方案,包括当前和新出现的治疗方案的证据,包括使用固定疗程的疗法进行再挑战、新疗法时代的异基因干细胞移植指征,并强调了支持使用T细胞导向疗法和新药靶点的早期数据。
RR CLL的治疗
慢性淋巴细胞白血病(CLL)患者的生存持续改善,很大程度上是由于治疗的进步。BTK抑制剂、PI3k抑制剂和BCL2抑制剂作用于B细胞受体信号通路,其问世改变了初治 (TN)和复发/难治性(RR) CLL的治疗格局,CLL患者在首次治疗指征时和/或后续复发时均可获得多种有效的新型治疗方案。随着T细胞导向疗法、CAR-T疗法、双特异性抗体(bsAb)和BTK降解分子的出现,治疗选择可能会继续扩大,它们在治疗RR CLL的早期研究中均显示出希望。
对于任何疾病复发,应仔细考虑疾病负荷和动力学、高危基因组病变以及Richter转化的风险。应利用复发和后线治疗之间的时间窗来优化CLL相关后遗症和非CLL相关健康问题。当需要治疗时,针对RR CLL的新疗法的选择和排序应个体化考虑患者的优先事项,包括对潜在副作用的耐受性和对治疗疗效的预测。《Blood Cancer Journal》近日发表一篇综述,概述了治疗RR CLL患者的最佳方案,包括当前和新出现的治疗方案的证据,包括使用固定疗程的疗法进行再挑战(rechallenge)、新疗法时代的异基因干细胞移植指征,并强调了支持使用T细胞导向疗法和新药靶点的早期数据。

RR CLL患者的评估
后线治疗的时机
发现RR CLL并不需要立即改变或启动后线治疗。总体而言,RR CLL的治疗指征应与TN CLL的iwCLL 2018治疗指征一致,但维持患者健康和功能应是最终目标,不应因等待满足正式iwCLL标准而推迟治疗。复发时,重要的是事先与患者讨论进一步治疗的时机,确定未来的治疗目标,并考虑其间临床和血液学监测的频率。
既往治疗和生物学变量对疾病进展动力学的影响,可以在MRD的动力学变化中得到理解。在MURANO研究中,对于接受固定疗程维奈克拉-利妥昔单抗(VenR)治疗后MRD无法测量(uMRD)的患者,从转为MRD阳性至达到iwCLL标准中疾病进展的时间为28.3个月;CLL患者伴复杂核型(CK,≥3个拷贝数变异[CNV])在VenR治疗后的中位MRD倍增时间短于无CK的患者(p=0.054),IGHV未突变 (umIGHV) 患者短于IGHV突变(mIGHV)患者(p=0.0057)。VenR后观察到MRD指数增长模式,而苯达莫司汀-利妥昔单抗(BR)治疗后观察到logistic型增长模式。这些数据表明,对于已知有高危基因组病变的患者需要密切监测,也可能需要为后续治疗方案制定更复杂的计划。
对于初治CLL,除非常规免疫抑制治疗失败,否则单独发生自身免疫性血细胞减少并不强制要求对基础CLL进行治疗。对于大多数接受治疗的CLL患者,伊布替尼(Ib)或Ven似乎可成功改善或缓解继发性自身免疫性血细胞减少。
需要进一步治疗的RR CLL患者死亡风险增加,可通过经过验证的BALL评分识别,其包括4分(每项1分):血清β2微球蛋白≥5mg/dL、乳酸脱氢酶高于正常上限、血红蛋白<110 g/L(女性)/<120 g/L (男性)和距离开始末次治疗的时间<24个月;综合评分越高,24个月内死亡的风险越大。该模型已在接受Ib、Ven或idelalisib(或免疫化疗[CIT])治疗的患者队列中得到验证。该评分的目的并非帮助在新型疗法之间进行选择,而是用于实践中讨论治疗目标,或考虑异基因干细胞移植或临床试验的作用时。
CLL相关慢性并发症和其他健康问题的评估
对RR CLL患者的检查也是一个回顾疾病和非疾病相关健康问题和相关预防性健康措施的机会。CLL存在固有的B淋巴细胞和T淋巴细胞功能障碍相关,可导致疾病的多种重要并发症,包括低丙种球蛋白血症、复发性感染和第二原发恶性肿瘤发病率增加。此外,许多患者可能因既往治疗而出现显著的免疫缺陷,从而可能会加剧上述风险。
确保对符合年龄和性别的恶性肿瘤筛查的依从性极为重要,如乳房X线摄影术、宫颈涂片、前列腺特异性抗原检测和结直肠癌筛查。鉴于CLL患者发生的非黑色素瘤性皮肤癌(和黑色素瘤)比例较高,必须警惕皮肤保护措施和每年的皮肤病学评估。应鼓励接种针对季节性流感、肺炎链球菌和带状水痘的非活疫苗。鉴于目前SARS-CoV-19大流行,按照地方卫生行政部门的建议接种疫苗很重要。尽管存在固有免疫功能障碍,通过多次接种疫苗仍可实现充分的血清转换,T细胞应答相对较高。围疫苗期停用BTKi可能提高血清阳转率,但无法提高总体抗刺突抗体滴度中位数。
RR CLL患者多为老年人,许多患者同时患有多种疾病。在RR CLL的检查中可能会发现看似不相关但有影响的问题,包括心血管健康状况恶化、糖尿病和高血压(HTN)、骨密度降低,以及更广泛的虚弱或无法独立生活。在老年人中,这些问题对健康和/或生存的影响可能比并存的CLL更大。在治疗前对更广泛的健康状况进行优化,可能有助于在治疗期间维持功能,并在相关的情况下最大限度地减少新疗法带来的并发症风险(如BTKi的房颤/房扑[AF]或Ven的肾功能受损影响肿瘤溶解)。
考虑Richter转化
向侵袭性B细胞淋巴瘤的Richter转化(RT)是CLL自然史的一部分,但不同研究报告的发生率不同。对于新发发热、高钙血症、不一致的局灶性腺病或累及结外部位等,由于更符合侵袭性B细胞淋巴瘤的增殖特征,临床上或生化上应怀疑RT。虽然“假阳性”常见,但对于FDG-PET上SUVmax >5-10不一致的主要病变应进行活检,以排除RT。在可能的情况下,应通过IGHV测序或评估组织学PD-1表达来确定与共存CLL的克隆关系,PD-1是克隆相关性的有用替代标志物。
基因组重评估:克隆演化和获得高危基因组异常的证据
高危基因组异常对CLL的预后有重要影响,尤其是17号染色体上的TP53异常[del([17p]和/或TP53突变],在新药时代仍具有预后意义。
虽然IGHV突变状态在整个治疗过程中不会变化,并且不需要重复检测,但通过核型分析和荧光原位杂交(FISH) 进行重新评估非常重要,以及既往无TP53的患者进行TP53测序。TP53异常的发生率随着系列治疗的增加而增加,且在氟达拉滨和/或双重难治性疾病患者中较高。存在基线亚克隆驱动突变的情况下,可能需要进行分子学检查以检测克隆进化,并且可能预示较差的预后。在来自伊布替尼的选择压力下,可以观察到显著的早期克隆转移,与疾病进展的风险较大相关。然而,虽然识别ATM、NOTCH1和BIRC3等已知驱动基因的动态突变可能具有学术意义,但目前无法指导当前的治疗选择。
检测RR CLL患者对新疗法的耐药突变在很大程度上仍处于研究阶段。持续暴露于BTKi或BCL2i可能诱导各自靶蛋白编码基因的耐药突变,但在疾病进展时识别变异的临床效用尚未完全确定。例如,共价BTKi(cBTKi)治疗后不论出现或未出现BTK C481变异,均不会改变不接受进一步cBTKi治疗的建议。目前正在评估二代BCL2i在存在BCL2变异的情况下是否有效(NCT04277637)。相比之下,新药有限期治疗后的耐药突变发生率似乎很低。
复发/难治性CLL的治疗策略
患者在CIT或新药或两者之后需要二线或后续治疗,鉴于新药的疗效较好,不建议对RR CLL重复使用CIT。如果既往仅接受过CIT,可以选择cBTKi或BCL2i,如果接受过1种新药后出现疾病进展,则一般建议选择其他新药类别作为后线治疗。但也有例外情况,包括在对初始cBTKi不耐受的情况下使用其他cBTKi,或在既往有限期联合治疗(如ven-抗cd20单抗)后再次使用同样的有限期联合治疗。目前还没有公开发表的头对头比较数据说明BTKi和BCL2i的疗效和安全性,因此治疗方案的选择取决于专家意见和患者与临床医师的个体化讨论。对初治CLL患者的新药进行的网络荟萃分析表明,ven-奥妥珠单抗(VenO)、IbO和阿可替尼(Acala)之间PFS无差异。图1描述的新药治疗排序供参考。
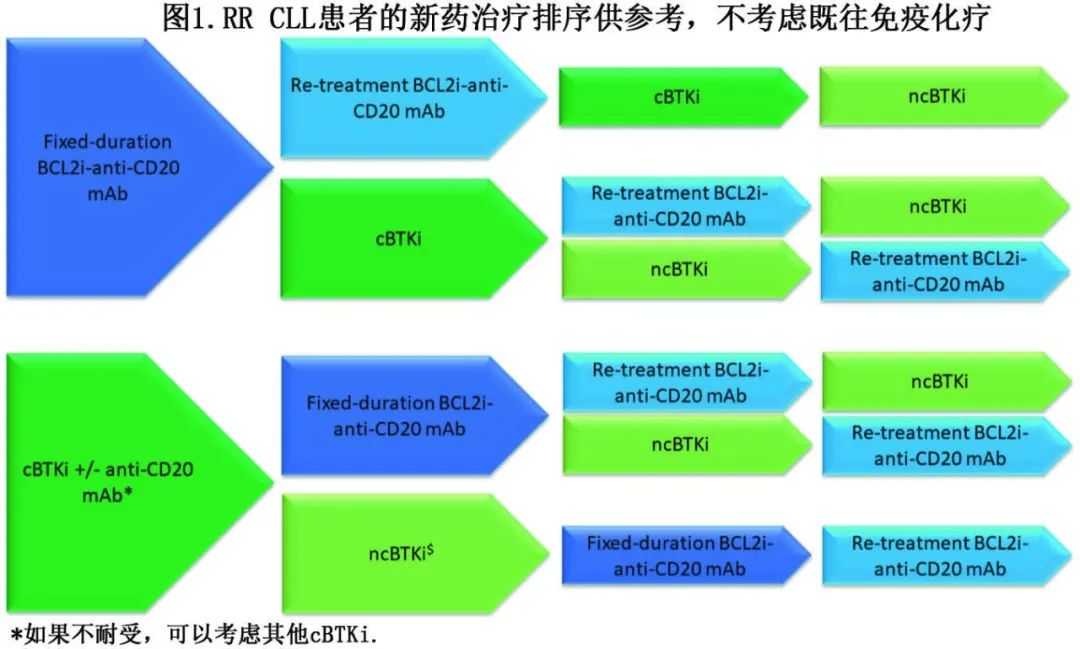
除了药物可及性和既往治疗之外,其他重要因素也会影响RR CLL患者下一步治疗方案的选择。需要讨论的重要内容包括:(1)患者的目标和优先事项,包括对无治疗缓解的倾向性;(2)对治疗目标的认知,是否支持序贯非治愈性策略,和/或潜在的治愈性异基因干细胞移植是否作用;(3)合并症和合并用药的潜在并发症;(4)临床试验的可及性,对临床试验优点和对治疗过程影响的认知。
关于cBTKi、非共价BTKi(ncBTKi)、BCL2i、PI3Ki疗效和安全性的主要证据见表1,其他研究可参考原文,不做赘述。

RR CLL的治疗排序
cBTKi和BCL2i-抗CD20 mAb均为RR CLL的高效治疗方法,由于具有独立的作用机制和耐药,可按任一顺序依次使用。但该认识还存在局限性,包括缺乏可说明这两种排序疗效的随机研究数据,在新药暴露患者和难治性患者之间缺乏全面差异化,以及关键研究中的大多数RR CLL患者既往接受过CIT。
评估Ven→cBTKi的前瞻性数据包括,14例在MURANO接受有限期VenR后疾病进展的患者,均对BTKi治疗有效。在一项回顾性队列研究中,BTKi初治患者在Ven停药后接受cBTKi治疗(n=42;73%接受Ven单药治疗),中位PFS为32个月。其他规模较小的回顾性系列报告了类似的疗效。
对于cBTKi→Ven,一项开放标签2期研究纳入91例在Ib停药(因PD[55%]、不耐受[33%]或其他原因)后接受Ven单药治疗的患者,ORR/CRR为65%/9%,中位PFS为24.7个月。在一项关于新药排序的真实世界研究中,伊布替尼治疗失败后,Ven单药治疗的ORR为79%。最近一项回顾性研究中纳入高危基因组病变富集的cBTKi经治患者,VenR后的PFS和TTNT似乎比MURANO报告的短(其中5例患者接受过cBTKi治疗)。此外,有限期Ib-Ven治疗后疾病进展后,单药Ib似乎有效。
选择初始的新药治疗需要患者与医师进行个体化讨论,考虑治疗目标和优先事项(包括治疗持续时间和后勤方面的问题),以及在已知合并症的情况下的潜在副作用。有限期VenR可能有利于实现潜在的无治疗缓解,并将累积的治疗相关毒性降至最低;但后勤方面的不足包括每周增加剂量,频繁静脉穿刺,可能需要间歇性住院观察,以及静脉给予抗CD20单抗;此外,重度肾功能不全患者不宜使用VenR。相比之下,BTKi是连续口服治疗,不需要剂量调整或类似的密集初始监测;其不足包括患者“药物负担”、导致治疗停止的累积毒性,以及通过持续选择压力选择耐药克隆。此外如前所述,对于有心血管合并症的患者,BTKi给药可能有障碍。
有限期治疗后可再次使用BCL2i-抗CD20 mAb治疗,因为动态耐药机制(包括BCL2突变)不太可能发生。在MURANO子研究中,25例患者在距末次Ven给药中位2.3年后接受了VenR治疗,ORR为72%,再次治疗后的中位PFS为23.3个月;与初始治疗相比,MRD阴性缓解相对短暂。一项回顾性研究显示,再次接受Ven治疗的患者(n=46, 40%有cBTKi暴露史,主要是RR CLL)显示相似的ORR(79%)和mPFS(25个月),uMRD缓解率为41.7%。这些发现提出了一个问题:未来对有限期Ven治疗后至下次治疗时间进行的分析,是否应在适当的情况下纳入再治疗的尝试。一项积极招募患者的研究试图探索VenO一线治疗后该方法的优点(NCT04895436)。
对于不能耐受一种cBTKi的患者,可以选择另一种cBTKi作为后线治疗方案。大多数预先定义的不耐受事件要么不会复发,要么严重程度降低,例如Ib不耐受后Acala治疗,或Acala或Ib和Acala不耐受后泽布替尼(Zanu)治疗。Ib后Acala治疗的RR CLL患者的24个月PFS为72%。但对于室性心律失常或大出血导致的不耐受,可能不应考虑第二种cBTKi。
关于未来BTK靶向治疗的潜在排序,仍有一些问题未得到解答。在Zanu之后发现了“死激酶(dead-kinase)”BTK变异(例如L528W),并证明随后Pirto疗效降低,从而引起了Zanu之后ncBTKi可能无效的担忧。此外,Pirto之后获得的非c481“死激酶”BTK耐药突变可能对二代cBTKi产生交叉耐药,可能影响ncBTKi作为首次BTK靶向治疗的考虑。然而,选择性cBTKi和ncBTKi后“死亡激酶”突变的真实发生率在很大程度上是未知的,因此这些担忧目前都仅是理论上的。
RR CLL的新型疗法
小分子和抗体。BTK蛋白降解剂是一类新兴疗法,对于既往接受过BTKi和BCL2i治疗的患者(包括有BTK耐药突变的患者)有潜在效用。BTK降解剂NX-2127、BGB-16673和NX5948的首次人体研究的初步数据表明,它们对RR非霍奇金淋巴瘤(包括R/R CLL)有早期疗效。
ROR1不由正常B细胞表达,可被单克隆抗体(cirmtuzumab)靶向,但最佳缓解仅限于少数CLL患者获得疾病稳定。在BTKi治疗不完全缓解或耐药突变后,建议使用抗baff抗体(Ianalumab, VAY736)加深缓解(包括uMRD)。
新型MCL1 AZD5991单药针对RR血液系统恶性肿瘤(包括5例CLL患者)开展的1b/2期研究,由于实验室肌钙蛋白升高的发生率高且缓解率低而提前终止。
T细胞导向疗法
虽然CAR-T在首批临床报告中成功治疗了CLL,但与NHL相比,T细胞导向疗法的发展相对缓慢,可能是由于有效的新型疗法的出现。
最近的CAR-T早期数据显示了有前景的ORR和骨髓(BM) uMRD率,包括高危基因组亚组的有限患者。近期自体CAR-T和bsAb治疗RR CLL的关键早期研究的疗效和有限的安全性数据见表2。少数患者可能在CAR-T治疗后达到持久缓解,目前报道CAR-T细胞的持续时间长达10年,从而引发这些患者的CLL是否已被治愈的问题。持久缓解的概率似乎与缓解深度(包括uMRD)相关。然而报告的所有患者的PFS结局相对较短。与非霍奇金淋巴瘤相比,CRS的发生率似乎较高,可能是由于目前存在更高的循环和/或骨髓疾病负荷;包括CRS和神经毒性在内的致死性TEAE也有报道。
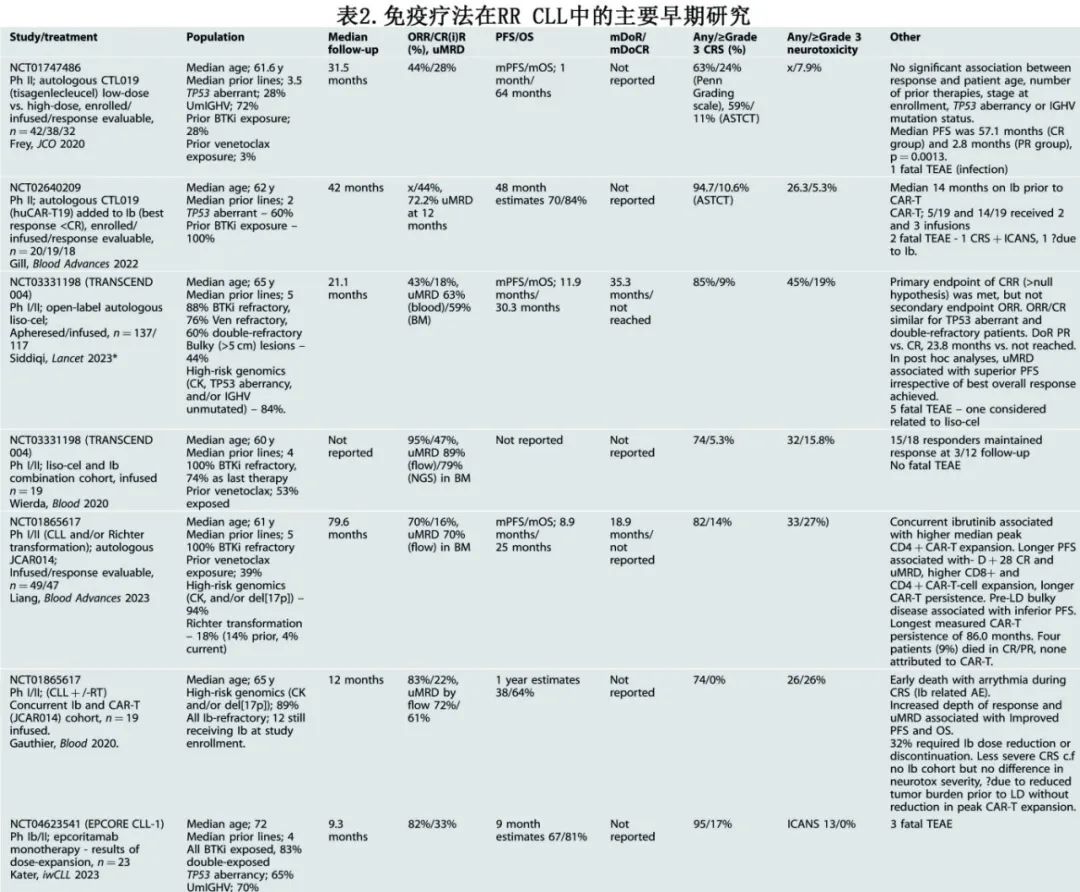
关于bsAb的数据较少,但初步疗效仍有希望。除了EPCORE CLL-1研究中CD20xCD3 bsAb的数据外(见表2),在有限期NVG-111治疗的少数RR CLL(和MCL)患者中也观察到客观缓解(ROR1 xCD3 bsAb)。
T细胞导向疗法治疗CLL的局限性尚不完全清楚,但许多焦点都指向提高自体T细胞健康度(fitness)。CLL相关固有T细胞失调表现为T细胞增殖和免疫突触形成受损,且可能因之前的细胞毒治疗而加剧。与骨髓病变的清除相比,免疫抑制性淋巴结微环境可能是导致CAR-T治疗后淋巴结病变相对持续的原因。多个研究团队探索了同时使用伊布替尼和CAR-T(多用于cBTKi难治性患者)的潜在优点,试图恢复T细胞健康度,并对淋巴结微环境产生有利影响,见表2。EPCORE CLL-1研究(NCT04623541)也计划使用epcoritamab的辅助方法。异基因CAR-T (NCT04030195、NCT03774654、NCT05878184、NCT 05643742)和CAR-NK产品(NCT05739227、NCT05487651、NCT05020678)目前也在评估中。
异基因造血干细胞移植
异基因干细胞移植(alloSCT)是高危CLL的一种潜在治愈方法,尽管由于非复发死亡率(NRM,主要是因为感染或移植抗宿主病),其使用仅限于年轻的较健康患者。在长期随访中,CIT时代的研究表明,在既往接受过多线治疗且高危基因组异常富集的患者中,有30~40%可达到持久的5~10年缓解,但即使采用低强度预处理,NRM仍高达36%。
在高危CLL患者中选择alloSCT的最佳患者是复杂的。年龄和合并症可预测NRM风险,并可通过HCT-CI评分正式计算。为了解alloSCT是否符合患者的优先治疗和未来目标,讨论短期和长期的潜在获益和风险很必要。
虽然2007年欧洲骨髓移植委员会首次定义了高危CLL,但在新药时代,高危CLL的定义仍具有挑战性。随着新疗法的广泛应用和TP53异常CLL患者生存结局的改善,“高危”可能通过以下两方面来动态改进:对第一种新药反应时间较短的较年轻患者,以及序贯治疗的可用性减少。“双重难治性”CLL患者极低的总生存结局,以及alloSCT后患者结局的改善(alloSCT时缓解程度更深),为alloSCT的潜在时机提供了一些指导。对于高危患者,建议在第二次深度缓解(例如接受第二种新药治疗)时考虑alloSCT。BTKi-BCL2i双药或BTKi-BCL2i-抗CD20单抗三药等一线联合治疗后疾病进展的最佳治疗策略尚未确定,但在接受一种或两种治疗再治疗的第二次缓解时也应考虑alloSCT。尽管CAR-T和bsAb等替代免疫疗法具有相当大的前景,但它们目前都处于研究阶段,治疗潜力未知。
总结
我们现在幸运地为RR CLL患者提供了多种有效的治疗方案,且安全性可耐受。随着新机制药物的出现,在最佳使用和有效治疗排序方面也产生新的挑战。RR CLL患者的完整治疗应包括:优化表面上与CLL无关的健康因素,考虑感染预防措施和早期识别继发恶性肿瘤,早期讨论生活目标和优先事项,评估可能驱动疾病进展动力学的因素。
参考文献
Bennett, R., Seymour, J.F. Update on the management of relapsed/refractory chronic lymphocytic leukemia. Blood Cancer J. 14, 33 (2024). https://doi.org/10.1038/s41408-024-01001-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#慢性淋巴细胞白血病# #异基因干细胞移植# #T细胞导向疗法#
19