抗磷脂抗体综合征肾病:病理生理学和管理
2023-07-16 柔济免疫 柔济免疫 发表于上海
抗凝治疗对APLSN患者肾脏结局的预后作用仍有待确定。尽管缺乏大型随机对照试验,抗凝仍然是APLSN治疗的基石。
抗磷脂抗体综合征
抗磷脂抗体综合征(APLS)是一种罕见的自身免疫性疾病,以反复发生动静脉血栓栓塞事件、妊娠相关并发症以及12周内持续抗磷脂抗体阳性为特征。 3%的APLS患者易发生肾脏并发症,其中肾动脉狭窄是最常见的肾脏相关并发症。 从肾脏病理可分为大血管和微血管血栓,其中狭窄、血栓形成和梗塞是主要的大血管事件,而APLS肾病是主要的微血管并发症, APLS肾病临床表现多种多样,从血尿、非肾病性蛋白尿到高血压,或者表现为一种严重的、危及生命的暴发性多器官衰竭疾病,即灾难性抗磷脂抗体综合征(CAPS)。 APLS肾病的处理取决于血管损伤的部位及严重程度、抗体亚型和滴度的血栓风险。在治理方面APLS肾病的主要预防措施是使用小剂量阿司匹林,在手术和住院等增加血栓栓塞风险的事件中进行预防性抗凝。 抗凝是治疗APLS肾病的基石,其INR的目标值取决于相关的静脉或动脉血栓事件。 利妥昔单抗、mTOR抑制剂、Eculizumab和Belimumab等免疫抑制剂的使用取得了一些成功,但缺乏对其使用的随机对照试验验证。大剂量激素冲击结合血浆置换、静脉注射免疫球蛋白是治疗CAPS的有效方法。
抗磷脂综合征相关肾脏并发症之一:肾动脉受累
肾动脉受累可能为单侧或双侧的狭窄或闭塞,源于原位血栓形成或动脉栓子,后者可能继发于血栓。 APLS是肾动脉梗塞的一种罕见因素,可能导致肾梗死和急性肾损伤,但它也可能表现为渐进方式,如慢性缺血性肾病所致的肾功能进行性下降。临床上,急性肾动脉血栓最常见的表现为严重的新发高血压或原有高血压加重伴腰痛、肉眼血尿或肾功能急剧下降。肾动脉多普勒超声是筛查肾动脉狭窄的首选检查。 在APL阳性高血压未控制的患者中,肾脏血管核磁共振可检测出26%的肾动脉狭窄患者,其次,还可通过血管CT、肾血管造影、肾核素显像或血管造影等手段进行检查。增强超声在评估肾损伤和疑似潜在肾脏梗死部位的灌注异常方面越来越受到人们的关注。LDH升高和白细胞增多是两个主要的生物学异常,可评估潜在的肾梗死。
抗磷脂综合征相关肾脏并发症之二:微血管肾病
APLS肾病(APLSN),是一种肾小血管病变,影响肾脏的静脉、毛细血管和动脉。APLSN可具有广泛的临床表现:高血压、镜下血尿、不同程度的蛋白尿,急性肾损伤或慢性肾病。APLSN可分为急性型和慢性型,抗磷脂综合征相关的肾脏病变与其他血栓性微血管病变(TMA)难以区分,如血栓性血小板减少性紫癜(TTP)、典型和非典型溶血性尿毒综合征、钙调磷酸酶抑制剂毒性、子痫前期、肾硬皮病危象、恶性高血压、以及肾移植的急性排斥反应。在APLS相关TMA急性发作期间常合并高血压,这对临床医生的一个极大的挑战。APLS相关TMA诊断的确立可以结合肾活检病理、APL水平、患者临床表现如妊娠相关并发症史、多次血栓事件包括动脉血栓和APS标准外表现。APLSN应进一步分为急性型和慢性型,血栓性微血管病变(TMA)是急性型APLSN的组织学特征,在动脉/小动脉和/或肾小球中可发现纤维蛋白微血栓。慢性型APLSN病变表现为动脉硬化、血管壁内膜细胞增生、纤维动脉闭塞、皮质萎缩、小动脉血管闭塞病变等。病理上,急性和慢性病变可共存于同一活检标本。在所有的抗磷脂抗体中,APSLN与狼疮抗凝物(LA)相关性最强。在灾难性抗磷脂抗体综合征(CAPS)中,肾脏病理可见到TMA的存在。
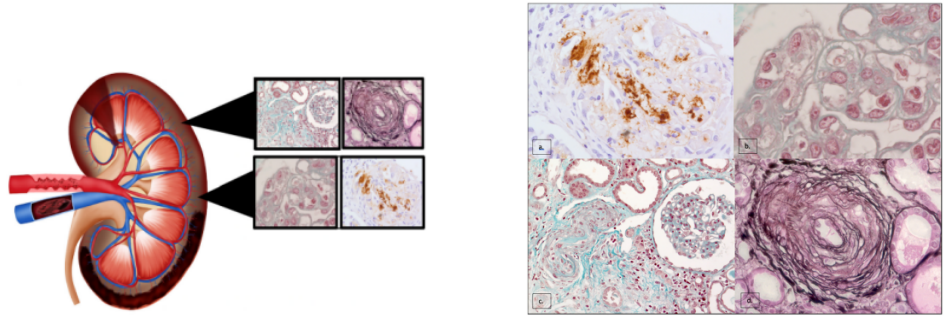
来自巴黎Tenon大学医院的组织学切片显示了APLSN的急性和慢性形式,慢性形式的内膜增生占主导,急性形式的TMA病变占主导。一些活检标本显示急性和慢性病变观察到的APLSN。a.抗cd61抗体(巨核细胞标记物)染色的肾小球TMA伴血小板血栓b.肾小球TMA伴GBM复制和亚内皮隙增宽。c.小动脉TMA d.慢性APLSN的动脉硬化。
APLS肾病的治疗
由于缺乏严格的随机对照研究,APLSN患者的管理一直存在争议。对于这些患者的治疗策略,目前尚无共识。然而,对于符合APLSN组织学诊断标准和符合Sydney APLS标准的患者,推荐使用维生素K拮抗剂进行抗凝治疗。对不完全符合Sydney APLS标准的患者的APLSN的管理尚不清楚。aPL检测呈阳性但无APS临床表现的患者通常使用每天100毫克的小剂量阿司匹林治疗。在一些研究(纳入对象为aPL滴度持续高滴度,但不符合悉尼标准的患者)中,羟氯喹和他汀类药物可使患者获益。EULAR建议: 对于不符合2006年Sydney标准的APLS高危患者,建议使用低剂量阿司匹林预防血栓形成。
静脉血栓患者使用维生素K拮抗剂进行抗凝期间,目标INR为2-3,动脉或复发性血栓患者INR为3-4。有关新型口服抗凝剂(NOAC)在静脉血栓APLS中的应用的前瞻性数据很少,而且证据不足。基于抗磷脂综合征患者利伐沙班治疗试验中观察到的相关数据,目前不推荐在高风险的三阳APLS患者中,或在有动脉或复发性血栓事件的患者中使用NOACs。建议将低分子量肝素(LMWH)作为所有潜在血栓事件(如手术或住院)的APL携带者的主要预防措施。由于致畸原因,在怀孕期间,无论是否有相关的APLSN,都可以用LMWH代替维生素K拮抗剂。临床医生应注意在从维生素K拮抗剂方案转为NAOC时,CAPS的风险是否增加。鉴于动脉高血压和蛋白尿的高发率,建议使用ACE抑制剂对APLSN患者进行肾脏保护性管理。在伴有继发性APLSN的系统性红斑狼疮患者中,除了抗凝治疗,可联合羟氯喹和免疫抑制剂。免疫抑制剂使用被发现在抑制抗磷脂抗体产生方面是有效的,但似乎并不能降低血栓栓塞风险。在APLS领域存在一些有希望的治疗方法,但目前均来自于病例报告或回顾性数据,尚缺乏充分的随机对照试验来验证其治疗潜力,Eculizumab、mTOR抑制剂和belimumab(BAFF抑制剂)是三种有希望的治疗药物。利妥昔单抗(抗CD20),已经在一项非随机的前瞻性研究中、Eculizumab在患有TMA的肾移植患者的队列以及几个难治性CAPS的病例中显示了疗效。
APLS肾病的预后
在原发性APLS患者中,肾脏预后的研究仍很匮乏。患者进展到终末期肾衰(ESKD)并不常见,因为前瞻性数据尚缺乏,接受抗凝治疗并诊断为APLSN的患者样本量小,以及这些患者随访中缺乏肾脏病理数据,抗凝治疗对APLSN患者肾脏结局的预后作用仍有待确定。尽管缺乏大型随机对照试验,抗凝仍然是APLSN治疗的基石。
参考文献
Scheen M, Adedjouma A, Esteve E, et al. Kidney disease in antiphospholipid antibody syndrome: Risk factors, pathophysiology and management. Autoimmun Rev. 2022;21(5):103072. doi:10.1016/j.autrev.2022.103072
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








怎么没有收藏功能
43