JAMA Oncol | 阿替利珠单抗联合贝伐珠单抗作为高肿瘤突变负荷的转移性非鳞状非小细胞肺癌患者的一线治疗:一项非随机对照试验
2024-02-17 daikun MedSci原创 发表于上海
该研究旨在评估阿替利珠单抗联合贝伐珠单抗在高TMB晚期非鳞状NSCLC患者中的临床疗效和安全性,联合方案在高TMB晚期非鳞状NSCLC患者中显示了有希望的临床疗效和持久的反应,同时安全性良好。
肿瘤微环境中的病理血管生成会阻止免疫细胞有效浸润肿瘤,增加对免疫检查点阻断的抵抗性,抗血管生成药物如VEGF抑制剂能够重新编程肿瘤微环境,增强免疫检查点抑制剂的效果,高TMB (≥10 mutations/megabase)与免疫检查点抑制剂的客观反应率、无进展生存期等临床指标相关,目前,尚无关于TMB与阿替利珠单抗联合贝伐珠单抗一线治疗高TMB晚期非鳞状NSCLC的生存获益相关性的前瞻性研究,通过II期非随机对照试验评估阿替利珠单抗联合贝伐珠单抗在高TMB晚期非鳞状NSCLC患者中的临床疗效和安全性。

方法
该研究为一项多中心、单臂、开放标签的II期非随机对照试验,纳入患者治疗初治的年龄≥18岁、病理证实的IIIB-IV期非鳞状NSCLC、ECOG评分0-1分、无已知EGFR/ALK/STK11/MDM2/ROS1基因变异、TMB≥10 mutations/megabase或≥16 mutations/megabase (血液样本),患者接受阿替利珠单抗1200mg + 贝伐珠单抗15mg/kg,每21天为一个周期,直至疾病进展或不可耐受毒性,主要终点:12个月无进展生存率,次要终点:总体生存率、客观反应率、反应持续时间等,探索性分析:TMB与疗效的相关性、预测生物标志物等。数据截止时间:2022年2月28日。
纳入人群
该研究纳入了38名患者,全部为IIIB-IV期非鳞状非小细胞肺癌,平均年龄为63.7岁,73.7%为男性,94.7%有吸烟史,中位吸烟量为45包年,ECOG评分:42.1%为0分,57.9%为1分,92.1%为腺癌,50.0%有高血压,44.7%有血脂异常,31.6%有慢性阻塞性肺病,28.9%有糖尿病,所有患者TMB均≥10 mutations/megabase或≥16 mutations/megabase (血液样本),无已知EGFR/ALK/STK11/MDM2/ROS1基因变异。

研究结果
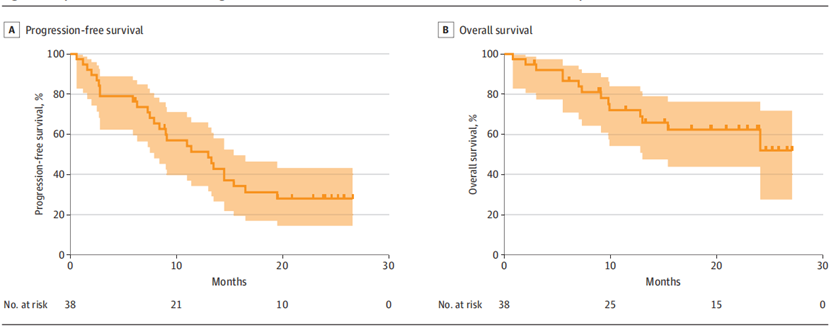
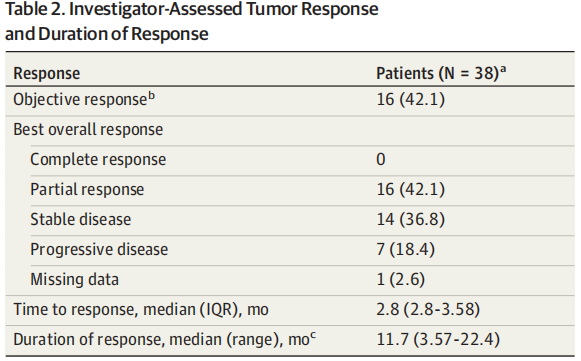
主要终点:12个月的无进展生存率为51.3%,达到研究的主要终点,表明该联合方案在控制肿瘤生长方面取得了显著的效果。次要终点:6个月和12个月的总体生存率分别达到86.6%和72.0%,显示出该方案在延长患者生存方面也有明显优势,42.1%的客观反应率显示,该联合方案对部分患者肿瘤的缩小和控制效果明显,11.7个月的中位反应持续时间表明,联合方案所引起的反应是持久的,未发现TMB水平与无进展生存率、总体生存率、客观反应率等疗效指标存在明显相关性,未发现与疗效相关的预测性生物标志物。
安全性
所有级别的不良反应中,阿替利珠单抗组最常见的是疲劳、瘙痒、乏食和腹泻,而贝伐珠单抗组最常见的是高血压和蛋白尿,3-4级不良反应中,阿替利珠单抗组包括肝功能异常、关节痛、关节炎、腹泻和胰酶升高,而贝伐珠单抗组包括高血压、肝功能异常、肛瘘、心肌梗死和血管病变,治疗中断和剂量调整主要出现在3-4级不良反应中,研究认为阿替利珠单抗联合贝伐珠单抗在该人群中的安全性良好,未发现新的安全信号。
结论
阿替利珠单抗联合贝伐珠单抗在高TMB晚期非鳞状NSCLC患者中显示了有希望的临床疗效和持久的反应,同时安全性良好,12个月无进展生存率为51.3%,符合研究的主要终点,6个月和12个月的总体生存率分别达到86.6%和72.0%,客观反应率为42.1%,反应持续时间为11.7个月,阿替利珠单抗联合贝伐珠单抗可能成为高TMB晚期非鳞状NSCLC患者的标准一线治疗方案,TMB水平与疗效无关,未发现与疗效相关的预测性生物标志物,研究存在局限性,需要进一步研究来验证这一联合方案的优越性。
原始出处
Provencio M, Ortega AL, Coves-Sarto J, et al. Atezolizumab Plus Bevacizumab as First-line Treatment for Patients With Metastatic Nonsquamous Non–Small Cell Lung Cancer With High Tumor Mutation Burden: A Nonrandomized Controlled Trial. JAMA Oncol. 2023;9(3):344–353. doi:10.1001/jamaoncol.2022.5959.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#贝伐珠单抗# #阿替利珠单抗# #高肿瘤突变负荷#
21