Science子刊:AD病原体假说新3D模型:疱疹病毒是AD独立诱因
2023-02-18 brainnew神内神外 brainnew神内神外 发表于安徽省
自然散发性AD,因病因复杂不确定以及疾病进展缓慢,对体外人类模型提出了巨大的挑战。迄今为止,尚未有研究利用3D人类脑模型表现疱疹病毒对AD的直接因果关系。
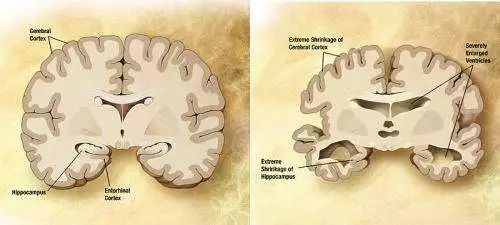
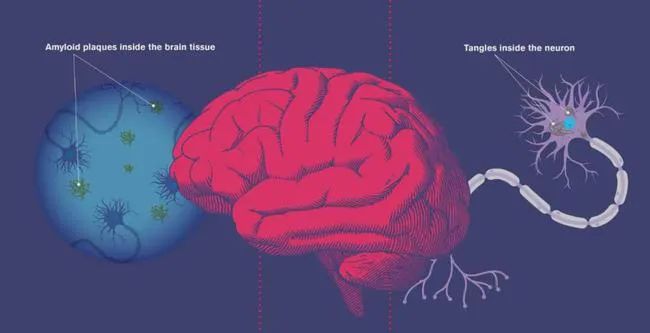
 阿尔茨海默症(AD)是导致认知下降、记忆丢失最终影响日常执行功能的一种神经退行性障碍。其标志性特征如大脑中老年斑的形成、神经纤维的缠结、神经胶质细胞增多以及炎症反应等。然而,其原因依然是未解之谜。越来越多的证据表明病原体参与了AD的发展,其中I型单纯疱疹病毒(herpes simplex virus type I , HSV-1)作为潜在的致AD病原体受到了越来越多的关注。美国塔夫茨大学David L. Kaplan 团队描述了一种多学科融合制作生理相关人体组织的方法,利用人类诱导的神经干细胞(human-induced neural stem cells, hiNSCs)和HSV-1感染生物工程改造的3D大脑模型来研究AD。其成果发表在ScienceAdvances杂志上。该文章提供了由疱疹引起的AD模型,该模型模拟了在完全没有任何外源性AD介质下具有多细胞淀粉样斑块形成、神经胶质增生、神经炎症及功能降低等特征病理改变,为未来治疗AD潜在下游药物靶点的鉴定提供新模型。
阿尔茨海默症(AD)是导致认知下降、记忆丢失最终影响日常执行功能的一种神经退行性障碍。其标志性特征如大脑中老年斑的形成、神经纤维的缠结、神经胶质细胞增多以及炎症反应等。然而,其原因依然是未解之谜。越来越多的证据表明病原体参与了AD的发展,其中I型单纯疱疹病毒(herpes simplex virus type I , HSV-1)作为潜在的致AD病原体受到了越来越多的关注。美国塔夫茨大学David L. Kaplan 团队描述了一种多学科融合制作生理相关人体组织的方法,利用人类诱导的神经干细胞(human-induced neural stem cells, hiNSCs)和HSV-1感染生物工程改造的3D大脑模型来研究AD。其成果发表在ScienceAdvances杂志上。该文章提供了由疱疹引起的AD模型,该模型模拟了在完全没有任何外源性AD介质下具有多细胞淀粉样斑块形成、神经胶质增生、神经炎症及功能降低等特征病理改变,为未来治疗AD潜在下游药物靶点的鉴定提供新模型。
1AD流行病学及病原体假说
AD是一种进展性神经退行性疾病,造成严重的认知下降、早期记忆缺失、语言功能受损、最终引起日常活动能力丧失。中国是痴呆患者最多的国家,发病率约占中国总人口的6.19%(World Alzheimer Report, 2015),占世界痴呆人口总数的25%。随着人口老龄化的不断加剧,加上目前并无医疗手段治愈或至少阻止这种破坏性疾病的进展,全球AD的罹患率及造成的家庭社会负担均将极速增加。对病因的探索是制定治疗疾病策略的基石,人类疾病相关离体组织模型的建立为病因的探索提供了探索及可操作验证平台。
淀粉样斑块蛋白(Aβ)的沉积作为AD最重要的标志性特征之一,约90%属于Aβ1-40亚型,另外10%为Aβ1-42亚型。其中Aβ1-42亚型以单体或寡聚物形式存在。实事上,Aβ1-42单体具有神经保护、抵抗由营养匮乏和兴奋性毒性造成的神经元失活的作用,而这些单体聚集成寡聚体,生成有助于老年斑形成的原纤维,最终形成老年斑并与AD中神经毒性相关。
越来越多的证据表明病原体参与了散发性AD的发展。AD病原体假说提出,各种各样的病原体可作为诱因来诱导和/或导致Aβ1-42单体的积累。很多病原体能够避开宿主特别是免疫功能低下和/或老年人的免疫应答并渗透进入大脑,造成潜伏及潜在的慢性感染。反过来,这些病原体继续诱发反应性神经胶质增生和促炎反应,最终导致进展性神经变性和痴呆。HSV-1是一种嗜神经性双链DNA病毒,通常以潜伏状态存在于整个周围神经系统中,拥有渗透入血脑屏障(blood-brain barrier,BBB)的能力,越来越多的证据表明HSV-1在AD的发展中具有潜在的因果关系。
2HSV-1感染诱导的hiNSCs病理变化
暴露在低水平HSV-1下可引起hiNSCs显著细胞形态学改变,24小时后即可检测出被感染的细胞,表达HSV-1感染的细胞数量随时间增多,且这些细胞具有感染其他细胞的能力。高水平HSV-1感染引起细胞凋亡。培养4天后的hiNSCs利用HSV-1感染3天后,Aβ1-42含量特异性显著增加,促进Aβ过表达的早老基因(presenilins 1/2, PSEN1/2)表达升高,神经胶质增生且神经炎症过度活化。但是值得讨论的是,裂解形成Aβ产物的淀粉样前体蛋白(amyloid precursor protein,APP)及促进APP裂解的β-分泌酶(enzyme β-secretase,BACE1)的含量却显著降低(图1)。一方面,BACE1的降低可能是hiNSCs 分化受损的结果;另一方面,BACE1是介导APP水解的第一阶段,反应时间早;而且,BACE1在APP以外的其他功能中起作用,相同的,其他具有相同或相似生理作用的酶类或许在HSV-1感染模型中起到了增加Aβ的功能。多方面的原因导致BACE1含量在HSV-1感染的hiNSCs模型中含量降低。

图1 HSV-1感染导致AD介质的特异性调节及神经退行性病理改变
3VCV降低HSV-1诱导的散发性AD表型
伐昔洛韦(VCV)是治疗HSV-1感染最常用的抗病毒药物,直接靶向被感染细胞的DNA复制。本研究中,VCV导致HSV-1感染显著减少,同时显著降低Aβ阳性纤维斑块状形成物(PLFs)平均数量及大小,并几乎将AD所有标志物如APP,BACE1,PSEN1和PSEN2恢复到对照值。VCV治疗由HSV-1感染的hiNSCs还可减少神经胶质瘤和神经炎症(图2)。


图2. VCV降低HSV-1感染hiNSCs引起的AD样表型
4HSV-1诱导的hiNSC 3D脑组织生理表型
甜甜圈样 hiNSC 3D脑组织模型培育4周后,利用低水平HSV-1 感染1周,模型组织出现神经元缺失,Aβ阳性并出现PLFs,BACE1含量降低,PSEN1/2上调,胶质及神经炎性活化等与hiNSC细胞相同的AD样表型。表明该3D模型可很好的模拟疱疹病毒诱导的AD。 图3. 低水平HSV-1感染的hiNSC 3D脑模型表现出AD样表型
图3. 低水平HSV-1感染的hiNSC 3D脑模型表现出AD样表型
5总结及展望
自然散发性AD,因病因复杂不确定以及疾病进展缓慢,对体外人类模型提出了巨大的挑战。迄今为止,尚未有研究利用3D人类脑模型表现疱疹病毒对AD的直接因果关系。本文将hiNSC技术与HSV-1生物工程结合,首次建立快速、可再生、稳健、有散发性AD生理相关的3D人类脑组织模型,该模型涵盖Aβ斑块形成,神经元丢失,神经胶质细胞过度活化,神经炎症以及神经网络功能性降低等多方面人类疾病的生理表现,解决了研究散发AD疾病的关键需求。本研究表明HSV-1感染导致该模型较大、多细胞、PLFs,内源性已知AD介质PSEN1和PSEN2的表达升高,并诱发神经胶质反应及神经炎症水平升高,而抗病毒药物可以减少这种AD样表型,提示抗病毒干预措施可能对临床AD的预防和/或治疗有效。该模型将为进一步阐明散发性AD机理提供平台,最终服务于开发更有效的策略来治疗这种复杂且具有破坏性的疾病。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言