Nature证实,不是β淀粉样蛋白导致阿尔兹海默症!
2022-06-09 四五七 MedSci原创
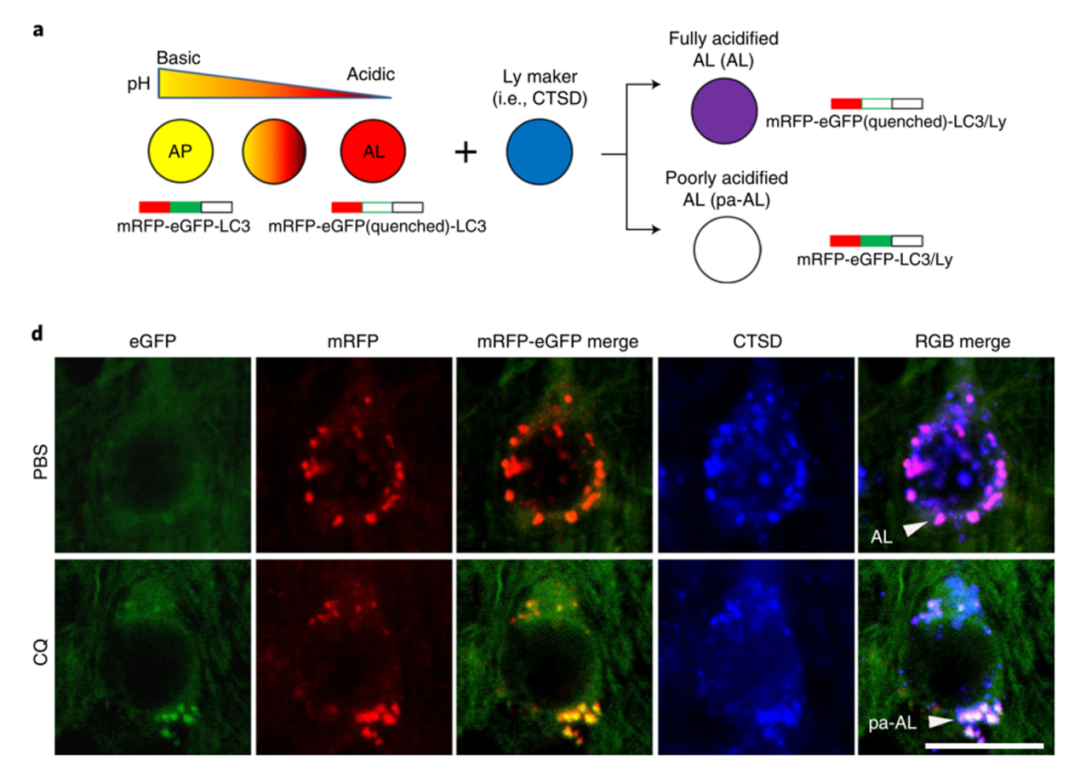
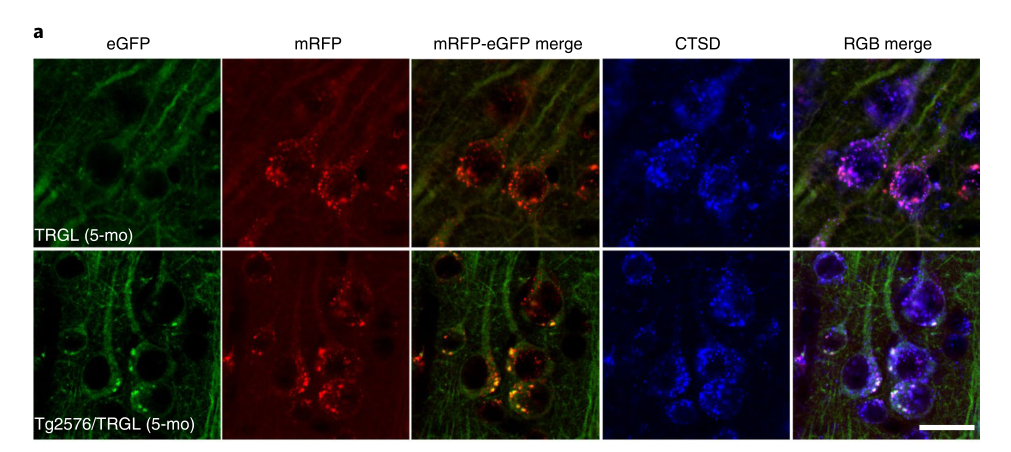
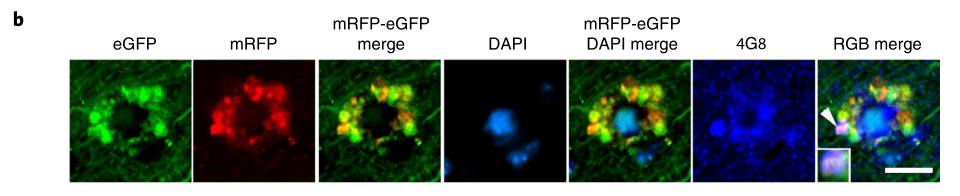
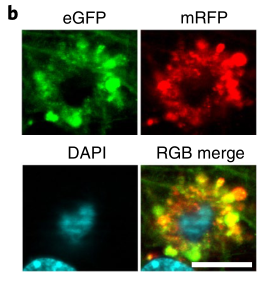
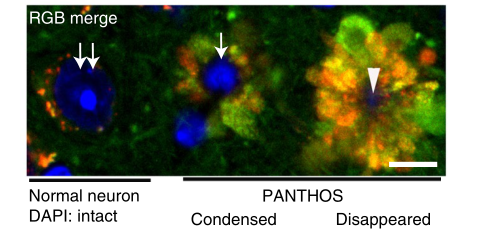
Nature子刊:颠覆了我们对阿尔兹海默症“先有细胞外淀粉样斑块形成,后有神经细胞死亡”的传统印象,提出“先有神经细胞死亡,后有细胞外淀粉样斑块出现”。
参考资料: [1]Lee JH, Yang DS, Goulbourne CN, et al. Faulty autolysosome acidification in Alzheimer's disease mouse models induces autophagic build-up of Aβ in neurons, yielding senile plaques [published online ahead of print, 2022 Jun 2]. Nat Neurosci. 2022;10.1038/s41593-022-01084-8. doi:10.1038/s41593-022-01084-8 [2]Lie PPY, Yoo L, Goulbourne CN, et al. Axonal transport of late endosomes and amphisomes is selectively modulated by local Ca2+ efflux and disrupted by PSEN1 loss of function. Sci Adv. 2022;8(17):eabj5716. doi:10.1126/sciadv.abj5716
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#Nat#
39
而且最近爆出来的Aβ56文章涉嫌学术造假,虽然不能说其他的亚型没用,但至少这么多年了,研究没进展,药物没疗效,就该换个思路了
50
有道理,久治不愈一定另有原因!
43
哇,这真是巨大的进展
47
(⊙o⊙)哇噻! 顿开茅塞,好文!
45
哇喔😯,真的是顛覆以前的看法
44
新的AD潜在治疗靶点
23
期待临床数据
39
#阿尔兹海默#
33
#淀粉样蛋白#
54