“渐冻人”孤儿药依达拉奉来了 国内药企如何应对?
2019-10-25 蔡德山 米内网
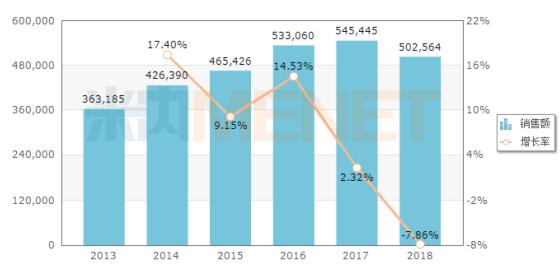
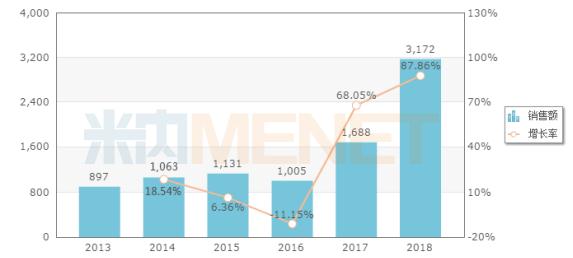
2019年7月25日,国家药监局批准了田边三菱制药的依达拉奉(Edaravone)100ml:30mg注射液。2019年4月12日,田边三菱制药以进口5.1类提交依达拉奉氯化钠注射液上市申请获得CDE承办受理,6月21日以“罕见病用药”为由拟纳入优先审评。虽然依达拉奉用于治疗ALS的作用机制尚不明确,但是全球渐冻人症治疗的最新药物。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言