Cell子刊:CRISPR直击HIV感染的预防和治愈
2016-10-31 佚名 生物谷
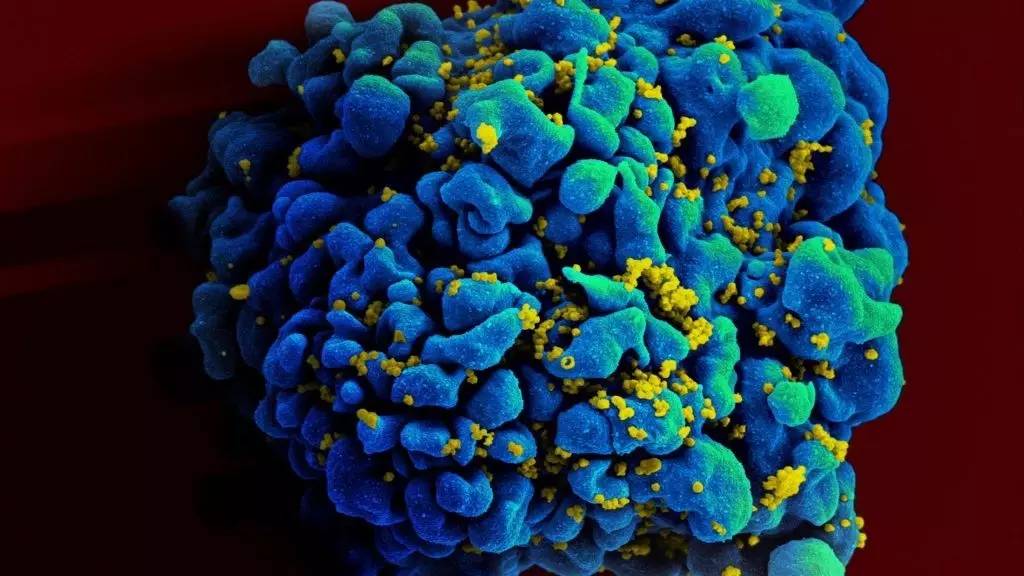
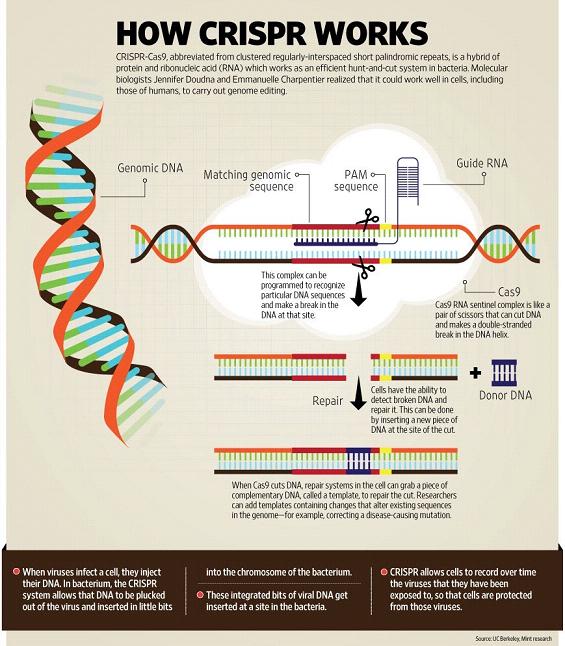
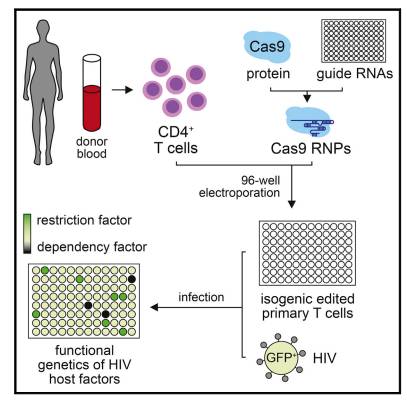
CRISPR是最近备受推崇的基因组编辑技术,它能够高效而精准地编辑基因组中几乎所有的序列,这将大大促进疾病研究和新疗法开发。著名科学期刊《Cell Reports》日前发布了一项新成果,科学家利用CRISPR/Cas9基因编辑系统,在人体免疫T细胞内对45个与HIV入侵宿主相关的基因进行特殊编辑分析,甄别出了其中某些基因经编辑改造发生突变后,可保护T细胞免受HIV病毒的侵入、整合、转染。这对于彻底
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Cell#
31
#CEL#
26
#CRISPR#
31