白细胞介素家族大汇总!
2022-11-22 癌图腾 癌图腾
白细胞介素,是由多种细胞产生并作用于多种细胞的一类细胞因子,因最初由白细胞产生又在白细胞间发挥作用,因此而得名,今天就来扒一扒它的生物学活性及其临床意义,希望对大家的研究有所启示。
白细胞介素,是由多种细胞产生并作用于多种细胞的一类细胞因子,因最初由白细胞产生又在白细胞间发挥作用,因此而得名,今天就来扒一扒它的生物学活性及其临床意义,希望对大家的研究有所启示。
主要由活化的单核巨噬细胞产生,属于白细胞介素-1家族,该家族包括11种白细胞介素。
【生物学活性】
1.局部作用局部低浓度的IL-1主要发挥免疫调节作用。
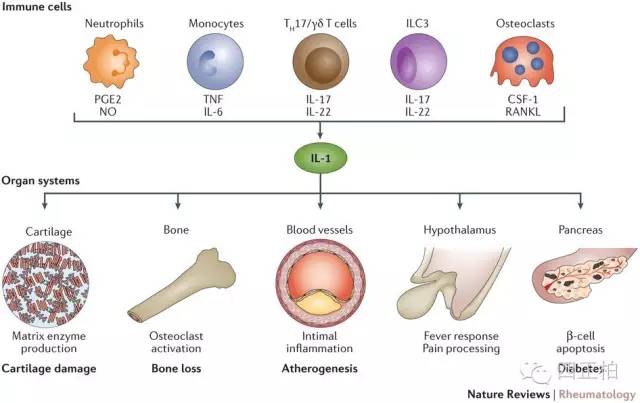
2.全身性作用动物实验证明,IL-1的大量分泌或注射可以通过血循环引起全身反应。
IL-1虽未广泛用于人体研究,但其对免疫系统的特殊作用使它在临床应用方面具有诱人的前景。另外,由于IL-1也参与机体的多种病理过程,所以研究IL-1抑制物可能也具有实际意义。现已克隆出IL-1受体拮抗剂(IL-1 receptor antagonist,IL-1RA),该物质可在体内外封闭IL-1的活性,是一种较理想的IL-1封闭因子。
【临床意义】
IL-1是重要的炎性介质之一,也是一种热原质成分,具有致热和介导炎症的作用。它主要在细胞免疫激活中发挥调节作用。IL-1受各种刺激因子(包括抗原、内毒素、细菌及病毒等)所诱导,在急性和慢性炎症的致病过程发挥重要作用,并与糖尿病、类风湿关节炎和牙周炎的病理过程密切相关。IL-1参与机体造血系统、神经、内分泌系统的反应,以及某些抗肿瘤的病理生理过程,它还介导急性髓性白血病、急性淋巴细胞白血病及多发性骨髓瘤的发病机制中,IL-1测定依据是它对胸腺细胞的影响。监测IL-1的释放有助于了解机体的免疫调节能力,可为疾病的诊断、疗效观察及预后判断等提供一项可靠依据。
-
IL-1升高在某些自身免疫性炎症反应,如类风湿性关节炎时IL-1参与了关节滑膜、软骨的病理损伤过程,在多种关节炎的关节液中可测出高水平IL-1,在结核和风湿等疾病时血中IL-1升高。
2. IL-1水平的高低在许多急性炎症疾病中可作为预后的重要评价指标。
3. IL-1降低在再生障碍性贫血患者,单核细胞产生IL-1能力明显降低。老龄人或癌症患者外周血中单核细胞产生IL-1能力也低于正常人,因而在感染后不易出现发热等临床症状。
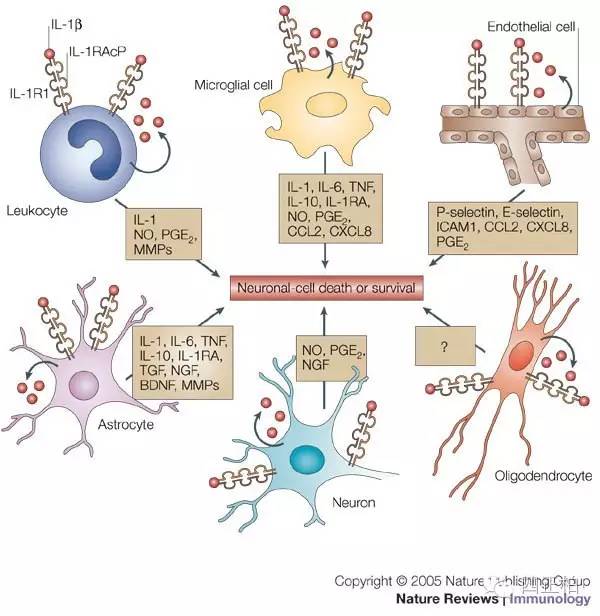
4. 研究表明,IL-1对神经系统伤后修复起调节作用,受伤部位IL-1的浓度高低直接影响受损神经元细胞的修复或诱导细胞凋亡。
又称T细胞生长因子,TCGF。主要由T细胞产生。
【生物活性】
- 刺激T细胞生长:各种刺激物活化的T细胞一般不能在体外培养中长期存活,加入IL-2则能其长期持续增殖,因此IL-2曾被命名为T细胞生长因子(T cell growth factor,TCGF)。静止的T细胞表面不表达IL-2R,对IL-2没有反应;受丝裂原或其它刺激活化后T细胞才能表达IL-2R,成为IL-2的靶细胞;而IL-2又可诱导靶细胞增加IL-2R的表达。在活体内,IL-2对CD4+ T细胞的作用是通过自分泌途径实现的,因为活化的CD4+ T细胞能够产生大量的IL-2;而CD8+ T细胞则通过旁分泌途径来维持细胞的生长。IL-2R在T细胞上的表达是一次性的,一般在活化后2~3天达到高峰,6~10天左右消失。随着IL-2R的消失,T细胞即失去对IL-2的反应能力。因此若要维持正常T细胞在体外长期生长,必须不断地用丝裂原或其它刺激物去刺激T细胞,以维持IL-2R的表达。

2. 诱导细胞毒作用:
3. 对B细胞的作用:IL-2对B细胞的生长及分化均有一定的促进作用。活化的或恶变的B细胞表面表达高亲和力IL-2R,但是密度较低;较高密度的IL-2可诱导B细胞生长繁殖,促进抗体分泌,并诱使B细胞由分泌IgM向着分泌IgG2转换。
4. 对巨噬细胞的作用:人类单核-巨噬细胞表面在正常时有少量的IL-2Rβ链表达,但是受到IL-2、 IFN-γ或其它活化因子作用后,可表达高亲和力IL-2R。单核-巨噬细胞受到IL-2的持续作用后,其抗原递呈能力、杀菌力、细胞毒性均明显增强,分泌某些细胞因子的能力也得到加强。
【IL-2的临床意义】
由于IL-2能诱导和增强细胞毒活性,目前应用IL-2治疗某些疾病、特别是对肿瘤治疗的研究得到了广泛开展,单独使用IL-2或与LAK细胞联合使用治疗肿瘤取得了一定的疗效;还可望用于病毒感染、免疫缺陷病及自身免疫病的治疗。
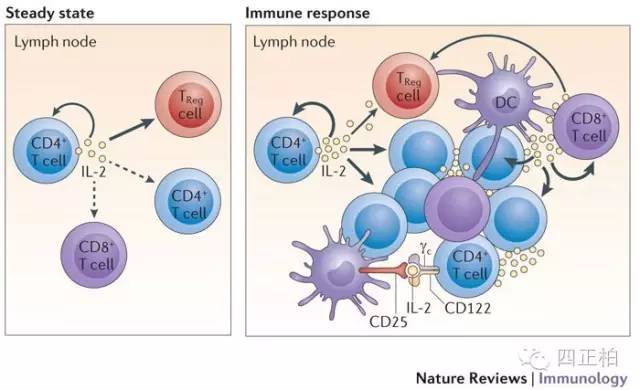
但IL-2的副作用也日益引起人们的注意:IL-2可引起发热、呕吐等一般症状,还可导致水盐代谢紊乱和肾、肝、心、肺等功能异常;最常见、最严重的是毛细血管渗漏综合征,使患者不得不终止治疗。IL-2的副作用常与IL-2的剂量及用药时间呈相关,停止用药后症状多迅速减轻或消失。IL-2引起副作用的机制是多方面的,但主要是间接性的,即IL-2诱导产生的某些因子或杀伤性细胞起着重要作用;现已知LAK细胞可通过溶解血管内组织而导致多种副作用。给予适当药物(如吲哚美辛、哌替啶、对乙酰基氨酚等)、采取联合用药、改进给药方式(如少量多次短时间输注)和给药途径(如改全身用药为肿瘤局部用药)等将有效地减轻不良反应。
白细胞介素3(Interleukin-3,IL-3)又称多集落刺激因子(Multicolony stimulationfactor,Multi-CSF)。目前研究最多的是人IL-3(hIL-3)和小鼠IL-3(mIL-3)。
【生物活性】
1、造血刺激因子的活性 IL-3是主要的早期造血生长因子,对造血调控起着极其重要的作用。IL-3主要作用于早期造血祖细胞,促进其增殖分化。晚期与造血生长因子红细胞生成素(EPO)、GM-CSF(粒细胞巨噬细胞集落刺激因子)、TPO(血小板生成素)共同作用,可促进髓系造血干细胞(THSC)、粒-单系祖细胞(CFU-GM)、粒系祖细胞(CFU-G)、巨噬系祖细胞(CFU-M)、巨核系祖细胞(CFU-Meg)、嗜酸性祖细胞(CFU-EQ)、嗜碱性祖细胞(CFU-Ba)、红系祖细胞(CFU-E)集落的形成。IL-3对于体内造血也有重要作用。
2、细胞活化因子的作用 激活嗜酸性粒细胞的吞噬功能及其细胞毒作用;促进嗜碱性细胞胞浆内组胺颗粒的释放;通过协助激活单核细胞中TNF基因的表达而激活单核细胞的杀肿瘤细胞作用(ADCC)。这种作用是由TNF介导的IL-3、GM-CSF能激活单核细胞中TNF基因的表达,至于单核细胞中TNF的释放还需要其它的信号刺激。IL-3还能促进成熟的嗜酸粒细胞和单核细胞的吞噬功能,刺激细胞产生多种内源性细胞因子(TNF-α,IL-6)等。
3、启动骨髓白血病细胞的生长分化 IL-3能支持从慢性髓性白血病病人血中分离的胚泡细胞增殖,同时还能启动这些集落形成后期的分化。
4、IL-3对淋巴细胞的作用 IL-3促进外周血T细胞的增殖。IL-3是激活B细胞分化后期的生长因子,在IL-2存在的条件下,IL-3能促进激活的B细胞增殖及分化。在IL-3刺激2-3天后,IL-3协同IL-2促进B细胞增殖。IL-3还能诱导激活的B细胞分泌lgG,促进白血病人B细胞前体的增殖及分化。
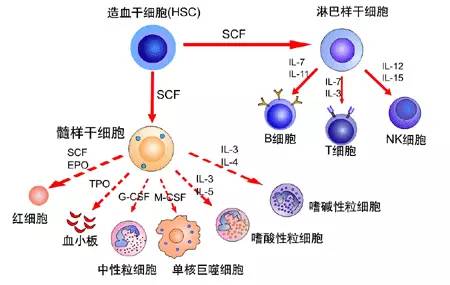
【临床应用】
在IL-3的诸多临床应用中,IL-3对骨髓造血功能的作用最为显著。IL-3对骨髓基质细胞的生长具有刺激作用,能促进异基因骨髓移植后造血微环境的重建。IL-3与GM-CSF、G-CSF、M-CSF或EPO合用可最适地刺激血细胞和血小板产生,能在化疗、放疗引起骨髓抑制时重建骨髓功能,并能改善再生障碍性贫血状态。 成纤维细胞介导的IL-3基因治疗能显著加快骨髓移植后造血重建过程,从而可能减少与之相关的感染、出血等严重并发症发生率,提高骨髓移植成功率及增加宿主对化疗、放疗耐受量。
有研究表明,新型细胞生长因子受体激活剂:SC55496(由高亲和力的人IL-3受体配基相似物组成)、MPO(由活化的人IL-3和G-CSF受体组成)、PMP(由人IL-3和c-mpl受体组成),能刺激多系造血干细胞生长因子,已应用于临床试验。这种结合物可增加血小板和嗜中性粒细胞的活性,适用于治疗化疗后骨髓消融,它。此外,商业化的IL-3/GM-CSF的融合蛋白(商品名Pixy321)已完成Ⅰ期、Ⅱ期临床试验,其结果表明该融合蛋白可大量提高外周血祖细胞数量,改善血小板减少症,使多系骨髓抑制症状缓解,嗜中性粒细胞减少症亦明显缓解。
IL-3与其他细胞因子联合应用,能诱导、扩增树突状细胞(DC)的产生。DC具有典型的表型,并可以通过多种途径应用于肿瘤疫苗的研制,起到抗肿瘤作用。同时,IL-3基因疗法特别适用于配合化疗药物治疗中晚期肿瘤患者。将IL-3基因疗法与IL-6基因疗法联合应用,能更有效地促进化疗后造血功能的恢复,且可互相补充各自造血调控的不足,该法适用于肿瘤患者放化疗导致的造血损伤的恢复。
IL-3、IL-5和GM-CSF在哮喘炎症反应中的作用非常显著,能有效提高哮喘患者的支气管粘膜、肺泡灌洗液及外周血中这三种细胞因子水平。
主要由活化的T淋巴细胞、肥大细胞、嗜碱性粒细胞产生的一种多效性细胞因子。
【生物学活性】
IL-4活化细胞毒性T细胞,它被认为是典型的由TH2细胞产生的细胞因子,对T、B淋巴细胞的发育以及驱动体液免疫反应和抗体产生都是十分重要的。IL-4对B细胞、T细胞、肥大细胞、巨噬细胞和造血细胞都有免疫调节作用。
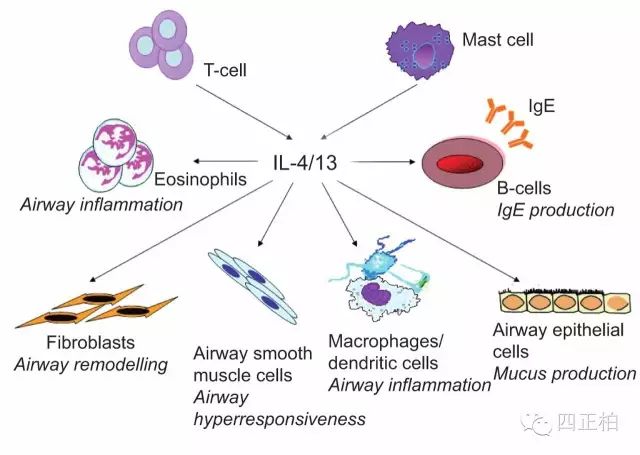
1、B细胞: 促进SAC或抗IgM预先刺激B细胞的增殖,这一生物学功能已被用来作为检测IL-4的生物学活性。IL-4促进B细胞MHCⅡ类抗原、FcεRⅡ/CD23和CD40的表达,并增强B细胞提呈抗原能力,使免疫系统对小量抗原刺激发生免疫应答。增加FcεRⅡ/CD23(IgE Fc 段低亲和力受体) 的表达,并释放可溶性CD23(sCD23)/IgE结合因子(IgE-BF),与mIgE阳性细胞结合并诱导其分化,可能与促进B细胞IgE的产生有关。IL-4提高LPS刺激小鼠B细胞 IgG1、IgE产生水平分别为8~10倍和10~100倍,但对IgG3分泌降低6~10倍,IgG2a、IgG2b和IgM有不同程度下降,对IgA产生无明显影响。IL-4增强IgG1和IgE水平的机理可能是:①使选择性刺激定向产生IgG1或IgE的B细胞的增殖和分化;②增加特异的重链稳定区(CH)Ig类的转换使Sμ-Sγ1结合,促进IgG1合成和分泌。IFN-γ对IL-4上述生物学功能有明显抑制作用。而IL-4则可抑制IFN-γ mRNA的转录和抑制IFN-γ诱导B细胞产生IgG2a。寄生虫感染时血清IgG1和IgE水平升高。此外,IL-4还可促进休止期B细胞的早期活化,从G0期进入G1期,细胞体积增大,并表达CD25。
2、T细胞: IL-4是T细胞自身分泌的生长因子,高剂量IL-4能诱导CD4-CD8+、CD4+CD8-或CD4-CD8-胸腺细胞的增殖。IL-4 增强PHA刺激T细胞释放GM-CSF和G-CSF。对人的杀伤细胞则有时表现为负调节作用,如在人MLC中IL-4选择性地促进Th增殖,同时伴有CTL、NK和LAK功能的降低。此外IL-4还能抑制IL-2所诱导的NK白血病细胞LAK活性。IL-4还可刺激CD3阴性NK细胞克隆的生长。
3、刺激肥大细胞增殖,并与IL-3有协同作用,尤其对于粘膜和结缔组织型肥大细胞体外生长是必需的。
4、促进巨噬细胞提呈抗原和杀伤肿瘤细胞,可能与调节MHCⅡ类抗原和FcR表达有关。IL-4与GM-CSF、IL-3和LPS有协同作用。IL-4可诱导外周血单核细胞分泌G-CSF和M-CSF,增强中性粒细胞介导的吞噬、杀伤活性和ADCC作用。
5、协同CSF刺激造血细胞的增殖,与G-CSF协同增强粒细胞集落形成,协同红细胞生成素(EPO)增强BFU-E的形成。
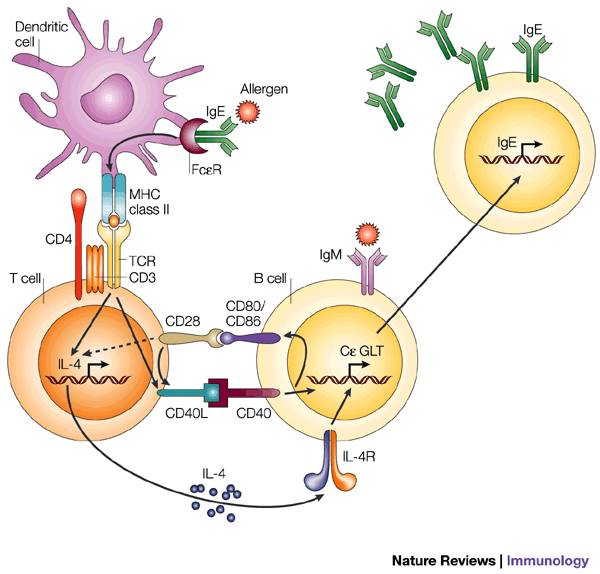
【临床应用】
IL-4是外分泌的糖蛋白,对于一些炎症和自身免疫疾病方面的研究具有很高的价值。由于体内、体外均证实IL-4可以抑制IL-1、IL-6和TNF分泌, 并促进IL-1ra产生,因此应用IL-4可能为治疗败血症休克提供一种新的方法。
IL-4可刺激气道上皮细胞产生粘液,还可激活气道平滑肌细胞引起气道高反应性,对于治疗过敏性炎症方面很有潜力。
IL-4在临床上涉及最多的是抗肿瘤治疗作用,已知IL-4受体在相当多的肿瘤细胞上表达,包括淋巴母细胞性白血病、多发性骨髓瘤、非霍奇金病、急性早幼粒细胞性白血病和某些实体瘤。IL-4作为肿瘤免疫调节剂已进入Ⅱ期临床试验。临床上,IL-4治疗霍奇金病、非霍奇金病、慢性淋巴细胞性白血病都有一定疗效。需要检查的人群:主要是肿瘤患者和相关疾病的患者需要检查。
一种多效性细胞因子,又名T细胞替代因子、嗜酸粒细胞集落刺激因子 1、嗜酸粒细胞分化因子等,主要由T细胞(1-4)生产。促进嗜酸性粒细胞分化、成熟、活化、迁移、存活。
【生物学活性】
与其它白细胞介素相比,IL-5生物学活性作用谱相对较窄。
嗜酸性粒细胞:促进骨髓中嗜酸性粒细胞的产生。IL-5转基因小鼠外周血、脾和骨髓有大量嗜酸性粒细胞,血清中可检测到IL-5。IL-5可活化嗜酸性粒细胞,促进其通过ADCC机制杀伤肿瘤细胞,通过调理作者用杀伤病原体,促进嗜酸性粒细胞超氧阴离子的产生,延长外周血中嗜酸性粒细胞的存活时间,促进嗜酸性粒细胞由IgG和IgA诱导的脱颗粒作用,增加嗜酸性粒细胞来源的神经毒素的释放,在粘膜免疫中有重要作用。
嗜碱性粒细胞:促进碱性粒细胞组胺和白三烯的产生,参与变态反应的发生。
B细胞:小鼠IL-5促进抗原刺激的B细胞分化为抗体产生细胞,主要作用于进入细胞增殖后期的B细胞,并增加活化B细胞IL-2R的表达,IL-5的这种刺激作用与IL-6功能相似。人IL-5对B细胞似无刺激作用。小鼠IL-5可促进IgA合成,其机制可能是:
(1)使mIgM阳性B细胞分化为mIgA阳性B细胞;
(2)促进IgA型B细胞的增殖和分化,成为分泌IgA的浆细胞。IL-4有协同IL-5促进IgA合成的作用。IL-5对IgM的分泌也有促进作用。
协同ConA或IL-2诱导的胸腺中细胞毒性T细胞前体分化为CTL。
【临床意义】
1. IL-5与嗜酸性粒细胞增多症以及某些变态反应性疾病的发病有关,寄生虫感染和变态反应发作时IL-5水平增高。抗IL-5人源化抗体治疗哮喘等过敏性疾病未见明显效果,但可减少嗜酸性粒细胞增多症病人嗜酸性粒细胞的循环数量。
2. IL-5是嗜酸性粒细胞的趋化剂,上调其粘附分子的表达,促进嗜酸性粒细胞同内皮细胞的粘附,此作用可能与慢性变态反应疾病所发生的组织损伤有关。
主要由单核巨噬细胞、 Th2细胞、血管内皮细胞、成纤维细胞产生。
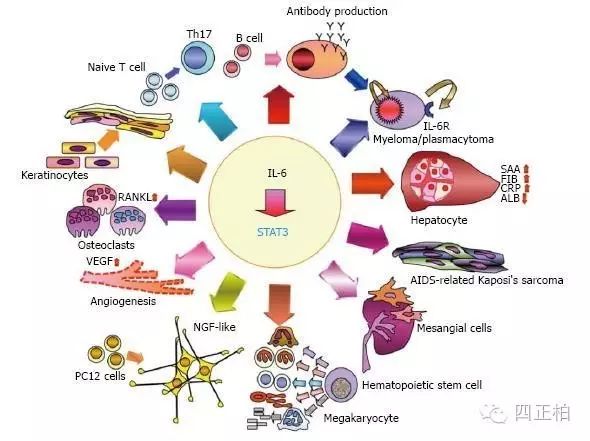
【生物学活性】
IL-6作用的靶细胞很多,包括巨噬细胞、肝细胞、静止的T细胞、活化的B细胞和浆细胞等;其生物效应也十分复杂,曾称为B细胞刺激因子2(bsf-2)、26KD蛋白、B细胞分化因子(bCDf)、肝细胞刺激因子(hsf)等。
(1)促进T细胞表面IL-2r的表达,增强IL-1和TNF对TH细胞的致有丝分裂作用。(2)作为肝细胞刺激因子,在感染或外伤引起的急性炎症反应中诱导急性期反应中诱导急性期反应蛋白的合成,其中以淀粉状蛋白a和c-反应蛋白增加尤为明显。
(3)促进B细胞增殖、分化并产生抗体;多发性骨髓瘤的恶变B细胞既能产生IL-6,又能对IL-6发生应答,提示IL-6可能作为这些细胞的自分泌性生长因子。
(4)IL-6具有抗瘤效应,IL-6 可直接或间接增强自然杀伤细胞(NK 细胞)及毒性 T 细胞的杀瘤活性。
(5)有效地促进TNF和IL-1诱导的恶病质;促进糖皮质激素合成;刺激破骨细胞活性和角质细胞生长;还能促进骨髓造血的功能。IL-6不能刺激相应细胞分泌其它细胞因子,在生理浓度下对免疫细胞的自分泌作用亦比较弱,提示其主要免疫学功能是加强其它细胞因子的效果。
IL-6强大的功能我们开篇就展示过了,这里我们再看看核心的:
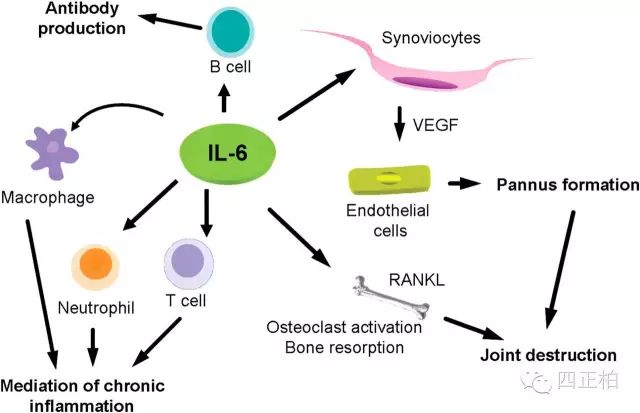
【临床意义】
IL-6能使B细胞前体成为产生抗体的细胞;和集落刺激因子协同,能促进原始骨髓源细胞的生长和分化,增强自然杀伤细胞的裂解功能。它可调节多种细胞的生长与分化,具有调节免疫应答、急性期反应及造血功能,并在机体的抗感染免疫反应中起重要作用。IL-6在多种疾病时有明显改变。IL-6表达失调可引起许多疾病,其临床表现主要为发病时IL-6水平增高。IL-6上升的水平与疾病的活动期、肿瘤的发展变化、排斥反应程度以及治疗效果都密切相关,因此,对病人体液中IL-6水平的检测可反映患者的病情变化。
1.多克隆B细胞激活或自身免疫性疾病,如心脏黏膜瘤、Costlemon病、类风湿性关节炎、系统性红斑狼疮、艾滋病、Reiter综合征、硬皮病、酒精性肝硬化、膜性增生性肾小球肾炎、银屑病等患者均表现有多克隆B细胞活化。
2. IL-6与肿瘤:浆细胞瘤、慢性淋巴细胞白血病、急性髓样白血病、多发性骨髓瘤、Lennet淋巴瘤、霍奇金病、心脏黏液瘤、宫颈癌等密切相关。
3. IL-6与神经系统疾病:阿尔兹海默症、舞蹈病、帕金森病、多发性硬化。
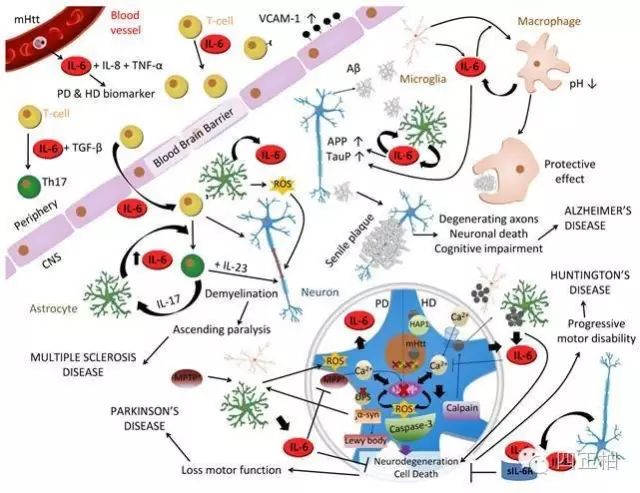
4.术后、烧伤、急性感染、器官移植排斥反应等疾病时,患者体液(血清、尿液、囊液、培养上清)中均可观察到IL-6明显升高。可由此了解患者的病情和疗效。
IL-7的靶细胞主要为淋巴细胞,对来自人或小鼠骨髓的B祖细胞、胸腺细胞及外周成熟的T细胞等均有促生长活性。
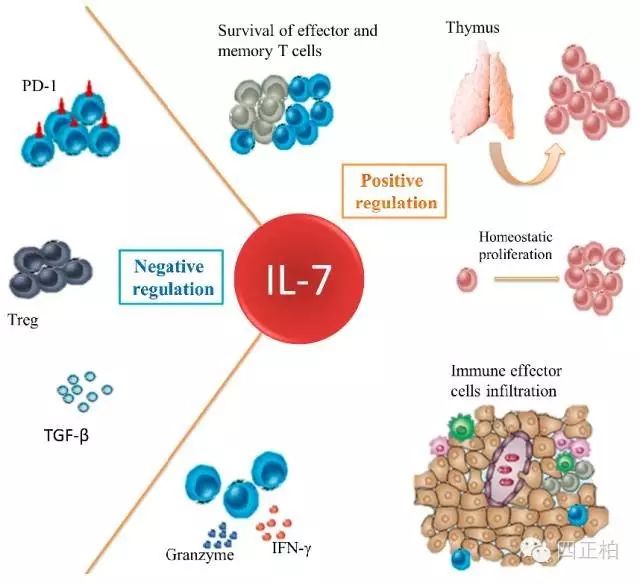
【生物学活性】
1.促进pre-B细胞生长:
① 来自新鲜骨髓的pre-B细胞用含IL-7的液体培养基培养2-5天后,细胞数量大大增加。
② 将pre-B细胞置于含IL-7的半固体琼脂培养基中培养,能生长成pre-B细胞的集落。
③ IL-7不能促进脾脏,淋巴结中成熟 B细胞的生长,表明 IL-7 能够促进pre-B 细胞生长而对成熟的B细胞无作用。
2. IL-7对胸腺细胞的作用:
① IL-7能单独诱导胸腺细胞增殖。
② 低剂量IL-2 (10u/ml)也能增强IL-7诱导的胸腺细胞增殖能力,所诱导的胸腺细胞为CD4+ CD8-、CD4-CD8+和CD4-CD8-,对CD4+CD8+胸腺细胞没有作用。
3. IL-7 促进T细胞生长的作用:合用IL-7 与ConA 时则能显著地诱导pro-T 细胞生长分化,且对CD4+ 和CD8+ 细胞皆有促增殖作用。
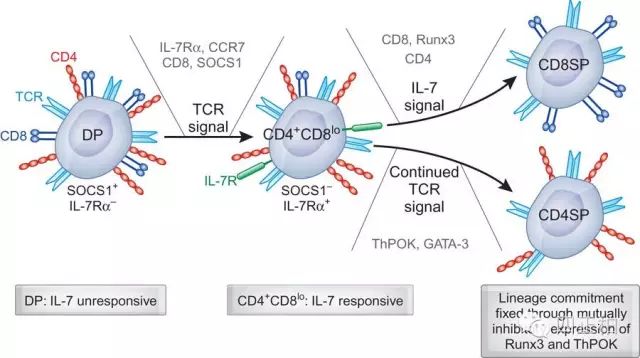
4. IL -7对杀伤性细胞的诱导作用:
IL-7不能增强抗原特异性CTL的杀伤活性,但它能诱导出一定水平的LAK活性,其诱导能力在诱导早期阶段 (如第7天时)弱于IL-2,但在诱导晚期阶段 (如第l5天时) 则强于IL-2。
【临床意义】
众多动物实验已经证明IL-7可以通过外周CD4+T细胞和CD8+T细胞的稳态增殖恢复免疫功能,能够在干细胞移植和化疗后促进免疫重建。另外,IL-7在应用疫苗,病毒感染和过继性细胞治疗时能够增强抗原特异性T细胞的反应。IL-7发挥效应的机制包括下调程序性细胞死亡因子1(PD-1)和细胞因子信号传导抑制蛋白3(SOCS3)的表达和上调抑制细胞凋亡基因BCL-2的表达,通过拮抗相关抑制网络的效应从而在急慢性病毒感染中发挥作用。
由Th1细胞分泌的细胞因子。趋化并激活中性粒细胞,促进中性粒细胞的溶酶体酶活性和吞噬作用。
【生物学活性】
IL-8是一种多功能因子,其生物学功能无种属特异性。早期发现中性粒细胞是其作用的靶细胞,能特异性趋化中性粒细胞进入炎性组织,促使其脱颗粒,产生超氧阴离子,引起呼吸暴发;并激活炎性细胞;促进急性期蛋白合成;引起发热、参与炎症病理性损害;促进炎性介质释放;促进成纤维细胞增殖-慢性炎症,所以在炎性反应中起重要作用。随着研究的深入,发现IL-8能作用于不同细胞,它能促进炎性反应进程、刺激血管的形成、促有丝分裂、调节宿主免疫功能等,与多种炎性反应性疾病、肿瘤、免疫性疾病的发生和发展密切相关。
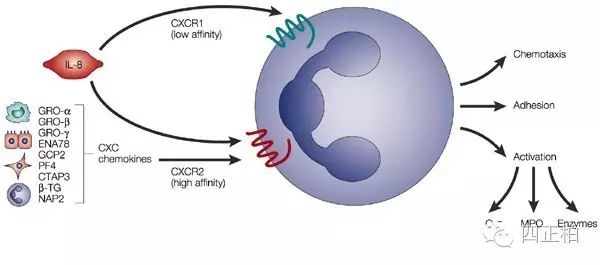
【在临床中的应用】
1. 在炎症方面的应用
(1)在溃疡性结肠炎的应用与治疗上,溃疡性结肠炎使IL-8的表达升高。炎症反应中的作用很大程度上是通过诱导IL-8来介导完成的炎症引起的肿胀应用激素可以迅速缓解。
(2)在某些与中性粒细胞积聚有关炎症和呼吸系统疾病的局部或血清患者中IL-8也有明显增高,如肺纤维化、呼吸窘迫综合征、慢性支气管炎、支气管扩张等IL-8水平升高,在肺内均可趋化并激活中性粒细胞、嗜酸性粒细胞、单核细胞和嗜碱性粒细胞,从而造成炎症介质的过量释放,诱发炎症反应和组织损伤。
(3)高铝暴露使癫痫患者癫痫大发作,体内IL-8的大量释放。
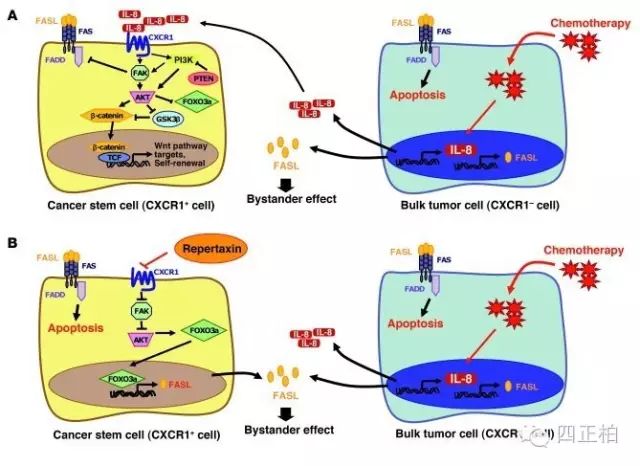
2. 在肿瘤方面的临床应用
抑制肿瘤细胞内的IL-8信号可提高肿瘤细胞对常规化疗的敏感性。抑制肿瘤内的IL-8信号传导可延缓肿瘤进程并可增加多种实体瘤对临床化疗的敏感度。
3. 在过敏反应方面的应用
国内外的一些研究均表明IL-8在过敏性紫癜血管炎中有表达,对过敏性紫癜的发生、发展过程发挥一定的作用。IL-8在过敏性紫癜患者血清中明显增高,治疗后下降明显,说明其在过敏性紫癜的发病中起到一定的作用。
4. 在神经根型颈椎病治疗
IL-8是急性期反应的主要细胞因子介体,是对炎性刺激反应时由单核细胞、巨噬细胞和内皮细胞释放的细胞因子。具有IL-8、P物质对疼痛及炎症的敏感性较之CRP更为敏感,常在CRP升高以前,就可发现IL-8、P物质升高。
5. 在精神分裂症方面的治疗
精神分裂症患者在治疗血清IL-8水平非常显著地高于正常人,经抗精神病药物治疗6周后与正常人组比较仍有显著性差异。
6. 醒脑静注射液对急性脑损伤患者IL-8的影响
醒脑静在促进意识恢复方面优于基础治疗。与治疗前比较,实验组治疗后IL-8明显降低。
7. 在妊高征肾病方面
妊高征肾病患者血清IL-8水平非常显著地高于正常孕妇组,其升高的机理可能是:IL-8对中性粒细胞、嗜碱性细胞具有较强的趋化作用,其主要生物学活性是趋化激活中性粒细胞,破坏血管内皮细胞、基底膜及内皮下肌层,导致血管内皮通透性增加,引起血管内皮细胞损伤之故。
人的IL-9(白细胞介素-9)又名P40,小鼠的IL-9(白细胞介素-9)又名P40、肥大细胞生长增强刺激剂、和T细胞生长因子Ⅲ。小鼠的IL-9作用于人细胞,人的IL-9对于小鼠细胞无活性。
【生物学活性】
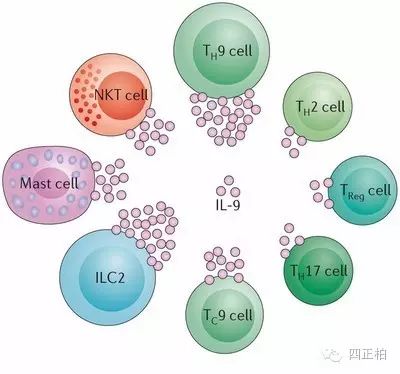
IL-9的免疫生物学功能有双向性,即它既能促进一些疾病的发生发展,又能抑制一些疾病的发展。目前研究认为,在超敏反应和自身免疫病中,IL-9是一种致病因子;而在寄生虫感染和皮肤移植中,IL-9能促进机体清除病原体以及移植物免疫耐受的形成。
1.超敏反应:以前人们一直认为肺部超敏反应由Th2细胞主导。最新实验证明,肺部超敏反应并非仅由Th2细胞介导,Th9细胞和NKT细胞也参与了此类疾病的发生发展。Th9细胞源性的IL-9能够促进肥大细胞的增殖并释放IL-13,IL-13能够进一步促进肺部粘液的分泌并引起气道高反应性;PU.1缺陷或PU.1和IL-25均缺限的小鼠气道炎症减轻。NKT细胞源性的IL-9能够介导肥大细胞进入肺部病灶。食物过敏时,Th2或Th9分泌的IL-9也会引起肥大细胞的增殖,并间接增强肠道的炎性浸润。
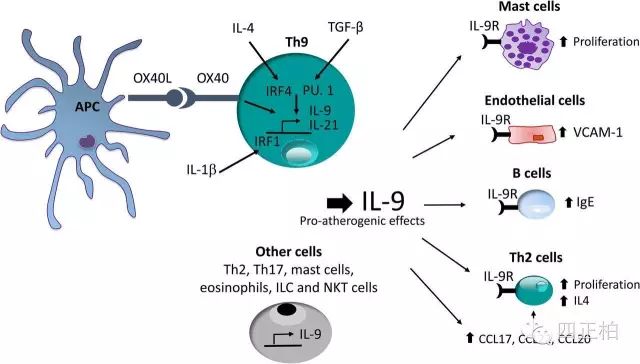
2.自身免疫性疾病:小鼠EAE模型(实验性自身免疫性脑脊髓炎模型)中,Th9和Th17细胞均能分泌IL-9。特异性阻断IL-9后,疾病进展减慢。虽然Elyaman称,IL-9能够抑制小鼠的炎症反应,但大多数免疫学家的实验表明,在EAE及其它自身免疫病中,IL-9具有促炎作用。例如,过继转移抗原诱导的Th9细胞能够促进EAE的炎症反应;小鼠口服免疫耐受剂后,IL-9的水平降低,EAE的炎症得到缓解;此外,Ⅰ型糖尿病患者血液中IL-9 +Th17细胞的数量增加。
3.寄生虫感染肠道寄生虫感染时,IL-9促进肥大细胞释放趋化因子和炎性介质,募集嗜酸性粒细胞,促进腺体细胞分泌粘液,加剧肠道浸润,增强平滑肌的收缩,促进肠道寄生虫的排出。鼠鞭虫感染时,细胞因子IL-9促进寄生虫排出肠腔,并有利于在局部组织形成肉芽肿包裹虫卵。肺部寄生虫(如曼森血吸虫)感染时,IL-9缺陷小鼠肺部粘液的分泌量以及肥大细胞的募集会显著减少,而肉芽肿的形成不受影响。
4.皮肤移植耐受皮肤移植时,IL-9能够加强移植物中Foxp3 +Treg细胞的免疫抑制作用,抑制宿主对移植皮肤的进行性免疫应答反应。Foxp3 + Treg细胞是分泌IL-9的主要细胞类型。IL-9通过肥大细胞的募集和脱颗粒来介导移植耐受。
【临床意义】
-
支气管哮喘急性发作期患者血浆IL-9水平与总IgE浓度呈正相关。老年支气管哮喘患者血浆中IL-9水平升高,与疾病的发生发展关系密切。
2.IL-9可能参与了川崎病(Kawasaki disease,KD)的早期发病过程,与疾病活动性有关。
3.在实验性自身免疫性脑脊髓炎和类风湿性关节炎动物,IL-9可以促进疾病发展,有致炎作用。近年研究发现IL-9有抑制Th1和Th17细胞反应的作用。IL-9、IL-10及TGF-β1均参与慢性乙型肝炎(CHB)的发病过程,IL-9及IL-10可能具有抑制炎症作用,其持续升高可能与CHB患者慢性感染状态有关。
4.Th9细胞相关细胞因子IL-9和转录因子PU.1参与过敏性鼻炎的发生发展过程。
5.白介素9(interleukin-9,IL-9)作为一种促炎细胞因子,在慢性气道炎症疾病中发挥重要作用。IL-9与自身变态反应的关系密切相关,特别表现再与支气管哮喘的发病过程中淋巴细胞和嗜酸粒细胞分泌IgE相关。鼻窦炎是一个有大量炎性细胞和炎性因子参与的局部炎症反应性疾病。研究发现,无论是慢性鼻-鼻窦炎(CRS)还是真菌性鼻窦炎患者,病变的鼻粘膜中均有IL-9蛋白和mRNA表达增加。目前认为,IL-9作为一种炎性细胞因子,使参与慢性炎症的炎性细胞再粘膜及粘膜下层聚集,从而使炎症持续存在。
6.IL-9的表达与促炎症因子肿瘤坏死因子TNF-α、IL-1、IL-17、干扰素-γ有一定的关联,这些细胞因子与IL-9共同介导炎症反应,参与自身免疫性疾病的病理过程。
也称为细胞因子合成抑制因子(CSIF),是一种多效性细胞因子,可以在多种类型细胞中发挥免疫抑制或免疫刺激的作用。
【生物学活性】
1、IL-10的单核细胞可有效调节单核/巨噬细胞功能。作为细胞介导免疫反应的负调节物,IL-10能抑制前列腺素E2和产炎性细胞因子包括TNF-α、IL-1、IL-6和IL-8的产生。IL-10可抑制人THO、Th-1、Th-2样T细胞克隆的增殖。
2、促进肥大细胞和胸腺细胞增殖,IL-10也是淋巴结、脾脏细胞生长的复合因子。
3、IL-10抑制炎症反应和细胞免疫反应,加强与适应性免疫和清除功能相关的耐受性,抑制由单核细胞和巨噬细胞产生的促炎因子。
4、提高B细胞的存活率,促进B细胞的增殖、MHCⅡ类抗原表达以及免疫球蛋白的分泌,并与Th2所产生的IL-4、IL-5有协同作用。
5、抑制NK细胞因子的产生。
6、抑制反应性氮氧化物的产生。
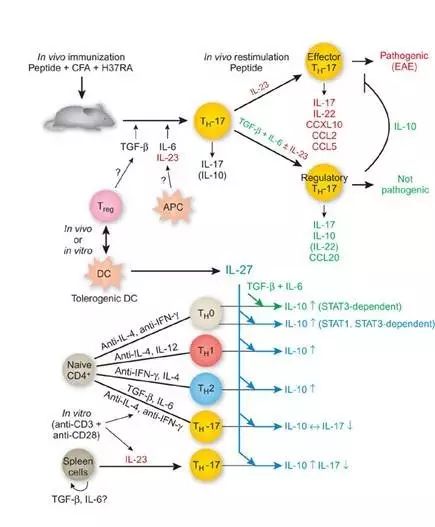
【临床意义】
IL-10具有双向免疫调节作用,IL-10可以通过抗原提呈细胞(APC)发挥免疫抑制,通过T细胞发挥负调节作用,在肿瘤环境中对免疫应答具有负向调节作用;另外,IL-10对T、B淋巴细胞具有刺激作用,并且在肿瘤环境中IL-10也能发挥刺激作用;IL-10的双向调节作用自从被发现起就一直被关注,它不仅影响免疫系统,而且可以通过调节生长因子、细胞因子影响许多病理生理过程,包括血管生成、肿瘤形成和感染,还能通过诱导调节性T细胞在外周耐受中建立作用;对克罗恩病、类风湿性关节炎银屑病、HCV感染、HIV感染等,IL-10都发挥着重要作用。
它是一种新的造血细胞因子。IL-11由人类骨髓基质细胞(成纤维细胞)及间质细胞分泌产生, 人甲状腺癌细胞 NTM-1亦能持续分泌 IL-11。
【生物学活性】
1、参与机体免疫反应
体外、体内试验证明, IL-11能参与原发性、继发性免疫反应, 调节特异性抗原抗体反应。在体外,IL-11 能促进IL-6依赖的浆细胞瘤细胞增殖和T细胞依赖性B细胞的发育。在含IL-11、EPO的培养基中原始细胞可分化成巨噬细胞。
2、参与造血调控
IL-11、G-CSF 、IL-6 协同IL-3刺激人类和鼠类巨核细胞集落形成;其中IL-11在巨核细胞生长、成熟中起着重要调节作用, 并能提高血小板数。IL-11 可特异性缩短造血干细胞细胞周期中的G0期,联合IL-4能促进原始造血前体细胞集落形成。协同IL-3或干细胞因子(SCF), IL-11 可使原始多系造血祖细胞扩增 , 同时可促进多系CFC, 红系爆式形成单位(BFU-C), 红系细胞形成单位(CFU-E)的分化。
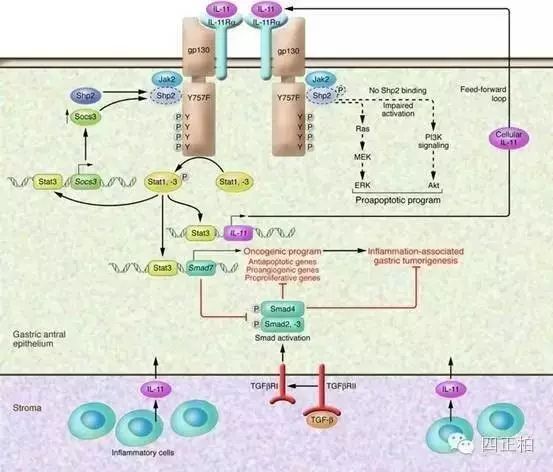
3、过度表达时的生理反应
Hawley等通过小鼠实验, 研究当人源IL-1过度表达时的生理表现。予受体小鼠致死剂量照射后进行小鼠骨髓移植, 其中供体小鼠骨髓细胞已被携带人源IL-11基因的逆转录病毒转染。经过一定时间的恢复, 受体小鼠高表达IL-11, 并出现一系列反应,包括:脂肪丢失、胸腺萎缩、血浆蛋白水平的转变、频发性眼睑炎、机体兴奋等。在受体小鼠外周血中, 出现持续的血小板水平增高, 脾脏中髓系祖细胞水平>20 倍, 但循环白血病细胞总数没有改变。
【临床应用】
化疗引起的骨髓抑制及与之相关的贫血、白细胞减少症和血小板减少是很多化疗药物的剂量限制性毒性。尽管几种生长因子的应用,如红细胞生长素、集落刺激因子的出现大大减轻了贫血及粒细胞减少症对患者的危害,但血小板减少却是一个一直都未解决的问题。虽然输注血小板可暂时缓解血小板减少,但这种作用仅是暂时的,同时还可能出现其他问题如感染、输血反应、抗体产生。因此,临床上对促进血小板生长因子的需要十分迫切。
在寻找血小板生长因子的过程中,人们陆续发现了TPO(促血小板生长素)、干细胞因子(c-kit片段)、IL-1、IL-3、IL-6、IL-11和GM-CSF,其中IL-11显示了较好的作用。重组人的IL-11(rhIL-11)由美国Genetics Institute(GI)公司研制成功,1997年11月经FDA批准上市,商品名为Neumega,它是目前治疗化疗导致的血小板减少症的惟一有效的药物。但在自体骨髓移植中,rhIL-11不能降低血小板输注事件的发生率,同时还会出现水肿和较高的心血管系统的不良反应。
主要的不良反应为水钠潴留,患者可出现周围性水肿、呼吸困难、疲乏,严重者出现胸水、腹水、心包积液。水钠潴留可导致血红蛋白、红细胞计数下降,有时患者还需输注红细胞。注射局部可出现疼痛、红肿,还有少数患者出现皮疹、厌食、暂时性视力模糊(由视神经盘水肿所致)、抗体形成、过敏等。部分患者出现心血管方面的不良反应,如心律失常、晕厥、心动过速、房颤等。
rhIL-11一般在化疗完成后6~24h开始皮下注射,剂量为50ug/kg,每日一次,连用14d,或直到血小板最低点过后计数≥100000/mm3方可停药。往往注射5~9d左右血小板数量开始上升,停止给药后连续7d血小板仍继续上升并于14d内恢复至基数水平。
虽然rhIL-11是目前唯一批准用于血小板减少症治疗的药物,但由于它对血小板生长的刺激程度仅为中等,同时,应用中又有一系列不良反应,因此人们还在不断研究以期开发出疗效更好、毒性更低的药物。目前正在进行研究的药物有融合蛋白PIXY321、C-mpl片段模拟胎、高度亲和的IL-3受体片段(IL-3-synthokine)等。也有学者试图联合应用几种有效药物综合治疗血小板减少症。
由树突状细胞(DC)、巨噬细胞、B淋巴细胞以及其他抗原递呈细胞(APC)产生。
【生物活性】
1、Th1/Th2 活性的作用调节
IL-12p70是细胞介导免疫中非常重要的细胞因子。其主要免疫调节作用是诱导早期辅助性T母细胞分化为Th1 细胞,并促进Th1 细胞的发育和增殖。辅助性T 细胞是细胞介导免疫应答和B 淋巴细胞产生抗体所必需的,可分为Th1 和Th2 两个亚群。前者产生IL-2 、IL-3 、IFN-γ和淋巴毒素及粒细胞-巨噬细胞集落刺激因子(granulocy te-macrophage colony stimulating factor ,GM-CSF)等, 参与细胞免疫;而后者则产生IL-4 、IL-5 、IL-10 和IL-13 等细胞因子,辅助B 细胞产生抗体,参与体液免疫。某些病原菌只能被Th1或Th2 有效地抑制。
IL-1 、IL-6 、肿瘤坏死因子-α(tumor necrotic factor ,TNF-α)以及转移生长因子-β(transfering growth factor ,TGF-β)都不能诱导Th1 细胞,只有IL-12P70 能独立诱导Thl 细胞的分化与增殖。同样,用单克隆抗体耗尽γ干扰素(interfe ro n-γ,IFN-γ),也会抑制Thl 细胞的分化和增殖。由此可见IL-12 促进Th1细胞的增殖, 可能是通过IFN-γ而发挥作用的。IL-4 和IL-10 均对IL-12P70 促进Th1 细胞分化和增殖能力有抑制作用。IL-4 通过促进Th2 的增殖对Th1细胞的增殖产生抑制。
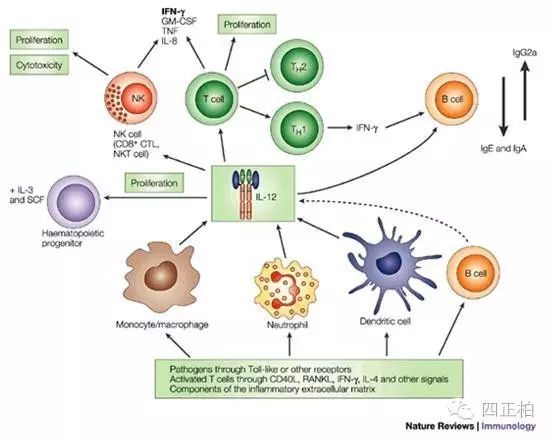
2. 促进T 细胞和NK 细胞的增殖及杀伤作用
IL-12P70 能促进T 细胞和NK 细胞的增殖。对外周血分离T 细胞、培养T 细胞克隆、CTL 细胞系和TIL 细胞都有启动生长增殖效应,IL-12P70 还可刺激CD4+和CD8+的TCR-αβ+ T细胞或TCR-γδ+ 淋巴母细胞的增殖,而IL-2 抗体或受体不能抑制其增殖,因此这一效应不依赖于IL-12P70 。说明IL-12P70 效应独立于IL-12P70。虽然IL-12P70 诱导PHA 激活的淋巴细胞增殖效应仅为IL-2 的一半, 但与IL-4 、IL-7 的作用相同, 而所需IL-12P70 的浓度远远低于IL-2 、IL-4 、IL-7 。IL-12P70 能直接刺激CD56+NK 细胞的活化,IL-2 和IL-7 对NK 细胞的刺激效应仅为IL-12 的15 %和50 %, 不过总的来说IL-12P70 诱导NK 细胞的增殖尚达不到T 细胞的同等水平。IL-12P70 能激活NK/LAK 前体细胞使之成为具有细胞溶解功能的杀伤细胞,CD56+NK 细胞与IL-12P70 过夜孵育后能显著增强对NK 敏感、NK 抵抗、抗体包被的肿瘤靶细胞及病毒感染的纤维母细胞或T 细胞的杀伤能力。IL-12P70 的上述性质提示其作为一种免疫调节因子治疗恶性肿瘤的潜在价值。
3. IL-12P70 对其他细胞因子产生的调节作用
IL-12P70 可刺激NK细胞和T细胞产生IFN-γ。但IL-12P70 诱导静止状态的外周血淋巴细胞(PBL)及刺激新生儿CD4+T 细胞产生IFN-γ时需要有H LA-DR+辅佐细胞(accessory cell s)的参与,这类辅佐细胞表面既无B 细胞标志, 又缺乏单核细胞表面标志,树突状细胞(dendritic cell,DC)是其中的一种;而IL-12P70 刺激激活的NK细胞和T细胞产生IFN-γ时则不需要辅佐细胞的协同。尽管I L-2也能刺激T 和NK 细胞产生IFN-γ, 但I L-12 诱导T 细胞、NK 细胞产生IFN-γ的主要信号途径与IL-2 的不同,抗IL-2 抗体只能略微降低IL-12P70 诱导的IFN-γ产量(22 %);而抗IL-12P70 抗体不能抑制I L-2诱导的IFN-γ产量,IL-12P70 和I L-2 联合应用有协同刺激NK 细胞、T 细胞产生IFN-γ的作用。另有研究发现IL-4 能增强IL-2 和IL-12P70 诱导的鼠NK 细胞表达IFN-γ。IL-12P70 除能诱导IFN-γ的表达外, 还能刺激其他细胞因子的生成。如可诱导NK 细胞表达微量TNF 。IL-12P70 和IL-2 联合应用在诱导TNF 表达方面有叠加作用。在人类IL-12P70 只能刺激新生儿CD4+T 细胞表达TNF-β , 却不能诱导其产生TNF-α;而小鼠IL-12P70 则不能诱导SCID 鼠脾细胞产生任何类型的TNF 。但IL-12P70 可使正常小鼠脾细胞mRNA 的表达量增加5倍左右。此外,IL-12P70 还可刺激NK 细胞产生可溶性的p55 和p75 TNF 受体。IL-12P70 能使小鼠脾细胞的IL-10mRN A 表达量增加46倍。由于IL-10 可抑制IL-12P70 的某些功能,因此IL-12P70 诱导IL-10 生成可能是体内的一种反馈调节。
【应用研究】
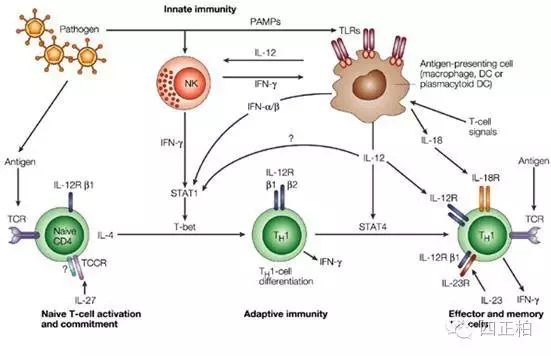
研究表明,Th1细胞在防止疟疾传染中发挥着重要作用,其分泌的IFN-γ可刺激巨噬细胞产生大量的一氧化氮,直接杀死病原菌。IL-12P70 是介导Th1 细胞免疫应答关键的细胞因子;IL-12P70 基因敲除小鼠不仅脾细胞分泌IFN-γ的能力下降,而且其巨噬细胞的吞噬调理作用也明显低下。NK 细胞对恶性疟原虫感染红细胞的细胞毒性作用也明显依赖于IL-12P70的存在。疟原虫初次感染的不同结局明显取决其感染早期Th1细胞免疫应答的建立与否。IL-12P70 则通过促进Th1 细胞的分化和增殖而在阻止疟疾传染中发挥作用。
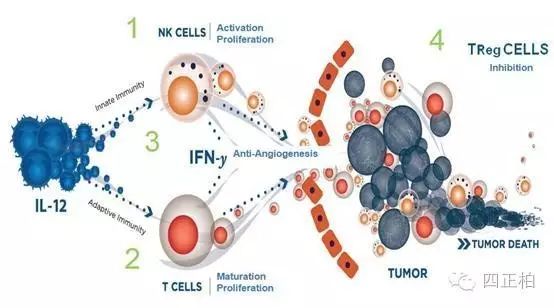
此外, IL-12P70 作为肿瘤免疫基因治疗的候选基因受到越来越多的关注。IL-12P70 除增加NK/ LAK 的杀伤活性外, 还能诱导特异性CTL 细胞的产生, 后者被认为是杀瘤作用最有力的细胞。诱导CTL 的产生需要IL-12P70 和肿瘤抗原的共刺激作用,用IL-12P70 和经放射照射的黑素瘤细胞同时诱导时, CD3+T 细胞能特异溶解受MHC 限制的靶细胞, IL-12P70 也能增强抗-CD3 单抗刺激的CD8+T 细胞溶解靶细胞的能力。有研究表明,应用肌醇磷脂特异性磷脂酶洗脱显示,IL-12P70是以锚定蛋白的形式嵌合在肿瘤细胞膜上,可以使IL-12P70 在免疫反应的局部发挥作用,克服了可溶性IL-12P70 的全身性不良反应和毒性作用及半衰期短等不足。
IL-13可由多种细胞分泌,如CD4+T细胞、CD8+T细胞、肥大细胞、嗜碱性粒细胞、嗜酸性粒细胞和自然杀伤细胞。特别是2型辅助性T细胞(Th2)。
【生物活性】
1、对单核巨噬细胞的调节作用
IL-13对单核细胞形态和表面分子表达具有调节作用。IL-13促进单核巨噬细胞形态改变,加速单核巨噬细胞融合,形成异物型多核巨噬细胞(foreign body giant cell,FBGC)。IL-3可增强人单核细胞表面CD23(IgE低亲和力受体IgERn)、主要组织相容性复合体II(MHCII)和甘露糖受体(与吞噬作用有关)表达。IL-13可抑制脂多糖(LPS)激活的单核/巨噬细胞致炎性细胞因子的基因转录和蛋白质合成,如IL-1、IL-6、IL-8等。
2、IL-13对B淋巴细胞具有调节作用
IL-13可以诱导B细胞表达CD23/CD72/IgM和MHC II。IL-13可以诱导CD4+T细胞共育的高纯度成熟B细胞表达IgE重链基因,合成IgE和CD4,但对IgG,IgM和IgA合成无作用。IL-13和另一个细胞因子IL-4在基因位置和DNA序列上具有许多相似之处,二者功能上也有所相似。IL-13是除了IL-4之外,在过敏性疾病中发挥重要作用的一个细胞因子。
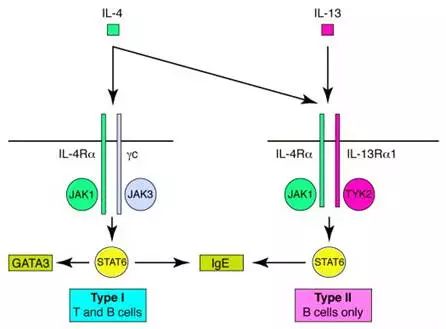
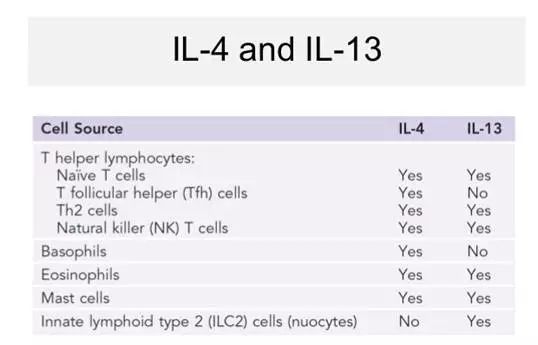
3、IL-13对血管内皮细胞的调节作用
IL-13可选择性诱导培养的人脐静脉内皮细胞表达血管间黏附分子1(VCAM-1),而不影响E-选择素和细胞间黏附分子-1(ICAM-1)表达,增强嗜酸性粒细胞与内皮细胞的黏附作用。
4、IL-13促进NK细胞产生IFN-γ,与IL-2具有协同作用。
IL-13调节肥大细胞的细胞因子,诱导肥大细胞早期英大基因(c-fos)表达,增强ICAM-1分子表达。基因转导研究证实,IL-13具有特异性和非特异性抗肿瘤活性。但具体机制并不清楚。
【临床应用】
过敏性哮喘以炎症过程为核心,典型地伴随有Th2型免疫应答。Th2细胞产生一系列细胞因子如IL-4、IL-5、IL-9和IL-13等,其中IL-13被认为是最为核心的因子,几乎参与到哮喘所有的并发过程。目前已经有大量试验证明,IL-13在哮喘发病机制中起到中轴的作用,因此,众多哮喘的治疗因子中,IL-13及其信号途径作为有前景的治疗靶位点展现了其在临床上的重要价值。基于此,应用IL-13的对抗物阻断哮喘病中大量表达的IL-13的生物活性,对与改善哮喘应该是一个好的方法。
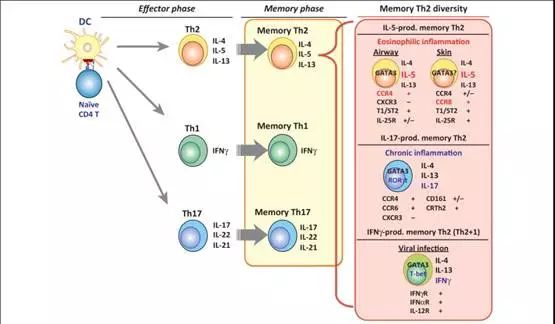
小鼠体内模型证明IL-13通过非淋巴细胞依赖途径诱导哮喘症状,这是IL-4所不及的,因此IL-13是治疗哮喘过程中更为有效的靶位点。此外,IL-13通过与IL-13Rα2结合诱导产生TGF-β,从而诱导哮喘患者的肺部纤维化。同小鼠体内模型一样,哮喘病患者体内IL-13也是大量表达,在人哮喘病发病中起到关键的作用。
sIL-4R是首次用于治疗哮喘的可溶性细胞因子受体,这是基于IL-4的定向靶位。与sIL-4Rα一样,sIL-13R重组体作为治疗哮喘的治疗因子,具有特异性抑制IL-13的作用。sIL-13R有sIL-13Rα1和sIL-13Rα2两种。剑桥抗体中心应用抗IL-13抗体单抗治疗重度持续哮喘患者,临床I期试验初步证明它是安全有效的。IL-13单克隆抗体治疗哮喘在国外已经呼吁II期临床试验(2013年),以疫苗形式诱导持续的IL-13中和抗体,对哮喘这样的慢性疾病而言具有更大的应用潜能。
能诱导活化的B细胞增殖以及对静止的B细胞不具刺激作用,又被称为高分子B细胞生长因子。
【生物学活性】
IL-14可诱导活化B细胞增殖,但对静止B细胞无刺激作用,也不诱导抗体合成和分泌。此细胞因子可给已被体内的Staphylococcus aureus Cowan I(SAC)或体外的抗μ活化的B细胞释放出增值信号。基于这些生物学特性,虽然为最佳的B细胞增殖所需要Bb的浓度比IL-14高得多,但是IL-14与来自补体替代途径的因子B的Bb活化片段的作用却是相似的。此外,IL-14,而不是Bb,能增加细胞质中的cAMP和Ca2+,因此,可提高受体的表达。IL-14在缺乏共刺激物时,仍可刺激慢性淋巴性白血病(CLL)细胞的集落形成。因此,有这样一种假说:此细胞因子是一个重要的造血生长因子,它可以调节CLL中集落产生“成熟的”白血病B细胞的增值活性。
此外,IL-14还与IL-4相似,能诱导抗μ链抗体激活的B细胞增殖,抑制免疫球蛋白分泌,选择性扩增特定的B细胞亚群(可能是记忆性B细胞亚群)。IL-14还具有抑制丝裂原诱导的B细胞Ig分泌的效应。
【临床应用】
1、具有高肿瘤细胞负担的非Hodgkin淋巴瘤(NHL-B)患者的渗出液体中存在IL-14。从病人体内新分离出来的NHL-B细胞可以表达IL-14 mRNA,分泌IL-14,而且与IL-14相对应进行增殖,而外源IL-14也能刺激体外的NHL-B细胞增殖。因此,它可能作为NHL-B细胞系的一个自分泌和旁分泌生长因子,并且假设可引起NHL-B细胞逃逸出正常的生长调控。因此,可以采用基于IL-14的反义寡核苷酸作为攻击性(中等程度和高级的)NHL-B一个治疗性手段。
2、IL -14 可能通过促进 B 细胞增殖、增强机体对胸腺依赖性抗原、胸腺非依赖性抗原的免疫反应,活化体液免疫,诱导 TgAb、 TPOAb 表达增高,进而引起桥本甲状腺炎的发病。最新的研究发现桥本甲状腺炎患者甲状腺组织中 IL-14 表达增高,甲状腺滤泡细胞可诱导表达IL-14,认为 IL-14 在桥本甲状腺炎的发病过程中起重要作用。研究还发现桥本甲状腺炎患者外周血中IL-14 表达增高, 且其表达水平与 TgAb、 TPOAb 表达水平呈正相关。研究进一步证实 IL-14 与桥本甲状腺炎的发病密切相关。
3、IL-14不仅是调节B细胞功能的重要细胞因子, 其受体也是B细胞上的重要功能分子,并且与某些B细胞性肿瘤和自身免疫性疾病密切相关。IL-14-α由IL-14外显子3-10基因编码。研究表明,原发性和继发性干燥综合征患者表达高水平的IL-14-α,IL-14-α的转基因小鼠更是表现出高丙种球蛋白血症、B细胞性非霍奇金淋巴瘤等干燥综合征典型症状,这提示IL-14在干燥综合征的病理生理学中存在重要意义,对其深入研究或为干燥综合征的发病机制及防治提供理论基础。
4、单纯性牙周炎是导致成年人牙齿丧失的主要因素,主要破坏患者的牙龈及牙周组织 。目前大量研究结果表明,单纯性牙周炎是由菌斑微生物引起的感染性疾病。菌斑微生物会产生脂多糖等内毒素,内毒素经过转运系统最终进入到结缔组织中,引起牙龈及牙周组 织的免疫反应,刺激单核细胞/巨噬细胞产生如IFN-r、SAA及IL-14等免疫调节因子使其浓度在患者牙周组织局部以及患者外周血中增加。IL-14既促进被有丝分裂原活化的B细胞增殖,又能抑制被有丝分裂原活化的B细胞分泌抗体,但是IL-14水平变化与单纯性牙周炎的关系尚未明确。
一种可溶性细胞因子,作为多种免疫细胞的趋化因子参与并调节机体炎症反应及免疫反应。
【生物活性】
1、刺激T细胞增殖:IL-15可刺激CTLL、PHA活化的T细胞、肿瘤浸润淋巴细胞的增殖,并与IL-2有协同作用。IL-15对T细胞有趋化作用,其趋化作用强于IL-8和MIP-α。X连锁SCID小鼠发病的部分原因是IL-15介导的功能有缺陷。
2、调节B细胞增殖和分化:IL-15可刺激活化B细胞的增殖,与CD40配体协同,刺激活化B细胞分泌IgM、IgG1和IgA,但不产生IgG4和Ig
3、调节NK细胞:IL-15诱导CD34+造血祖细胞分化为CD56+ NK细胞,NK细胞对IL-15刺激有一定的增殖反应,并明显提高杀伤活性,维持存活。IL-15可促进穿孔素和粒酶的表达。IL-15可协同IL-12促进NK细胞的杀伤活性和细胞因子的分泌。在小鼠体内IL-15亦具有促进NK杀伤活性的作用。它还可诱导CTL和LAK的产生和杀伤活性。
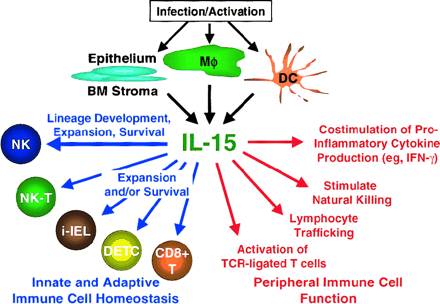
4、IL-15的趋化作用:IL-15对人外周血单核细胞具有明显的趋化作用。体外实验证明,IL-15在0.6ng/ml的浓度时,能导致人外周血单核细胞出现去极化现象,其作用明显强于IL-8和巨噬细胞炎性反应蛋白-1α,而且IL-15对CD4+或CD8+T细胞亚群的极化作用无明显差异,但对B细胞和中性粒细胞无极化作用。IL-15的趋化作用预示它可能参与炎症反应的调节。
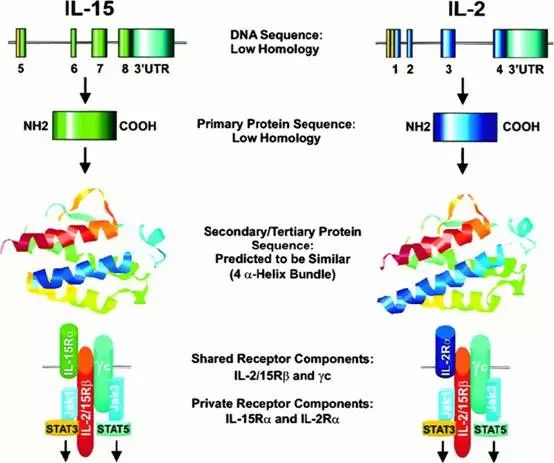
【临床应用】
IL-15和 IL-2对于调控体内淋巴细胞功能和稳态起重要作用。在体外具有类似的刺激淋巴细胞增殖作用,然而在体内的作用却明显不同。不同生理功能是由于各自不同受体亚基介导的不同信号转导通路、不同受体亚基表达模式。反式呈递方式介导的信号转导是IL-15功能不同于IL-2的一个重要机制。尽管它们的异三聚体受体中有两个共用亚基,这两种细胞因子在适应性免疫应答中具有明显不同的作用。IL-2独特的作用是清除自身反应性T细胞防止自身免疫性疾病发生,相反, IL-15可长久维持记忆性T细胞针对病原体的免疫应答。
1、在慢性的炎症性疾病(类风湿关节炎)中,IL-15通过趋化作用征集和活化T淋巴细胞的能力已得到证实,这表明IL-15在病理状况下能发挥生物学作用。目前在类风湿关节炎中,直接针对T细胞的治疗方法证明能够改善疾病状况。在类风湿关节炎中,IL-15可能是未来治疗性介入的一个有用的对象。
2、IL-15在抗蠕虫及原虫感染等方面可发挥免疫增强作用。
3、IL-15可能在肿瘤免疫中发挥重要作用。体内、外实验都已证实,IL-15能够诱导CTL细胞和LAK细胞活性而体现抗肿瘤活性。有研究证明IL-15能够在相对稳定的黑色素瘤患者体内诱导淋巴细胞中的LAK细胞活性,从新的肿瘤组织中杀伤自体固有的黑素肿瘤细胞。
主要由活化的CD8+T细胞产生,受体是CD4,能趋化CD4+T细胞、单核细胞和嗜酸性粒细胞,诱导T细胞和单核细胞表达IL-2R和HLAII类分子。
【生物活性】
1、诱导人CD4+淋巴细胞、单核细胞和嗜酸性细胞迁移;
2、诱导人CD4+细胞和单核细胞的IL-2R和HLA-DR表达:在与其他一些趋化粘附分子共同作用时, LCF能够诱导IL-2R的表达和向上调节静息状态下人T淋巴细胞主要组织相容性复合物Ⅱ型分子;
3、影响蛋白激酶C(PKC)的分布;
4、抑制CD3依赖淋巴细胞活化与增殖。IL-16与CD4的相互作用导致了抗原非依赖性趋化作用和IL-2R的表达,这一炎症前期状态与经CD3/TCR复合体参与的免疫应答暂时被抑制有关。
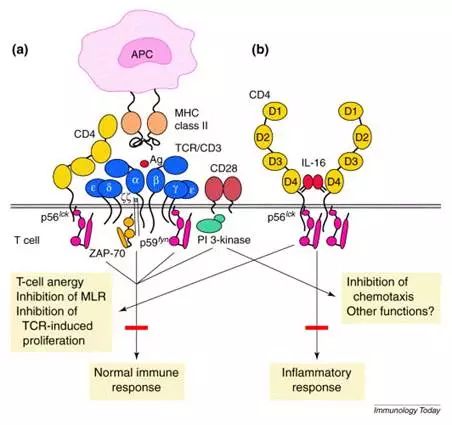
【临床应用】
1、糖尿病和IL-16水平有关联,具有代谢综合症的Ò型糖尿病病人血清中的IL-16水平显著升高。
2、IL-16是一种早期促炎因子,可诱导单核巨噬细胞、T淋巴细胞、树状细胞等表达细胞因子受体,进而使这些细胞分泌细胞因子,从而扩大机体的炎症反应。在肝移植上尽管有严格的组织差异性,肝炎患者肝移植之后还会普遍存在病毒的复活现象。
【生物活性】
1、 IL-17A具有强大的致炎性:
① 它能促进机体局部产生趋化因子,如IL-8、MCP-1(单核细胞趋化蛋白-1)、Gro-a (生长调节因子-a),因此有助于单核细胞和中性粒细胞的迅 速增多。
② 能刺激产生IL-6和PGE-2,增强局部炎症。此外,IL-17A可刺激产生造血细胞因子G-CSF和GM-CSF,引起骨髓细胞系的增生;
③ 还能诱导细胞表面的细胞间粘 附分子(intercellular adhesion molecule,ICAM ),驱动T细胞的应答。
2、IL -17E在体外和体内也均具有强大的促炎性效应:
① 作为IL -17A 的类似物,IL-17E也能刺激NF-kb的活化,后者是促进某些重要的致炎分子包括TNF、IL-1b信号转导的转录因子。
② IL-17E的过度表达可引起免疫应答的明显变化。
③ IL-17E的存在可诱导多种组织,尤其是肝脏、心脏、肺的病理改变,其特征是混合性的炎性细胞浸润、上皮的增生和肥大。
3、新的IL-17家族成员各自具有明显不同的表达形式,因此可能具有各不相同的生物学作用:
① IL-17A的表达被高度调控着,且除了在那些特定的、活化的T细胞之外,基本上不能检测到IL-17A的转录。
② 在某些外周组织和免疫组织,如胰腺、小肠和胃组织中,IL-17B可适量表达。
③ IL -17C的表达极为罕见,但像IL-17A一样,它的表达在炎性条件下被高度调控着。
④ IL-17D在肌肉组织和神经系统中的表达特别高,提示其生物学活性可能与IL-17A明显不同。
⑤ IL-17在很多外周组织中的表达都极低,但能通过PCR检测到。IL-17FmRNA的表达与IL-17A很相似,其表达普遍很低,但在T细胞的活化群体中可清楚地观测到。
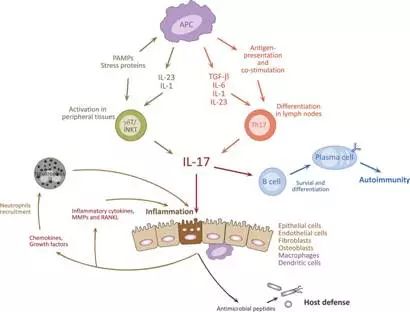
IL-17家族的信号转导
1、IL-17A由活化的T细胞产生,并与普遍表达于所有细胞类型的IL-17R结合介导炎症反应。然而,IL-17A信号传递的确切机制仍未完全阐明。在包括RA的慢性炎症中,IL-17A可通过直接使基质降解,或间接使活化的炎性细胞增多并诱导其它致炎细胞因子包括IL-1b和TNF-a进入炎性组织,引起组织损害。
2、 IL-17A活化MAPKs(丝裂原活化蛋白激酶)所有的三个成员,即细胞外信号调节激酶(ERK1和ERK2 )p44和p42、Jun蛋白N-端激酶 (JNK )和p38。
3、 在人的纤维母细胞、肠上皮细胞和培养的软骨细胞中可见IL-17A诱导NF-kb的活化,该作用可能与TNF受体相关因子(TRAF)-6有关。
4、 在人单核白血病细胞系U 937中,IL -17A可诱导Janus激酶 (JAN ) 以及信号转导 和转录激活蛋白(STAT )途径的某些成员发生酪氨酸磷酸 化,其中包括Tyk2、JAK1,2和3、STAT1,2,3和4,提示JA K/STAT途径可能参与调节IL-17A的生物学效应。
【临床意义】
IL-17家族与多种疾病有关。目前的研究表明,IL-17A和RA、气道炎症、其它慢性炎性疾病以及肿瘤的生长相关。通过序列的相似性而鉴定出来的IL-17家族,与已知的细胞因子家族相比,具有特异性。目前对于IL-17家族的研究,大部分是在探索该蛋白质的生物学功能。然而,迄今为止我们所 知的IL-17及其新的家族成员的功能提示,这些分子能引发深刻的生物学应答,并可能在免疫应答的微调中起重要作用。该家族的某些成员与炎症相关,并可诱导其它与炎性应答相关 的细胞因子,提示可通过抑制或者调节这些蛋白质的功能,进行治疗性的应用。
【生物活性】
IL-18是一种多功能因子,其生物学功能无种属特异性。早期发现中性粒细胞是其作用的靶细胞,能特异性趋化中性粒细胞进入炎性组织,促使其脱颗粒,产生超氧阴离子,引起呼吸暴发;并激活炎性细胞;促进急性期蛋白合成;引起发热、参与炎症病理性损害;促进炎性介质释放;促进成纤维细胞增殖-慢性炎症,所以在炎性反应中起重要作用。随着研究的深入,发现IL-18能作用于不同细胞,它能促进炎性反应进程、刺激血管的形成、促有丝分裂、调节宿主免疫功能等,与多种炎性反应性疾病、肿瘤、免疫性疾病的发生和发展密切相关。
【临床应用】
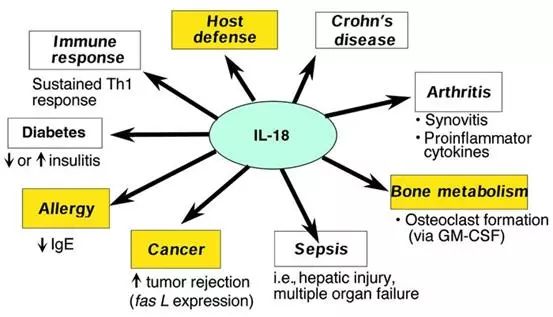
IL-18 与感染性疾病
流感病毒感染的巨噬细胞产生IL-18 增多;应用数种不同的微生物刺激人外周血单核细胞(PBMCs),均使IL-18 的分泌增加;感染性中枢神经疾病患者脑脊液及结核病患者血清IL-18滴度上调。在抗新型隐球菌等引起的感染中,IL-18 与IL-12 有协同作用。IL-18 可独自作用激活CD8+T 细胞,CD8+T 在病毒清除上发挥重要作用。
IL-18 与肿瘤性疾病
IL-18 可使细胞毒T 淋巴细胞(CTL )的杀肿瘤活性升高,应用转基因技术发现IL-18可抑制纤维肉瘤在裸鼠上的生长。将外周血单核细胞中的NK 细胞去掉后,IL-18 还可以激活人CTL 细胞毒活性,抑制自身肿瘤的发生。
IL-18 与免疫性疾病
应用RT-PCR 和免疫组化方法发现Crohn’s 病患者肠上皮的IL-18 的mRNA 表达和蛋白分泌水平均上调。类风湿性关节炎(RA)患者的关节滑膜组织中IL-18 基因及蛋白量的表达上调。在非肥胖性糖尿病小鼠胰腺IL-18 的mRNA 表达上调。在系统性红斑狼疮(SLE)的发病中,IL-18 升高是该病活动性的标志。IL-18可引起SLE患者外周血淋巴细胞凋亡率增强,并导致调节紊乱。此外,IL-18还可与自身免疫性脱髓鞘疾病、重症肌无力密切相关,患者血清中IL-18 和IFN- γ含量均升高,且与病情呈正相关。
IL-18 与免疫性肾疾病
在IL-18 与肾疾病的研究中,发现狼疮性肾炎小鼠IL-18 表达水平上调并与狼疮性肾炎的病情严重相平行。不仅浸润的单核细胞表达IL-18,而且原代培养的肾小管上皮细胞成为IL-18 的主要表达者,还发现IL-18 可增加肾小管上皮细胞(TECs)凋亡,上调细胞黏附分子1(ICAM-1)和血管细胞黏附分子(VCAM-1)的表达。研究还发现在人类狼疮性肾炎患者中,外周血及肾组织IL-18 基因及蛋白的表达量均较对照组显著增高,尿IL-18 水平也显著升高。原发性肾病综合征和狼疮性肾炎患者肾小管间质区有比肾小球区更多的IL-18 表达,而且等级相关分析,发现肾上管间质区的IL-18 表达量与肾小管间质的损害程度呈正相关。已证实,IL-18 可增强Fas 配体(FasL)介导的细胞毒性,导致细胞凋亡。
IL-19是IL-10家族的细胞因子之一,主要在人类的单核细胞,B淋巴细胞和T淋巴细胞中大量表达,也在炎症细胞中表达。
【生物活性】
1. IL-19主要是通过IL-20R1/R2这一对受体复合物传导生物信号而起生物学作用。IL19、IL-20是细胞因子IL-10家族的成员,但IL-19的作用还不十分明确,对于IL-19是一个促炎性或抗炎性的细胞因子仍然存在争议和不确定性。有研究认为IL-19可能和IL-10一样具有抗炎效应,并且可能存在诱导淋巴细胞从Th1向Th2转变的表型。也有研究认为在单核细胞IL-19上调IL-6和TNF-α中产生,显示IL-19有促炎症的特点。尽管没有检测到IL-20R1在免疫细胞群的表达,但还是有很多研究清楚地显示出IL-19对这些细胞的效应。大多数的研究表明IL-19是Th2系统的一部分。
2. 有研究表明,IL-19在心肌炎中发挥抗炎效应。在炎症性肠道中内源性IL-19呈现出保护性作用,有学者建立了IL-19小鼠DSS大肠炎模型,并且表明这些小鼠相比于那些免疫完整的小鼠更易感大肠炎。活动性克恩病中,IL-19表达缺陷及对其反应的缺少有利于疾病炎症的发展。此外,腺病毒介导的IL-19融合基因转入大鼠后能有效减少损伤,并且激活MAPK;进一步发现一些细胞炎性因子能诱导IL-19的产生。而IL-19能通过减低编码炎症性蛋白的mRNA种属的稳定性从而减少血管平滑肌的炎症反应。一些体外实验的研究表明IL-19能诱导CD4+T细胞产生Th2细胞因子,在周围血单核细胞IL-19增加IL-10的产生,长时间暴露于IL-19的T细胞会下调IFN-γ,上调IL-4和IL-13。但是也存在一些争议的研究发现在单核细胞IL-19上调促炎因子IL-6和TNF-α的产生,在银屑病患者皮肤发现IL-19及其2条受体链IL-20R1/IL-20R2的表达,进一步研究发现减少IL-19水平的治疗是有效的。
目前关于IL-19的生物学功能仍未明确,抗炎作用和促炎作用众说纷纭,我们认为可能与IL-19在不同的疾病和不同细胞类型中会表现出不同的效应有关。
【临床意义】
1、炎症和自身免疫机制在扩张型心肌病(DCM)发病机制中发挥着重要作用。DCM的进展取决于各种促炎和抗炎细胞因子之间的平衡,这些细胞因子的主要来源是浸润心脏的炎症细胞,特别是单核细胞、T细胞,也包括心肌固有的树突状细胞(DCs)、肥大细胞,甚至心肌细胞。IL-19、IL-20可以在DCM患者外周血的血浆存在高水平表达,表明IL-19/IL-20可能是参与DCM过程中复杂的炎症与抗炎网络的一部分。
2、IL-19参与了多种疾病的免疫发应,报道表明IL-19通过促进炎性细胞因子和趋化因子(IL-1β、IL-6、IL-8、CCL5和CXCL9)的表达而参与内毒素休克的病理过程,在Th1主导的疾病如银屑病、Th2主导放入疾病如哮喘以及Th1和Th2均主导的疾病的发病机理中起作用。因此,IL-19被认为是自身免疫和炎症性疾病的一个潜在治疗靶点。目前IL-19是否发挥促炎抗炎作用尚不清楚,尤其是在心血管疾病方面的研究仍较少。
近来发现的白细胞介素10 相关细胞因子家族的新成员;IL-20 能够调节皮肤正常生理功能,活化角质细胞中的STAT3 途径,促进一些细胞因子、趋化因子的大量表达,从而调节皮肤早期炎症的发生。
【生物学活性】
1、IL-20促进细胞因子和趋化因子的分泌
Blumberg等发现IL-20可以激活人类角质细胞系Ha-CaT细胞的STAT3途径,引起STAT3分子相关基因的活化和转录, 具体来说研究人员发现在IL-20刺激下,HaCaT细胞中TNF-α、MCP-1、M RP-14 等细胞因子的表达上调,而这几种细胞因子和早期的炎症启动和免疫应答密切相关:TNF-α可活化单核和巨噬细胞, 提高其杀伤活性, 并上调巨噬细胞MHC Ⅱ分子,提高它的抗原递呈能力, 还能刺激内皮细胞表达MHC Ⅰ类抗原,同时促进中性粒细胞、淋巴细胞、单核细胞黏附到内皮细胞上,参与炎症反应;MCP-1则可趋化激活T 细胞、单核细胞、激活嗜碱性粒细胞, 促进NK细胞细胞毒活性;MRP-14是一种S100 钙离子结合蛋白;在白细胞整合素的活化中起作用, 调节表皮炎症。
进一步研究发现,STAT3基因敲除的角质细胞尽管可以形成表面上正常的表皮,但它们在外伤愈合和毛发生长方面有着明显的缺陷,而且STAT3敲除的角质细胞对表皮生长因子(EGF)、肝细胞生长因子(HGF)、IL-6的刺激不产生细胞效应。研究人员还发现IL-20可刺激角化细胞的增生和分化,这一过程似乎和活化的T 细胞有关,活化的T 细胞可分泌IFN-γ,尽管IFN-γ在正常条件是诱导巨噬细胞、T细胞、B细胞等细胞MHC Ⅱ分子的表达, 提高它们的抗原递呈能力, 但在皮肤炎症这样一个环境中,IFN-γ则可促进角质细胞的增生。
2、IL-20与皮肤炎症、疾病:在皮肤炎症发生、发展的过程中, IL-20和IL-20受体在上皮细胞、内皮细胞、淋巴细胞中均有较高的表达。
通过对正常人和银屑病患者皮肤中IL-20 受体α、β2个亚单位的检测发现银屑病患者皮肤中角质细胞、上皮细胞、单核细胞检测到极高水平的IL-20R 的m RNA, 而在正常皮肤中只有很低的表达,提示IL-20与IL-20R 的相互作用可能与银屑病的发病有关。
IL-20 主要由外周血单个核细胞(PBMC)及活化的上皮细胞分泌,其主要靶器官是皮肤。IL-20的受体由IL-20Rα 和IL-20Rβ 两个亚单位结合而成。IL-20必须同时与IL-20Rα和IL-20Rβ结合,才能使信号转录活化因子STAT3发生转位,进而激活下游基因的表达。IL-20Rα和IL-20Rβ表达量高的细胞,激活STAT3 转位所需IL-20的量相对减少,证明增加受体数量可提高IL-20的效应强度。
IL-20受体结合后,激活重要的转录因子STAT3,能分泌大量的细胞因子如TNF-α、单核细胞趋化蛋白-1(MCP-1)和迁移抑制因子相关蛋白14(MRP-14)。有研究发现IL-20参与数种慢性炎症性疾病和自身免疫性疾病:IL-20在类风湿性关节炎患者的关节液中升高,能够趋化中性粒细胞迁移,在胶原诱导类风湿性关节炎(RA)动物模型上证实IL-20 可能在类风湿关节炎发病过程扮演重要角色。进一步的研究发现选择性拮抗IL-20抑制了胶原诱导的RA动物模型的炎症和骨质破坏。
过度表达IL-20 的转基因小鼠,其组织病理学改变与人类银屑病有许多相似之处:皮肤显著增厚、角化过度,电镜下可见线粒体内有脂质包涵体和点状透明角质颗粒。但IL-20 转基因小鼠皮损处没有银屑病皮损中常见的免疫活性细胞浸润现象。IL-20,IL-20Rα和IL-20Rβ在动脉粥样硬化患者病变血管腔表达升高,IL-20可能是一种促动脉粥样硬化炎症介质。研究发现IL-20 在过敏性支气管哮喘患者血清中也显著升高, 如前所述IL-20能够促进TNF-α、MCP-1、MRP-14 等炎症介质表达释放增加,这可能是升高的IL-20 参与支气管哮喘慢性气道炎症的途径之一。
此外研究还表明IL-20能够促进多种增殖相关炎症介质如bFGF,VEGF,MMP-2,MMP-9的表达升高。已经证实bFGF,VEGF,MMP-2,MMP-9 参与支气管哮喘血管增殖重塑、多种肺部实质细胞增殖、变性、胶原沉积、上皮下纤维化等气道重塑过程。IL-20可能通过增加支气管哮喘患者bFGF、VEGF、MMP-2、MMP-9表达,加重支气管哮喘气道炎症,参与支气管哮喘气道重塑。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









很全面,学习收藏了
36