J Endod:MAPK信号通路对脂多糖介导的根尖牙乳头来源干细胞成骨/牙本质分化的影响
2019-02-15 lishiting MedSci原创
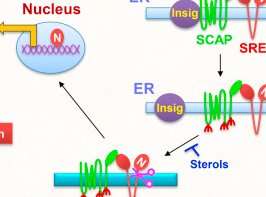
人根尖牙乳头来源干细胞(SCAPs)的成牙本质分化是未发育完成牙齿牙根发育的必不可少的步骤。然而,炎症状态对SCAPs成骨/成牙本质分化的影响还未可知。这篇研究的目的是为了评估脂多糖(LPS)对SCAPs增殖和成骨/成牙本质分化的影响以及MAPK信号通路在LPS介导的SCAPs成骨/成牙本质分化中的作用。
人根尖牙乳头来源干细胞(SCAPs)的成牙本质分化是未发育完成牙齿牙根发育的必不可少的步骤。然而,炎症状态对SCAPs成骨/成牙本质分化的影响还未可知。这篇研究的目的是为了评估脂多糖(LPS)对SCAPs增殖和成骨/成牙本质分化的影响以及MAPK信号通路在LPS介导的SCAPs成骨/成牙本质分化中的作用。研究培养了从人第三磨牙获取的SCAPs。检测细胞活力以及碱性磷酸酶活性和矿化能力。在SCAPs成骨/成牙本质分化过程中评估成骨/成牙本质分化和MAPK信号通路相关基因的表达变化。结果显示,在0.1 μg/mL LPS组中,SCAPs的细胞增殖、ALP活性和矿化明显上调。实时定量聚合酶链式反应检测显示,DSPP、Runx2和BSP表达升高。然而,并未发现任何OCN的表达变化。另外,LPS刺激上调了SCAPs内p-ERK和p-p38的表达,并且抑制ERK和p38 MAPK通路显著阻断LPS诱导的SCAPs的分化。结论:结果显示,LPS在适当的浓度会促进SCAPs的增殖和成骨/成牙本质分化。ERK和p38 MAPK通路参与了LPS介导的SCAPs成骨/成牙本质分化的调控。原始出处:Liu J
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#MAPK#
41
#成骨#
37
#脂多糖#
59
#牙本质#
26
#信号通路#
36