《自然》综述:组织干细胞和微环境的衰老(上篇)
2022-12-07 干细胞者说 干细胞者说 发表于上海
大多数成体器官中含有具再生能力的干细胞,通常位于特定的微环境。干细胞的功能对于组织稳态和损伤修复至关重要,而这功能的发挥依赖于其与微环境的相互作用。
撰文:步步先生
来源:干细胞者说
● ● ●
大多数成体器官中含有具再生能力的干细胞,通常位于特定的微环境(亦称壁龛或小生境或生态位, 英文名:niche)中。干细胞的功能对于组织稳态和损伤修复至关重要,而这功能的发挥依赖于其与微环境的相互作用。干细胞衰老与机体衰老息息相关。
在衰老过程中,干细胞的再生潜力和分化能力下降,从而导致组织不完整甚至健康状况的恶化。与衰老相关的干细胞变化,包括干细胞静息态维持、分化能力、分化偏好、克隆扩增能力等方面的缺陷,以及干细胞微环境中免疫细胞的浸润。
2022年7月,斯坦福大学的Anne Brunet、Thomas A. Rando和贝勒医学院Margaret A. Goodell在Nature Reviews Molecular Cell Biology上发表了题为“Ageing and rejuvenation of tissue stemcellsandtheirniches(组织干细胞及其微环境的衰老与再生)”的综述文章,我们试着解读一下。本文分上下两篇,将近9000余字,阅读耗时较长。强烈推荐收藏,并细细阅读!

| 目录 |
|
| 1 |
干细胞和干细胞微环境 |
| 2 |
衰老过程中的干细胞缺陷 |
| 3 |
衰老过程中的干细胞微环境缺陷 |
| 4 |
组织衰老和疾病中的干细胞 |
| 5 |
干细胞微环境的再生策略 |
| 6 |
干细胞的再生策略:局部重编程 |
| 7 | 文末小结 |
-01-
干细胞和干细胞微环境
成体内的不同器官和组织——大脑、心脏、脉管、肝脏、肠道、肌肉等——具有截然不同的功能,并包含许多不同的细胞类型。构建每个组织器官的细胞类型受到更新换代速率的影响。有些分化的细胞类型可以维持终生(例如大脑中的神经元或心脏中的心肌细胞)。有些些分化的细胞类型不断丢失并被迅速补充(例如红细胞、单核细胞及皮肤和肠道的上皮细胞)。
具有快速更新频率的细胞,在很大程度上是由非常活跃的干细胞(通常称为“成体干细胞”或“组织干细胞”)所产生。例如,位于骨髓中的造血干细胞 (HSC) 可以产生血液中的所有细胞,位于肠道隐窝中的肠干细胞 (ISC) 则产生排列在肠道内的上皮细胞。相比之下,具有较低或非常低更新频率的细胞(如神经元和肌肉纤维)是由非常稀有的干细胞群体再生的。除了成体干细胞外,哺乳动物的性腺或至少雄性性腺还含有生殖干细胞,具有产生配子的独特特性。
干细胞对组织稳态起着至关重要的作用,它们由其所在的微环境进行维持和调节,二者共同形成了一个再生单元。这些再生单元会对机体损伤等刺激做出剧烈反应。不仅如此,它们的功能也受到一些影响衰老的环境刺激影响,如饮食和运动。
众所周知,组织干细胞起源于其对应的胚胎位置。尽管胚胎干细胞增殖非常活跃,但大多数组织干细胞的一个关键特征则是它们的静息(quiescent)状态。因此,静息的干细胞形成了一个特殊的“细胞库”,这些细胞可以被诱导增殖,可在衰老过程中用于组织再生和修复。
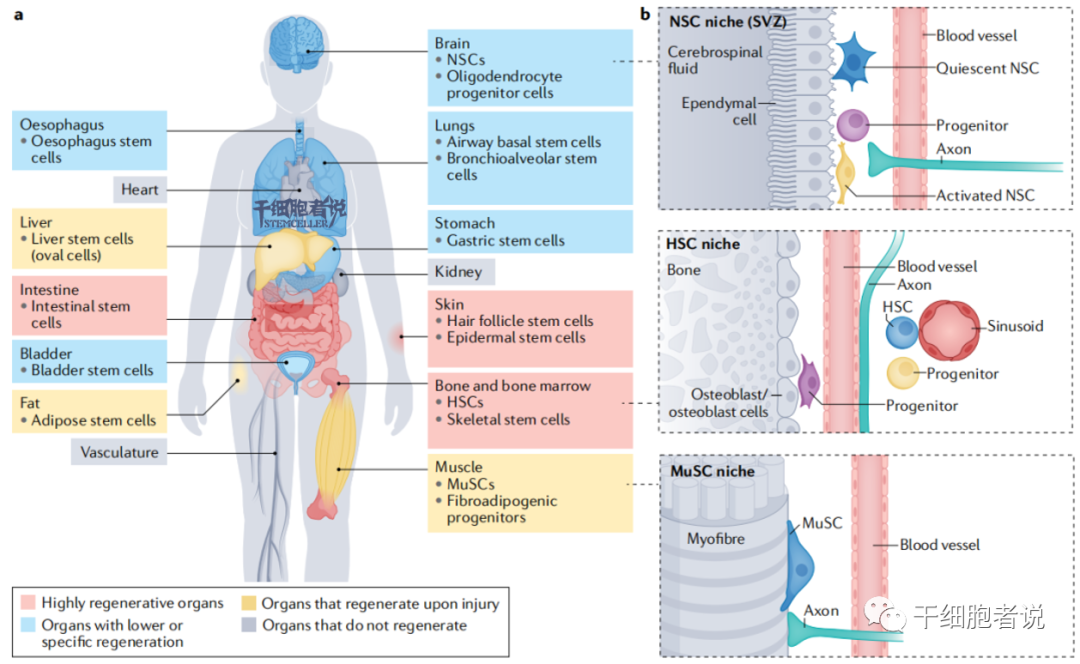
图1. 具有干细胞和干细胞微环境的器官。
-02-
衰老过程中的干细胞缺陷
衰老引起组织干细胞功能衰退。绝大多数成体干细胞的数量和功能会随着机体衰老而下降,造血干细胞除外。因为,造血干细胞的数量会随着年龄的增长,居然是增加的,虽然其功能却依然会衰退。干细胞功能衰退的现象与组织功能和修复能力的下降有关。
单细胞转录组学、谱系追踪和克隆分析等细胞水平的检测,让我们对衰老过程中干细胞的变化认知地更加清晰:
▉ 衰老的主要特征之一:成体干细胞产生后代的能力降低。
例如,在小鼠大脑中,单细胞RNA-seq分析表明,在脑室下区(SVZ)和海马的神经干细胞微环境(niche)中,活化的神经干细胞(NSC)和成熟神经细胞(后代)的数量随着年龄的增长而减少。随着年龄增长,人类海马微环境中神经干细胞产生新神经元(神经形成)的能力也会下降.在血液中,衰老造血干细胞产生的淋巴样细胞较少,偏向于骨髓谱系。在肌肉中,衰老和年轻肌肉干细胞(MuSC)的活化和分化轨迹不同,即衰老肌肉干细胞在动力学上激活、分化更慢。总之,这些数据表明在衰老过程中干细胞产生子代细胞的能力出现异常。
▉ 衰老的主要特征之二:静息干细胞的异质性逐渐增高。
衰老过程中的干细胞异质性,可能是由于老年个体中静息干细胞异质性增加导致。在大脑中,静息的神经干细胞数量随衰老增加,同时激活能力下降;一部分神经干细胞在衰老过程进入深度静息,不再维持年轻时的较浅的可逆静息。同样地,肌肉干细胞随着衰老进入更深的静息状态,同时也伴随激活能力的下降。
▉ 衰老过程中干细胞命运的异常:
随着年龄的增长,干细胞亚群的命运和行为可能会出现异常。干细胞可能进入衰老状态、过度激活状态或异常分化状态。异常激活伴随着特定祖细胞的分化偏倚,如随着年龄的增长,肌肉干细胞亚群变得更加“准备就绪(primed)”(即趋向肌源性命运),而其他则趋向纤维化状态。同样地,一些造血干细胞在衰老过程中变得更倾向于髓系祖细胞;在大脑中,老年祖细胞表现出较低的分化动力学,并趋向于星形胶质细胞命运。
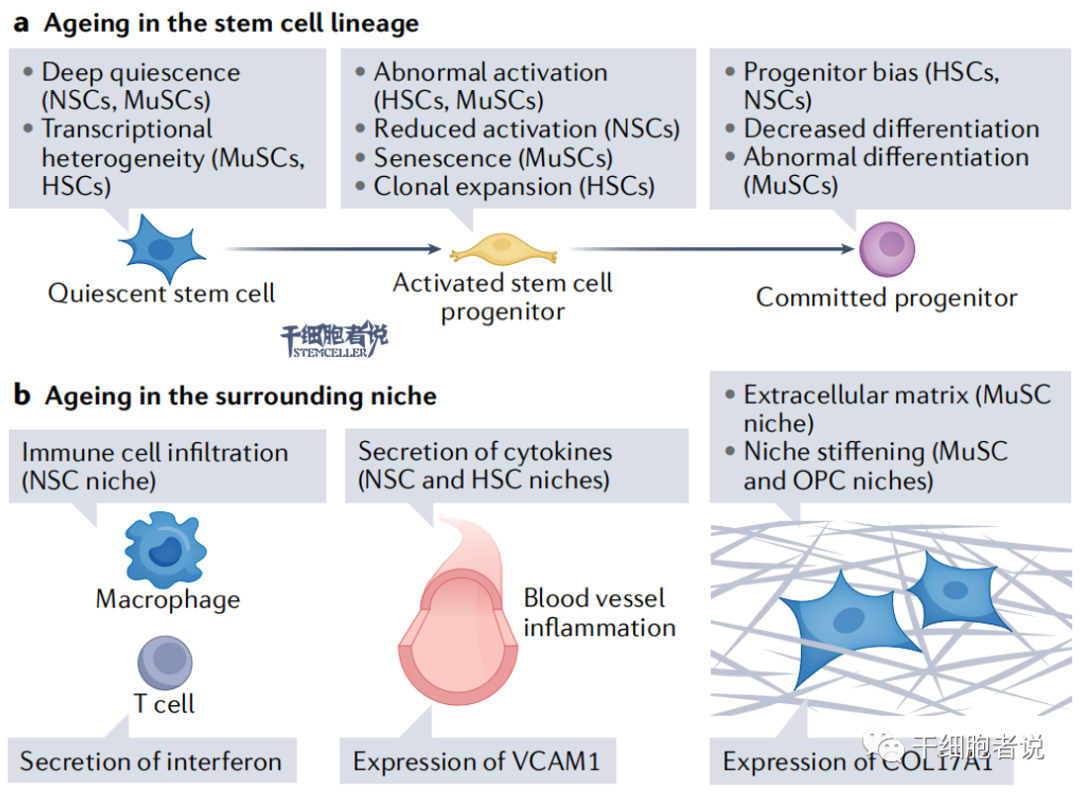
图2. 衰老过程中干细胞及其微环境的变化。a. 衰老过程中的干细胞谱系变化。b. 衰老过程中微环境变化。
衰老过程中干细胞突变增加伴随克隆性竞争:
干细胞库中的细胞异质性导致干细胞之间竞争,人类中的示例为“克隆性造血”,即一个或几个造血干细胞克隆随着时间的推移不成比例地促进血液生成。在克隆性造血中扩增的干细胞通常在编码表观遗传调节因子的基因中具有体细胞突变。克隆性造血增加了恶性肿瘤发展的风险,是血液肿瘤发生发展的基础。克隆性扩增也发生在其他组织,比如肌肉中也见报道,但其与衰老的关系还需进一步研究。突变发生与克隆性扩增的变异程度之间的关联仍有待确定,包括结肠和肝脏在内的几种干细胞类型已被证明在衰老过程中以稳定的速度获得体细胞突变,这可能是通用的,但需要动物模型来进行研究与证明。
▉ 衰老标志物的积累:
衰老过程中,干细胞积累特定的衰老相关转录组和蛋白质组标志。转录谱的变化反映了细胞损伤和衰老标志物的积累。在肌肉中,衰老会导致转录异质性增加,尤其体现在影响干细胞-生态位互作的基因中;在皮肤中,干细胞也表现处转录变化,伴随着细胞外基质(ECM)蛋白表达的增加;在骨髓中,衰老的HSC也表现转录异质性增加,但含细胞黏附标志物的一组标志物始终随衰老而上调,这可能也指示了炎症状态和偏倚分化。
总而言之,衰老干细胞的一个共同特征是其产生功能性子代细胞的能力降低。然而,在衰老过程中,干细胞增殖与分化能力的具体改变、功能衰退的时间和分子缺陷的类型可能因组织不同或年龄时间点的不同而存在差异。
-03-
衰老过程中干细胞微环境的缺陷
最近的研究进展揭示:不仅干细胞本身,构成微环境细胞(除干细胞之外)和微生物本身环境及其物理特性也随着衰老而变化。
在衰老过程中,构成微环境细胞的年龄依赖性变化:
单细胞RNA-seq分析揭示了微环境组成的强烈变化(即干细胞本身以外的不同细胞类型的比例)以及衰老过程中特定干细胞微环境细胞的转录组变化。
例如,在SVZ神经源性微环境中,RNA-seq揭示了11种细胞类型(包括内皮细胞、小胶质细胞、少突胶质细胞和周细胞)的存在。衰老伴随着这些生态位细胞的强烈转录变化,如内皮细胞(形成血管)和小胶质细胞(大脑中的巨噬细胞),这与炎症变化一致。在肌肉中,定量蛋白质组学研究也发现了组织的强烈变化,尤其是ECM成分的增加。随着年龄的增长,许多组织中的生态位细胞也会经历剧烈的转录组变化,这可能会间接损害干细胞的功能。
干细胞微环境中不同免疫细胞浸润是衰老的一个关键标志。事实上,单细胞RNA测序结果表明,克隆扩增的具有细胞毒性的CD8+ T细胞在老年神经源性微环境中发生浸润。免疫荧光染色证实:在老年小鼠和人类的再生区域中存在T细胞浸润。衰老的大脑和其他组织中也观察到克隆性扩增的T细胞和B细胞的浸润。相反,其他免疫细胞(如Treg细胞)在衰老的皮肤中数量减少,这可能导致该再生微环境的组织调节失衡。在未来,精准识别干细胞微环境中存在的免疫细胞,并确定其克隆扩增是否由衰老特异性抗原导致,具有重要意义。
▉ 可溶性因子和干细胞环境的衰老变化:
干细胞微环境也随着衰老发生变化,可溶性因子(细胞因子、生长因子、代谢物和营养物质)出现变化。例如,因为免疫细胞的浸润、巨噬细胞和小胶质细胞的活化,以及衰老细胞的存在,神经干细胞微环境可能因为衰老变得发生炎症。炎症细胞因子(包括干扰素和IL-33和CXCL10等),在神经干细胞微环境中被上调。其他炎症细胞因子(包括TNF、TGF-β1、IL-6和IL-1β),在老年骨髓(造血干细胞微环境)中上调。
干细胞微环境生理特性的衰老变化:
干细胞微环境在衰老过程中硬化,并且细胞外基质(ECM)组成发生剧烈的变化。在衰老的脑组织中观察到硬度在持续增加。在骨髓中,淋巴祖细胞微环境含有参与成骨的机械敏感细胞。在骨骼肌中,细胞外基质成分也会随着年龄的增长而变化。肌肉微环境中,胶原蛋白弯曲度随着衰老而降低,微环境硬度则随着衰老而增加,这可能与肌肉干细胞异常的分化有关。在皮肤中,细胞外基质蛋白增加,并伴随微环境硬化和毛干小型化。总之,随着衰老,干细胞微环境的周围环境可能变得僵硬、炎症也会加重,这可能使干细胞出现缺陷。
-04-
组织衰老和疾病中的干细胞
干细胞的功能衰退是组织衰老的核心特征。干细胞和微环境的衰退,一般会影响衰老过程中的器官退行。我们需要知道的另一个重要问题是干细胞在衰老相关疾病中的作用。
本节回顾干细胞微环境在衰老和疾病中组织功能衰退中的作用。
▉ 组织干细胞的强制消耗
组织中干细胞数量的减少,通常会导致衰老过程中组织衰退的发生。例如,骨骼肌中纤维脂肪生成祖细胞的消耗导致肌少症的衰老组织表型。相比之下,尽管肌肉干细胞的强制消耗可能参与修复缺陷,但本身并不足以导致肌肉衰退(肌少症)。
在大脑损伤时,由神经干细胞分化的胶质细胞和神经元能够迁移到损伤部位并改善修复。因此,精准检测衰老过程中干细胞在组织功能和修复的各方面作用将会很有趣。需要注意的是,衰老引起的干细胞数量减少的速度,比遗传因素较缓慢。有趣的是,在一些再生区域(比如造血干细胞微环境)中,干细胞的数量随着衰老而升高。
因此,人们需要精准模拟衰老相关变化的幅度和类型,以检测干细胞对体内平衡和修复下降的贡献。第一种是:损害干细胞功能,使其衰老。第二种是:移植衰老干细胞。例如,将衰老的脂肪间充质干细胞腹腔移植至老龄小鼠体内,会导致行走速度和握力下降等虚弱表型的增加。<步步先生注:这个很有意思>
▉ 干细胞耗竭与衰老相关疾病的关系
干细胞数量减少和功能衰退,可能也是衰老相关疾病发生的基础。在造血系统中,细胞突变驱动造血干细胞功能障碍,导致衰老相关的骨髓增生异常综合征,且衰老的炎症环境可加剧病情。造血干细胞中的体细胞突变,可进行克隆造血,通过所有下游血液谱系传播,导致血液循环异常,进而影响远端组织的功能,并导致心血管疾病和其他年龄相关疾病。
虽然关于成人海马中新神经元的形成存在争议。同龄人相比,阿尔茨海默病患者的海马神经功能衰退速度似乎加快了。事实上,参与阿尔茨海默病的风险因子基因突变会损害微环境细胞(星形胶质细胞和小胶质细胞),进而可能改变神经干细胞的功能。因突变而患有其他神经退行性疾病的患者(例如,帕金森病、亨廷顿病和肌萎缩侧索硬化症)表现为星形胶质细胞和小胶质细胞的数量(以及新生神经元的异常形态)异常增加,不过神经干细胞的数量受到的影响不大。总之,神经源性微环境和神经干细胞功能衰退可能衰老相关疾病发生的基础,尤其是阿尔茨海默病。
▉ 增强干细胞在健康和寿命方面的功能
目前,在衰老细胞被年轻细胞替代,或衰老细胞原位再生的情况下,干细胞功能增强对维持健康和延长寿命是令人信服的。<步步先生注:文章肯定了干细胞移植的保健和抗衰作用>
总的来说,在干细胞更新勤快的组织中(如血液和肠道),如果干细胞出现功能障碍,可能会在衰老和疾病期间造成组织衰老;在干细胞更新懒惰的组织中(比如肌肉和大脑),如果干细胞出现功能障碍,可能在疾病、损伤修复能力下降时候更为重要。在没有干细胞更新的组织中(比如心脏和脊髓),衰老可能具有不同的(在分子水平和细胞水平)总体特征。
因此,需要我们搞清楚的是:干细胞哪些特征对组织衰老、疾病和修复最为关键,在有干细胞和无干细胞的器官或组织中,组织衰老的差异到底有什么不同。
参考文献: https://doi.org/10.1038/s41580-022-00510-w
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言