ANNIE研究:安罗替尼联合尼拉帕利可作为铂耐药卵巢癌的后线治疗
2024-03-23 苏州绘真医学 苏州绘真医学 发表于上海
在这项研究中,研究人员评估了尼拉帕利-安罗替尼联合治疗在PROC患者的活性和安全性。
根据 2023 年妇科肿瘤学会(SGO)女性癌症年会上公布的 2 期ANNIE试验(NCT0437607)的敏感性分析数据,多激酶抑制剂安罗替尼(AL3818)联合使用PARP抑制剂尼拉帕利(Zejula)为铂耐药复发性卵巢癌患者带来了总生存期(OS)获益,安全性良好。在最终生存分析中,联合治疗的患者(n = 40)的中位OS更新为 18.2 个月(95% CI, 12.1-未达到)。值得注意的是,数据截止时(2022 年 7 月 7 日),已有 18 例患者死亡。该研究的主要作者及其同事写道:“在随后的长期随访中,尼拉帕利联合安罗替尼显示出良好的安全性和有效性,可作为铂耐药卵巢癌晚期治疗的一种选择。”
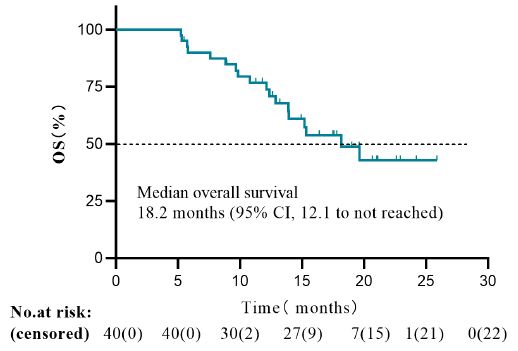
▲2023年SGO更新的OS
背 景
上皮性卵巢癌(包括上皮性卵巢癌、输卵管癌和原发性腹膜癌)是女性癌症死亡的主要原因之一。由于缺乏有效的筛查方法,超过 70% 的患者确诊时已处于晚期。尽管患者最初会对基于铂类和紫杉类的化疗有反应,但大多数患者都会在 2 年内复发。随着复发间隔时间的逐渐缩短,这些患者最终会从铂敏感的复发进展为铂耐药的复发。
对于铂耐药复发性卵巢癌(PROC)患者,可供选择的有效治疗很少。标准的非铂类化疗,如紫杉醇、PLD和拓扑替康,客观缓解率(ORR)为 10%-30% ,无进展生存期(PFS)为 2-5 个月。在其它获批的治疗方案中,在化疗中添加抗血管生成药物贝伐珠单抗时,显著改善PFS和ORR,但不良事件的发生率有所增加。PARP抑制剂奥拉帕利和尼拉帕利可用于既往治疗≥ 2 或≥ 3 线的铂耐药患者,但需要患者携带BRCA突变或同源重组缺陷(HRD)。此外,还需要耐受性更好的方案。因为许多铂耐药患者先前已经接受过多线化疗,身体状况差,无法耐受足额剂量或频率的进一步化疗。静脉输注贝伐珠单抗和化疗也给患者带来不便,并可能影响生活质量。
抗血管生成药物和PARP抑制剂都在卵巢癌治疗中发挥着重要作用,它们的联合使用已经取得了进展。在HRD细胞中,PARP抑制剂会导致细胞无法修复DNA双链断裂并累积,进而使基因组不稳定性增加,最终令细胞死亡。临床前研究表明,抗血管生成药物可通过微环境缺氧和同源重组修复基因下调诱导HRD,从而使肿瘤细胞对PARP抑制剂敏感。相反,PARP1可能与血管生成有关,因此PARP抑制剂可能带来额外的抗血管生成作用。这就是抗血管生成和PARP抑制剂之间潜在协同作用的机制基础。值得关注的是,这两类药物联合使用是否会提高治疗PROC的疗效,迄今为止只有西地尼布联合奥拉帕利被广泛评估。
中国的一些医疗机构发现PARP抑制剂尼拉帕利联合抗血管生成安罗替尼临床应用于PROC患者(完全知情同意),这些患者多线化疗失败,缺少其它有效的治疗方案。通过对这些患者的观察获得了临床疗效的初步证据,表明尼拉帕利-安罗替尼联合治疗可能是一种新的治疗选择,值得在这一难以治疗的患者群体继续探索。
尼拉帕利是一种高选择性PARP 1/2抑制剂,获批用于新诊断或铂敏感性复发性卵巢癌的维持治疗,以及在HRD且铂敏感的情况下作为四线或后线治疗。即使在晚期HRD阴性卵巢癌患者的早期治疗和后线治疗中,尼拉帕利也显示出一定的临床获益。在AVANOVA研究中,对于铂敏感的复发性卵巢癌患者,尼拉帕利联合贝伐珠单抗的疗效优于尼拉帕利单药,且不良反应可耐受。
安罗替尼是一种口服小分子受体酪氨酸激酶抑制剂(TKI),靶向VEGFR1/2/3、c-Kit、PDGFR-α和成纤维细胞生长因子受体(FGFR1/2/3),对肿瘤血管生成和生长具有广谱抑制作用。安罗替尼在中国获批用于几种癌症类型的挽救治疗,包括肺癌和软组织肉瘤。证据显示安罗替尼对铂耐药卵巢癌有一定的疗效。尼拉帕利和安罗替尼具有不同的代谢途径,因此药物相互作用最低,有利于这两种药物的安全联合使用。在这项研究中,研究人员评估了尼拉帕利-安罗替尼联合治疗在PROC患者的活性和安全性。
ANNIE研究
研究设计
ANNIE研究(NCT04376073)是在中国三家医院进行的一项单臂、开放标签的 2 期临床试验。研究方案由各参与地点的机构审查委员会批准,并获得每位参与患者的书面知情同意。中山大学肿瘤防治中心委员会对这项研究进行了监督。
入组患者需符合如下要求:年龄在 18-70 岁;组织学证实为卵巢上皮癌、输卵管癌或原发性腹膜癌;在最后一次接受铂类治疗后不到 6 个月内复发;有可测量的病灶(基于RECIST v1.1标准);入组前必须有可用的胚系(gBRCA)或肿瘤(tBRCA)BRCA检测结果,任何BRCA或同源重组状态的患者都符合条件;患者的预期寿命必须超过 16 周;ECOG评分为 0 或 1 ;以及足够的器官功能。既往接受过抗血管生成治疗的患者可以入组,但既往接受过PARP抑制剂的患者被排除在外。接受铂类化疗的线数没有限制。有以下情况的患者被排除在外:对研究药物过敏;有症状的脑转移;三周内进行过大手术;两年内患有卵巢癌以外的其它癌症;无法控制的心血管疾病。
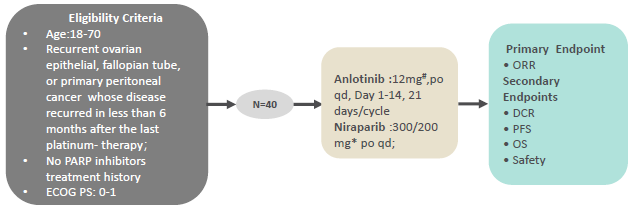
▲研究设计
研究流程
符合条件的患者在连续 21 天的周期内接受尼拉帕利联合安罗替尼治疗。在每个周期的 1-14 天,每天口服 12 mg或 10 mg安罗替尼(QD)——在期中分析前 23 名患者时,观察到的毒性主要是手足综合征(n = 8,2 例≥ 3 级)和高血压(n = 7,1 例≥ 3 级),因此,2020 年 11 月 25 日将安罗替尼的起始剂量从 12 mg QD减少到 10 mg QD。尼拉帕利每日口服 300 mg(QD,如果基线体重≥ 77 kg)或 200 mg(QD,如果基线体重< 77 kg)。第一次给药必须在前一次抗肿瘤治疗结束 4 周后(如果前一次治疗方案含有丝裂霉素,则为 6 周)。
患者会持续接受治疗,直到疾病进展、出现不可接受的毒性、撤回同意、死亡或失去随访,以最先发生的事件为准。允许通过剂量调整管理不良事件,安罗替尼和尼拉帕利的剂量可以根据研究者决定相互独立地减少或中断。中断的最长时间为 28 天。
从 2020 年 5 月 22 日至 2021 年 4 月 22 日,从中国 3 个地点招募了共 40 例患者(图1)。40 例患者均接受了尼拉帕利和安罗替尼治疗,构成了ITT人群。只有 1 名体重 78 公斤的患者接受了 300 mg尼拉帕利的起始剂量。目前分析的截止日期为 2022 年 1 月 31 日,随访工作正在进行中。中位随访时间为 15.4 个月(95% CI,12.6-17.7)。根据数据截止日期,有 4 名患者仍在接受治疗。停止治疗是由于疾病进展(n = 24)、不良事件(n = 5)、患者请求(n = 6)和违反治疗方案(n = 1,接受化疗)。
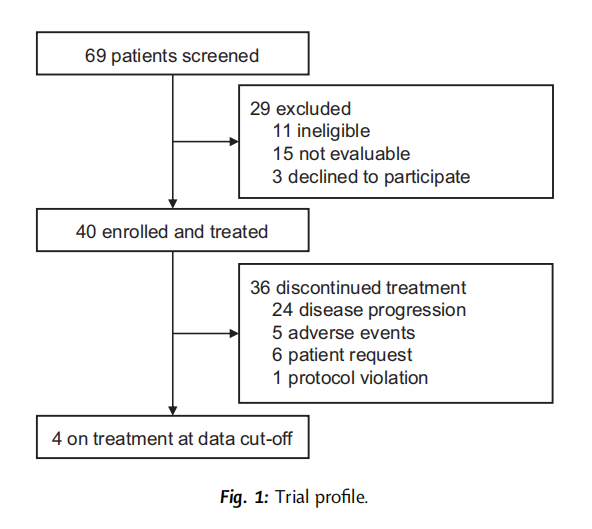
▲图1 研究流程
主要终点是ORR(确认完全或部分缓解患者的百分比),次要终点包括PFS、至症状缓解时间(TTR)、缓解持续时间(DOR)、无铂类治疗间期(PFI)和总生存期(OS)(基于RECIST v1.1标准)。安全性终点包括治疗不良事件(TEAE)的发生率、严重程度和药物相关性。
基线数据
表1 总结了基线人口统计学和临床特征。中位年龄为 54 岁(范围为 37-69 岁)。肿瘤病理学显示主要是高级别浆液性腺癌,大多数患者在诊断时有III期或IV期疾病。患者接受了中位 4 线的化疗(范围1-9)。大多数患者(68%,27/40)之前曾接受过抗血管生成治疗。5 例患者携带BRCA胚系突变(gBRCAmut)。
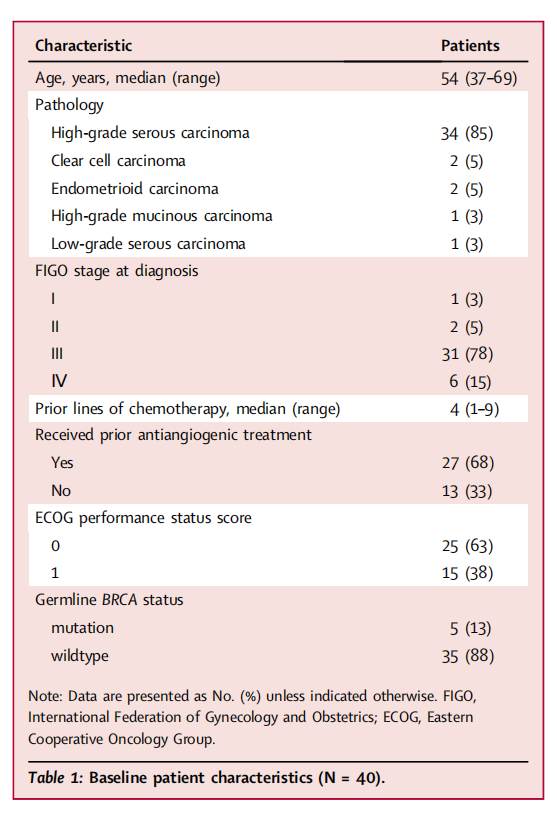
▲表1 患者特征和基线数据
相关数据
疗效数据
数据截止时,ITT人群中的ORR为 50.0%(95%CI,33.8-66.2),包括 1 例完全缓解和 19 例部分缓解(表2)。4 例患者在没有进行基线后肿瘤评估的情况下退出,剩下 36 例患者(包括疗效可评估人群),ORR为 55.6%(95%CI,38.1-72.1)。根据最佳总体反应,36 例可进行疗效评估的患者中有 31 例(86%)靶病灶直径减少(图2)。基线期检出gBRCA突变患者的ORR为 100%(95%CI,47.8-100,5/5例患者),而gBRCA野生型患者的ORR为 42.9%(95%CI,26.3-60.6;15/35例患者)。30 例接受了肿瘤评估的高级别浆液性腺癌患者的ORR为 50.0% 。研究结束后的亚组分析没有发现其它影响PFS的因素,中位TTR、DOR和PFI的分别为 2.8 个月(95%CI,1.6-4.9)、6.9 个月(95%CI,4.2-9.7)和 13.2 个月(95%CI,11.0-17.7)。有 24 例PFS(均为疾病进展),中位PFS为 9.2 个月(95%CI,7.4-11.9),6 个月PFS率为 81.17%(95% CI,62.75–91.08)(图3A)。

▲表2 肿瘤反应评估
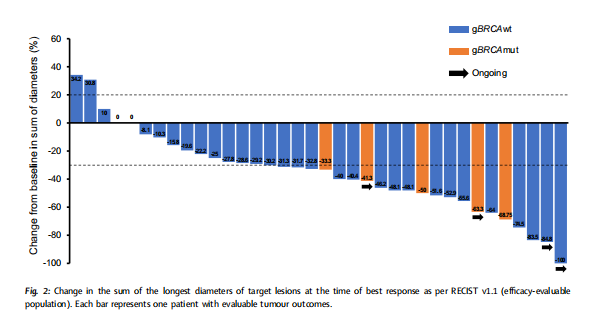
▲图2 最佳反应时靶病灶最长直径之和的变化
数据截止时,有 17 例患者死亡,中位OS为 15.3 个月(95%CI,13.9-不可评估)(图3B)。之前接受过抗血管生成药物对PFS没有影响。既往使用抗血管生成药物和化疗线数不影响OS。
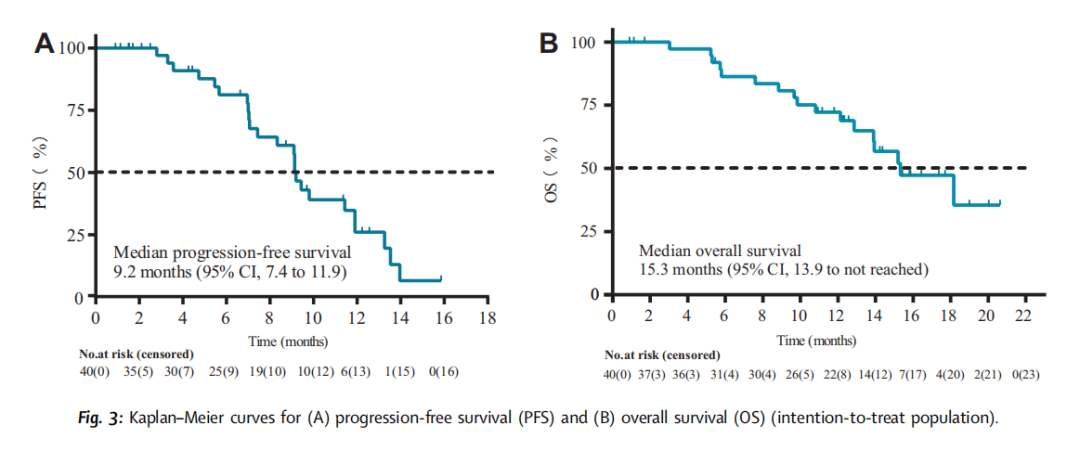
▲图3 PFS(左)和OS(右,SGO更新前的数据)
安全性
最常见的任何级别TEAE(表3)是高血压(22例,55%)、白细胞减少(18例,45%)和手足综合征(17例,43%)。药物相关≥ 3 级TEAE报告 26 例(68%),其中 1 例以上的有:中性粒细胞计数减少(7例,18%),手足综合征(6例,15%),贫血和高血压(5例,13%),血小板计数减少和白细胞计数减少(4例,10%),高甘油三酯血症和肠梗阻。未记录到与治疗相关的死亡或骨髓增生异常综合征。
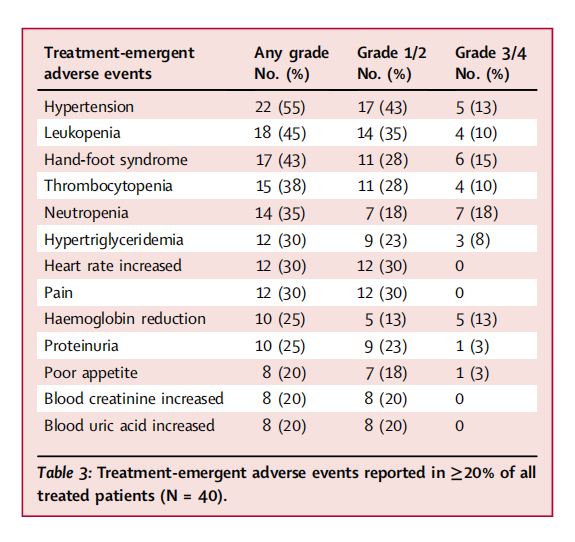
▲表3 超过20%患者出现的治疗相关不良事件
探索性分析
为了对循环肿瘤标志物进行探索性分析,从 12 名患者中获得 56 份血浆样本。根据ctDNA的结果,3 名基线期检出BRCA突变的患者都取得了客观缓解,而 8 例基线期检出BRCA野生型的患者中,只有 1 例获得客观缓解(P = 0.024)。基线SPEN突变患者与基线无SPEN突变患者相比,在最佳反应时观察到更大的肿瘤体积缩小(P = 0.048)。相反,PPM1D野生型患者比PPM1D突变患者经历了更大的最佳反应肿瘤体积缩小(P = 0.048)。PPM1D的变异等位基因频率随着治疗周期和肿瘤变化率的增加而增加。
讨 论
目前PROC患者的治疗选择非常有限,本研究表明尼拉帕利-安罗替尼联合治疗在PROC中是有效的,在肿瘤缓解和PFS方面产生了临床疗效。联合用药耐受性良好,与单药治疗的安全性相比,没有观察到新的安全性信号。因此,尼拉帕利-安罗替尼联合治疗可能为PROC患者提供一种潜在的新治疗方案。
既往研究证实了抗血管生成药物和PARP抑制剂联合治疗铂敏感性卵巢癌的价值。在铂耐药疾病中,PARP抑制剂单药在有BRCA突变和没有BRCA突变的患者中ORR分别约为 25%-35% 和< 5%。同样,抗血管生成TKI单药在铂耐药疾病中的ORR为 0%-20% 。在本文的研究中,50% 的ITT人群获得了客观缓解,这支持了两种药物联合使用时抗肿瘤活性增强的理论。由于贝伐珠单抗被广泛推荐用于晚期或复发性卵巢癌,本研究中的大多数患者先前都接受过抗血管生成治疗,本文的研究结果表明,抗血管生成治疗史似乎并不影响随后安罗替尼与尼拉帕利联合应用的疗效。
在PROC中评估的另一种抗血管生成药物-PARP抑制剂组合是西地尼布联合奥拉帕利。从 4 项 2 期研究(NCT02345265、CONCERTO、BAROCCO、OCTOVA)中观察到,西地尼布-奥拉帕利在患/不患有gBRCA突变的患者中ORR为 15%-20% ,中位PFS为 5.1-5.6 个月,在数字上比每周使用紫杉醇的患者(3.1-3.9个月)更长,但统计优势尚未建立。在本文的研究中,只在 13%(5/40)患有gBRCA突变的患者组中,ORR达到了 50%。这是令人鼓舞的,表明尼拉帕利-安罗替尼可能克服了PARP抑制剂单一治疗的生物标志物限制,能让更广泛的铂耐药患者受益。同样值得注意的是,研究中的中位PFS超过半年,转化为相当长的PFI。一些患者在研究治疗结束后对进一步含铂化疗表现出反应,这是一个有意义的观察结果,需要进一步的研究来验证。
在对ctDNA的探索性分析中,无法确定与显著疗效相关的分子生物标志物。在分析中发现,PPM1D突变的存在和积累似乎与较差的肿瘤反应相关。PPM1D参与调节OVCA细胞的化疗敏感性,并且在弥漫性内生性脑桥胶质瘤(DIPG)中发现PPM1D抑制会使PPM1D突变型DIPG细胞对PARP抑制剂治疗敏感。本文的结果与这些早期发现一致,这些发现表明PPM1D突变可能与PARP抑制剂耐药性有关,从而导致较差的肿瘤反应。本文分析还显示,SPEN突变患者的肿瘤反应更好。目前,关于SPEN和卵巢癌的报道非常有限。SPEN与肿瘤反应之间的关系及其潜在机制有待进一步研究。
联合治疗应提供增强的疗效而不增加毒性。在本文的研究中,与各自的单药安全性相比,尼拉帕利-安罗替尼没有观察到新的安全性信号。血液毒性(尤其是贫血)的发生频率低于其他尼拉帕利试验。这可能与安罗替尼产生的缺氧环境有关,安罗替尼通过缺氧诱导因子调控促红细胞生成素的表达来促进红细胞生成。与早期使用固定起始剂量 300 mg的尼拉帕利研究不同,本文的研究使用了基于体重的个体化起始剂量,大多数患者从 200 mg开始使用尼拉帕利。此外,通过严格的血常规检查,一旦患者血小板水平降至 100,000 /μL以下,会立即停用研究药物。这些措施可能有助于降低 3-4 级血小板减少的发生率。与既往研究相比,安罗替尼相关的常见不良事件,如高血压、手足综合征和某些生化指标异常的发生率没有增加。本研究3-4级TEAE主要为中性粒细胞减少症、手足综合征、高血压和贫血,均为可管理和控制的AE。值得注意的是,晚期患者往往骨髓功能较差,因此更容易发生与骨髓抑制相关的≥ 3 级TEAE。研究人员计划在未来的研究中通过可能的剂量优化进一步探索TEAE的预防和管理。
大多数小分子TKI如安罗替尼、西地尼布、帕唑帕尼和阿帕替尼通过CYP450途径代谢,大多数PARP抑制剂如奥拉帕利、卢卡帕利、帕米帕利和氟唑帕利也是如此。因此,抗血管生成和PARP抑制剂联合使用的最大耐受剂量通常低于单一药物的完整临床剂量。在西地尼布-奥拉帕利的研究中,西地尼布(每次20mg而不是每次30mg)或奥拉帕利(每天两次200 mg [BID]而不是300mg BID)需要降低剂量水平;通过间歇性给药的方式进一步减少了剂量,从而提高了安全性,但这是以牺牲PFS为代价的。相比之下,尼拉帕利通过羧酸酯酶代谢,与通过CYP450途径代谢的药物之间的相互作用最小。在本文的研究中,尼拉帕利和安罗替尼都以常规临床剂量给药,并且耐受性良好。使用完整剂量可能有利于疗效的优化,并在必要时为管理TEAE和改善患者的生活质量提供更多的剂量调整空间。
这项研究有几个局限性。首先,这是一项单臂、小样本量的 2 期研究。虽然有观察到ORR增加和PFS延长的趋势,但长期疗效需要在大型试验中验证。其次,HRD状态与疗效之间的关系无法确定,因为很难从大量经治患者群体中获得有效的标本。第三,本研究排除了先前暴露于PARP抑制剂的患者,鉴于PARP抑制剂在卵巢癌的广泛一线应用,这些患者可能占PROC患者的相当大的比例。计划进行一项扩展研究(ANNIE Plus),纳入先前接受PARP抑制剂治疗的患者,以加强研究结果的临床相关性。四是新冠肺炎疫情导致部分患者无法定期现场随访。研究人员进行了密切的电话随访,邮寄研究药物,并在可能的情况下引导患者前往当地医院,以尽量减少无法现场随访的影响。ANNIE是一项早期非随机研究,旨在初步探索尼拉帕利-安罗替尼在PROC中的应用,而这种组合的临床应用有待进一步的证据支持,例如随机对照试验的结果。ANNIE和ANNIE Plus研究的结果有望为未来的此类随机对照试验提供信息。
结 论
本研究显示,尼拉帕利-安罗替尼联合治疗在PROC中具有活性,具有在肿瘤缓解和PFS方面的临床疗效。联合用药的耐受性良好,与单药治疗的安全性相比,没有观察到新的安全信号。总之,尼拉帕利-安罗替尼联合治疗对PROC患者显示出良好的抗肿瘤活性和可耐受的毒性。这种口服、无化疗的联合治疗可能代表了PROC患者的一种潜在的、新的治疗选择。
参考文献:
[1]Liu G, Feng Y, Li J, Deng T, Yin A, Yan L, Zheng M, Xiong Y, Li J, Huang Y, Zhang C, Huang H, Wan T, Huang Q, Lin A, Jiang J, Kong B, Liu J. A novel combination of niraparib and anlotinib in platinum-resistant ovarian cancer: Efficacy and safety results from the phase II, multi-center ANNIE study. EClinicalMedicine. 2022 Nov 30;54:101767. doi: 10.1016/j.eclinm.2022.101767. PMID: 36583171; PMCID: PMC9793276.
[2]ANNIE Data Support Anlotinib/Niraparib Combo as Late-line Option in Platinum-resistant Ovarian Cancer.https://www.onclive.com/view/annie-data-support-anlotinib-niraparib-combo-as-late-line-option-in-platinum-resistant-ovarian-cancer
[3]Liu G, Xian B, Li J, et al. Updated survival and safety results from the phase 2 study (ANNIE) of anlotinib and niraparib dual therapy evaluation in platinum-resistant recurrent ovarian cancer. Presented at: 2023 Annual Meeting on Women’s Cancer; March 25-28; Tampa, Florida. Poster 314.

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#安罗替尼# #尼拉帕利# #卵巢癌#
14