学术交流|辛颖教授:内质网应激触发的铁死亡通过XBP1-Hrd1-Nrf2途径促进糖尿病肾病的EMT进展
2024-01-19 医悦汇 医悦汇 发表于陕西省
考虑到ERS和铁死亡在细胞中的不同机制,作者提出ERS激活可能参与了触发糖尿病肾病EMT进展过程中肾小管上皮细胞铁死亡的作用。
研究背景
糖尿病肾病是一种严重的糖尿病微血管并发症,影响40%的糖尿病患者,已成为全球终末期肾病的主要原因。糖尿病肾病进展为慢性肾功能衰竭的最终途径是肾小球硬化和肾小管间质纤维化。在病理状态下,肾小管上皮细胞经过上皮间充质转化(EMT)失去上皮表型,分化为成纤维细胞/肌成纤维细胞,分泌细胞因子和趋化因子促进细胞外基质的合成,最终导致肾功能恶化和肾小管间质纤维化。肾小管EMT被认为是导致肾功能衰竭的主要病理特征。抑制EMT可以减轻糖尿病肾病的肾功能障碍,逆转间质纤维化的进展。
在EMT进展过程中,肾小管上皮细胞中存在过量的活性氧(ROS)。过量的ROS攻击生物膜,诱导脂质过氧化,导致各种形式的细胞死亡,如自噬、细胞凋亡和铁死亡。在糖尿病肾病中,ROS产生加速EMT发展的具体细胞死亡类型尚未明确。在糖尿病肾病小鼠和高糖培养的人肾小管上皮细胞中,转铁蛋白受体1(TFR-1)的表达上调和溶质载体家族7成员11(SLC7A11)的表达下调增加了脂质的Fe2+氧化、谷胱甘肽(GSH)的耗竭和Gpx4的合成减少,从而产生羟基和脂类烷氧自由基,产生ROS并促进糖尿病肾脏损伤。另有研究观察到高糖处理后肾小管上皮细胞线粒体脊减少和双层膜密度增加。提示铁死亡可能参与了糖尿病肾病的EMT过程。
内质网应激(ERS)是EMT进展过程中的重要影响因素。在糖尿病肾病小鼠和高糖处理的HK-2细胞中,ERS因子ATF6和GRP78的表达水平增加。并有研究表明,ERS在铁死亡发生时增加。考虑到ERS和铁死亡在细胞中的不同机制,作者提出ERS激活可能参与了触发糖尿病肾病EMT进展过程中肾小管上皮细胞铁死亡的作用。
实验结果
铁死亡参与了糖尿病肾病小鼠EMT的进展
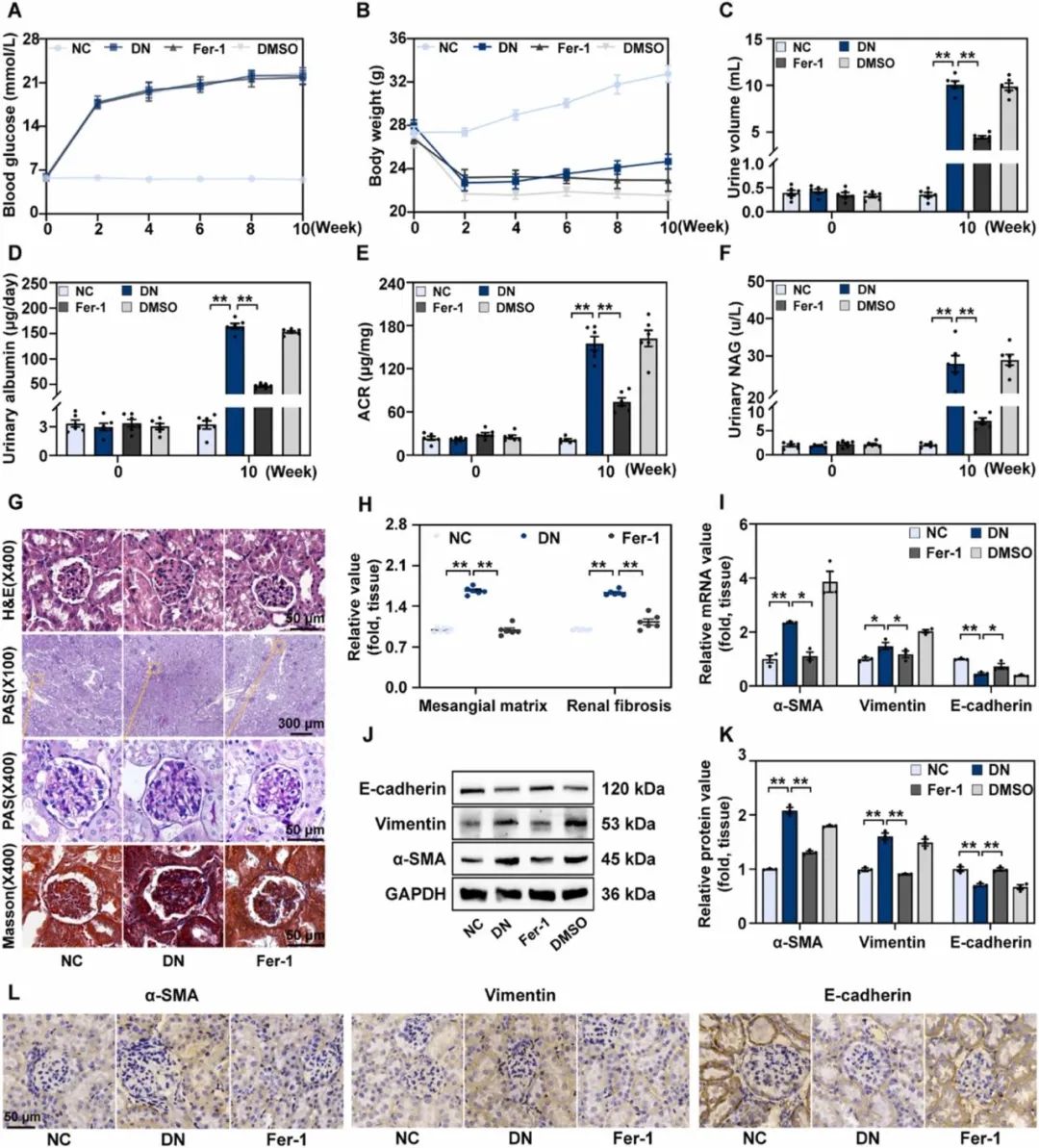
糖尿病小鼠连续5天注射链脲佐菌素建立糖尿病模型,糖尿病进展期间给予铁死亡抑制剂Fer-1治疗8周。在实验期间,糖尿病肾病组、Fer-1组和DMSO组的小鼠有相似的高血糖进展曲线。注射链脲佐菌素后,各组小鼠的血糖水平均达到18 mmoL/L,并逐渐升高,而正常对照组(NC组)小鼠的血糖水平约为7 mmoL/L(图1A)。注射链脲佐菌素后,NC组大鼠体重缓慢增加,其他各组大鼠体重显著下降,随后出现轻微波动(图1B)。处死小鼠前,检测24 h尿量、24 h尿蛋白尿和ACR,以评价糖尿病肾病模型的建立。在糖尿病肾病的发展过程中,与正常对照组相比,糖尿病肾病组的24小时尿量、24小时尿蛋白尿和ACR显著增加,而Fer-1治疗逆转了这些变化(图1C-E)。尿NAG是近端肾小管上皮细胞中的一种酶,用于评估肾小管损伤。糖尿病肾病小鼠尿NAG显著增加,经Fer-1治疗后得到缓解(图1F)。肾脏切片H&E染色显示,糖尿病肾病小鼠的肾小球体积大于NC组。PAS和Masson‘s染色显示,糖尿病肾病组小鼠肾小球系膜基质扩张和胶原纤维沉积较NC组明显,提示糖尿病肾病小鼠肾脏纤维化进展。在Fer-1治疗后,小鼠的这些组织病理学变化明显减轻(图1G-H)。此外,作者评估了Fer-1对肾组织中EMT相关指标的影响,以进一步证实EMT进展过程中铁死亡的行为。糖尿病肾病组小鼠E-钙粘蛋白基因和蛋白表达水平降低,α-SMA和Vimentin表达显著增加,而Fer-1治疗后这些指标的变化有所改善(图1I-K)。
铁死亡诱导高糖介导的HK-2细胞内皮细胞转化
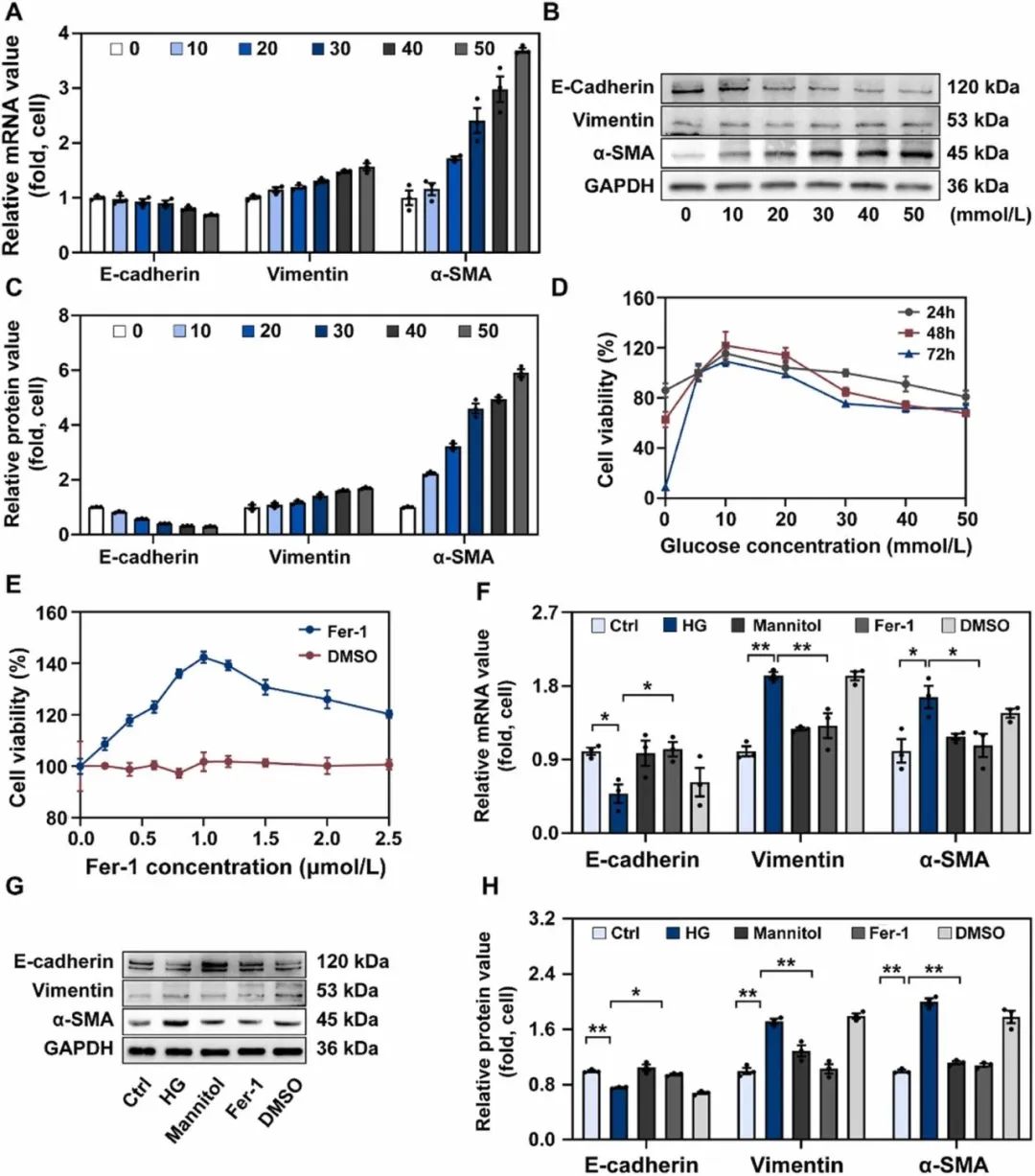
用不同浓度的葡萄糖(0~50 mmol/L)处理HK-2细胞,观察高糖对细胞内皮细胞转化的影响。葡萄糖以剂量依赖的方式诱导E-cadherin mRNA表达显著降低,SMA和Vimentin mRNA水平升高(图2A)。且蛋白质水平与mRNA表达一致(图2B-C),表明HK-2的EMT进展受到高糖刺激影响。随后作者用30 mmol/L葡萄糖处理HK-2细胞48h后,细胞存活率显著下降(图2D)。同时进行CCK8实验发现细胞存活率在1μM Fer-1时达到最大水平(图2E)。在高糖条件下,检测1μM Fer-1处理的HK-2细胞中EMT相关分子的表达,探讨铁死亡抑制对EMT进展的影响。Fer-1(图2F)可减轻高糖引起的E- cadherin基因表达下调、Vimentin和α-SmA基因表达上调。且每组的蛋白质表达都有相似的变化(图2G-H)。以上结果表明,高糖通过铁死亡促进了HK-2细胞EMT的进展。
ERS在体内和体外参与EMT的进展
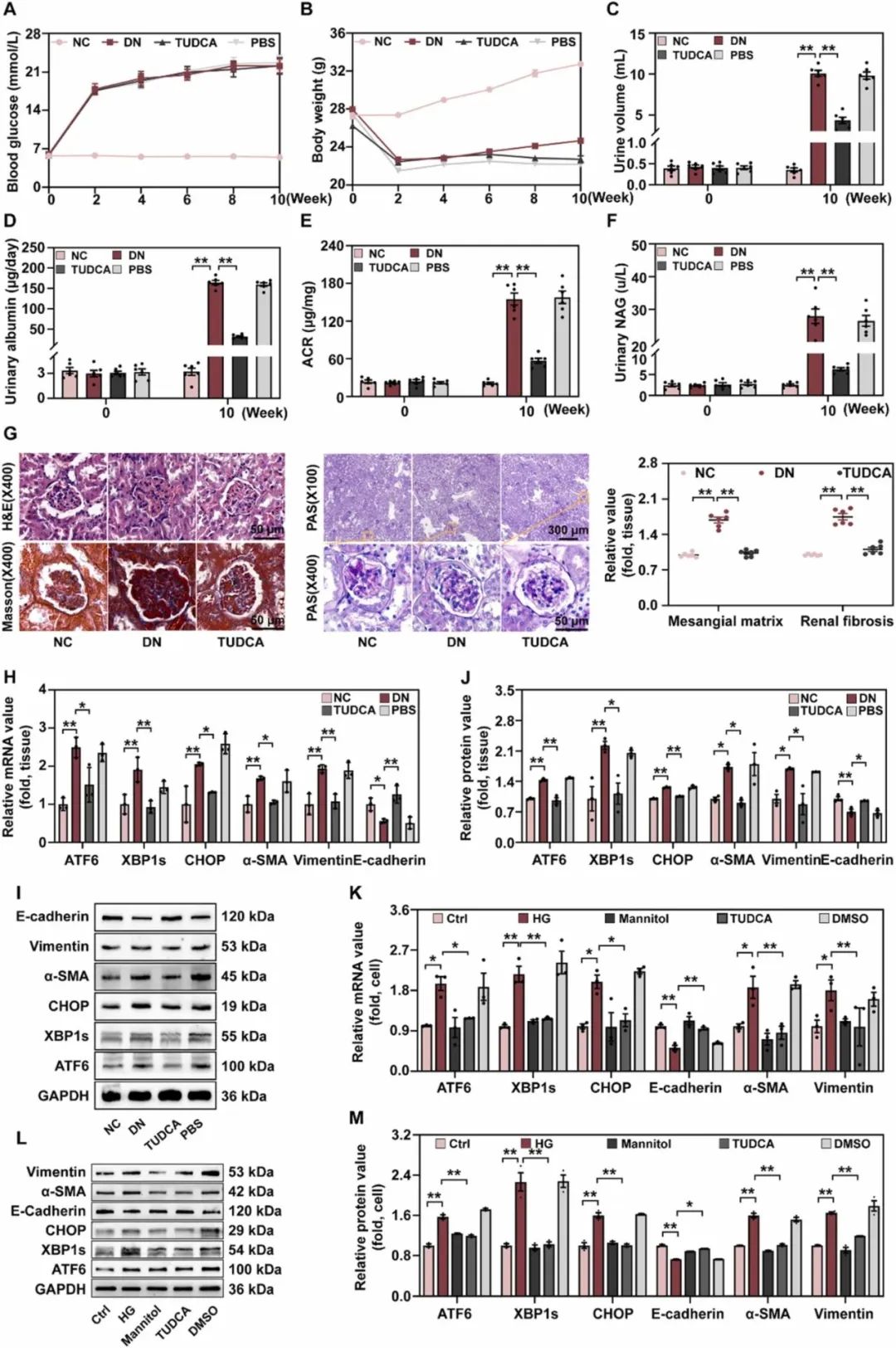
在动物实验中,在连续注射链脲佐菌素5天后,糖尿病肾病组、TUDCA(内质网应激抑制剂)组和PBS组的血糖水平显著上升,而NC组小鼠的血糖水平维持在大约7 mmol/L(图3A)。相反,DN、TUDCA和PBS组的体重低于NC组(图3B)。与NC组,糖尿病肾病组小鼠的24小时尿量、24小时尿蛋白尿、ACR和24小时尿NAG均增加,而TUDCA可逆转这些影响(图3C-F)。H&E染色显示,糖尿病肾病小鼠肾小球体积较正常对照组大,包膜受压程度较重。PAS和Masson‘s染色显示糖尿病肾病小鼠肾小球胶原纤维沉积,系膜基质扩张。TUDCA治疗减轻了这些组织病理学改变(图3G)。此外,作者进一步检测了NC组、糖尿病肾病组、TUDCA组和PBS组ERS标志物和EMT相关分子的表达,以确认高糖暴露是否在EMT进展过程中激活了ERS。糖尿病肾病组肾组织ATF6、XBP1s和CHOP的mRNA和蛋白表达水平显著升高,提示高糖激活了肾脏ERS。另外,高糖诱导的EMT相关分子的这些变化,包括E-钙粘蛋白表达下调,α-SMA和Vimentin表达上调,都被TUDCA治疗挽救(图3H-J)。与体内观察一致的是,高糖处理后HK-2细胞的ERS和EMT相关反应也被检测到增加,这些变化可以通过给予TUDCA来挽救(图3K-M)。
抑制ERS降低糖尿病肾病小鼠对铁死亡的易感性
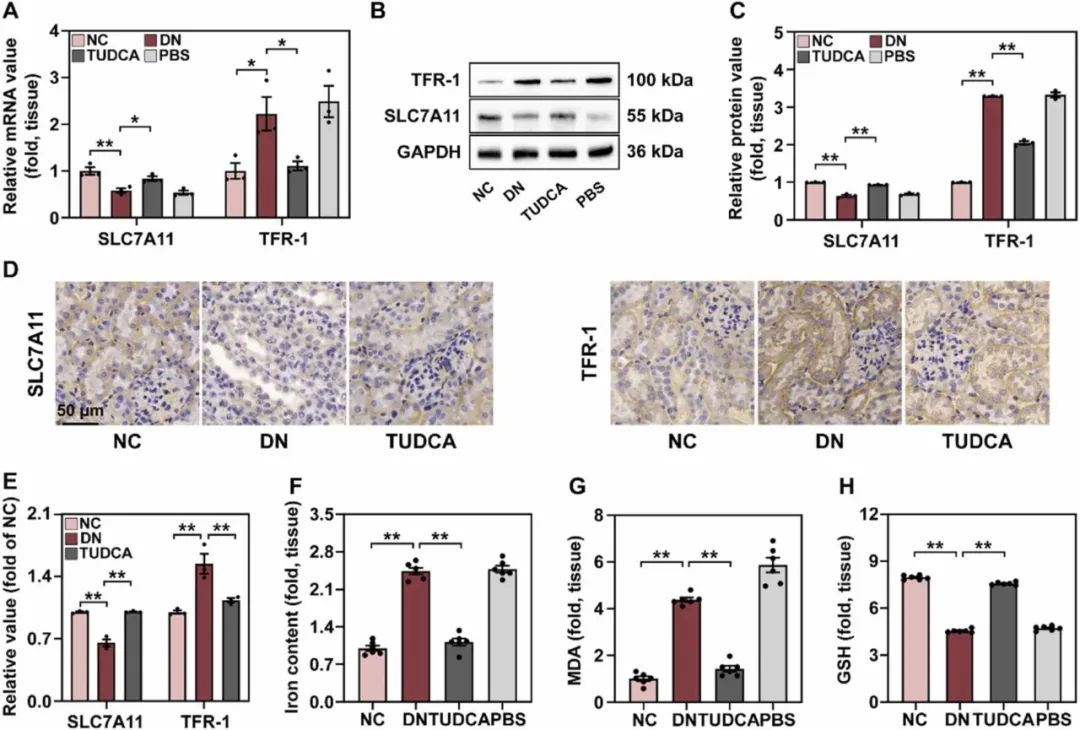
因内质网反应在糖尿病肾病进展过程中铁死亡中的作用仍不清楚。作者检测了肾组织中铁死亡相关分子的表达。与NC组比较,糖尿病肾病组小鼠SLC7A11的mRNA和蛋白表达水平降低,TFR-1表达水平升高,提示糖尿病肾病进展过程中可诱发铁死亡。而这些与铁死亡相关的变化可以通过TUDCA治疗来挽救,这表明高血糖激活的ERS过程中伴随着铁死亡(图4A-C)。免疫组织化学结果显示出与WB和qRT-PCR结果相似的趋势(图4D-E)。此外,与NC组小鼠相比,糖尿病小鼠表现出更高的铁和丙二醛水平以及更低的GSH水平,这些变化可以被TUDCA治疗逆转,表明抑制ERS可以改善糖尿病小鼠的铁超载、脂质过氧化和抗氧化能力下降(图4F-H)。所有这些结果表明,TUDCA治疗可通过抑制ERS反应来减轻糖尿病肾病小鼠的铁死亡。
ERS和铁死亡在高糖处理的HK-2细胞中的相互作用
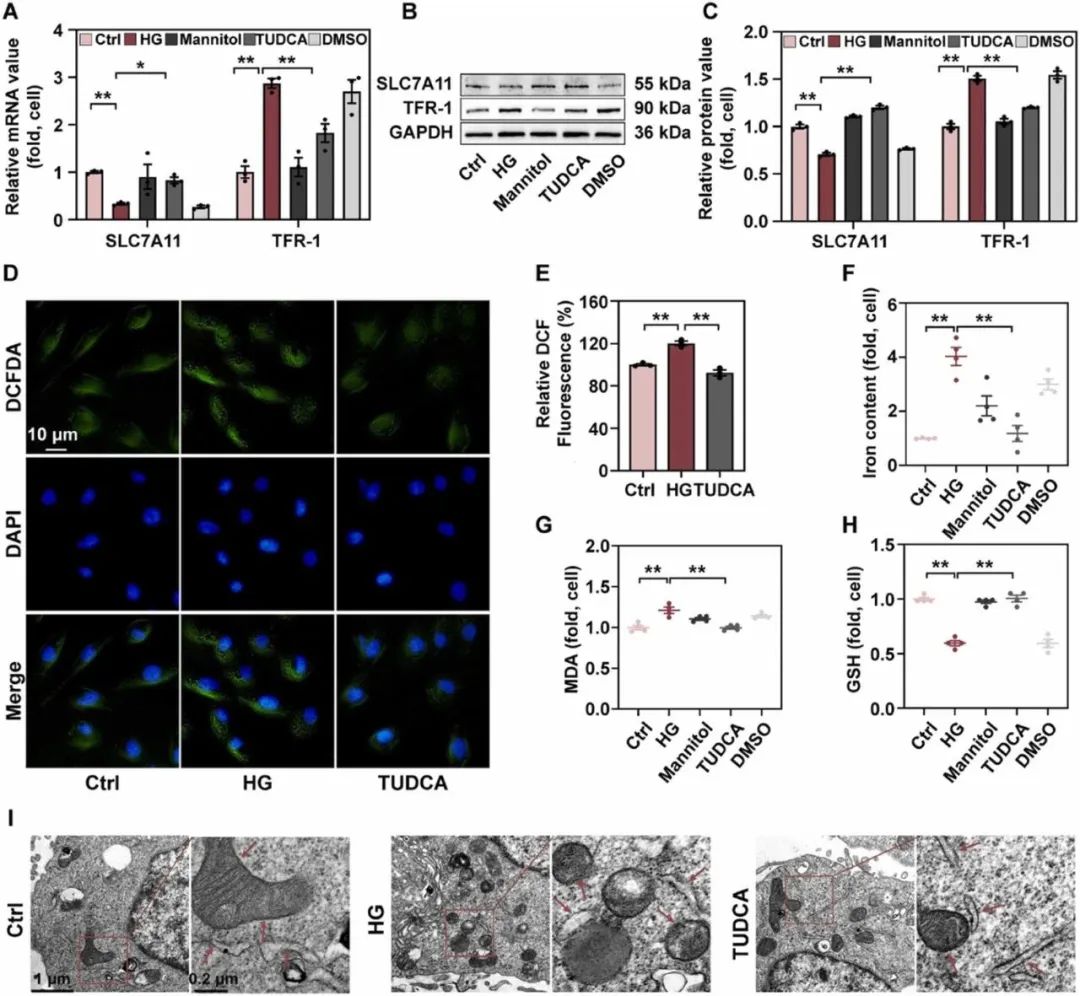
在HK-2细胞中,作者进一步研究了ERS与高糖引起的EMT过程中铁死亡的关系。结果显示,高糖培养的细胞SLC7A11的表达低于NC组,TFR-1的表达高于NC组(图5A-C)。在高糖处理的细胞中观察到比在NC细胞中ROS指标荧光染色更强(图5D)。此外,在高糖处理的细胞中检测到铁死亡特征性的铁和丙二醛的产生增加、GSH浓度的降低(图5E-G)。用透射电子显微镜观察线粒体形态的变化。与NC相比,高糖处理组表现出更多的空泡变性和线粒体脊溶解(图5I)。铁死亡相关的改变通过TUDCA治疗得以缓解(图5A-I)。结果表明,抑制ERS改善高糖培养的HK-2细胞中铁死亡的发生。
高糖上调ERS的XBP1-Hrd途径
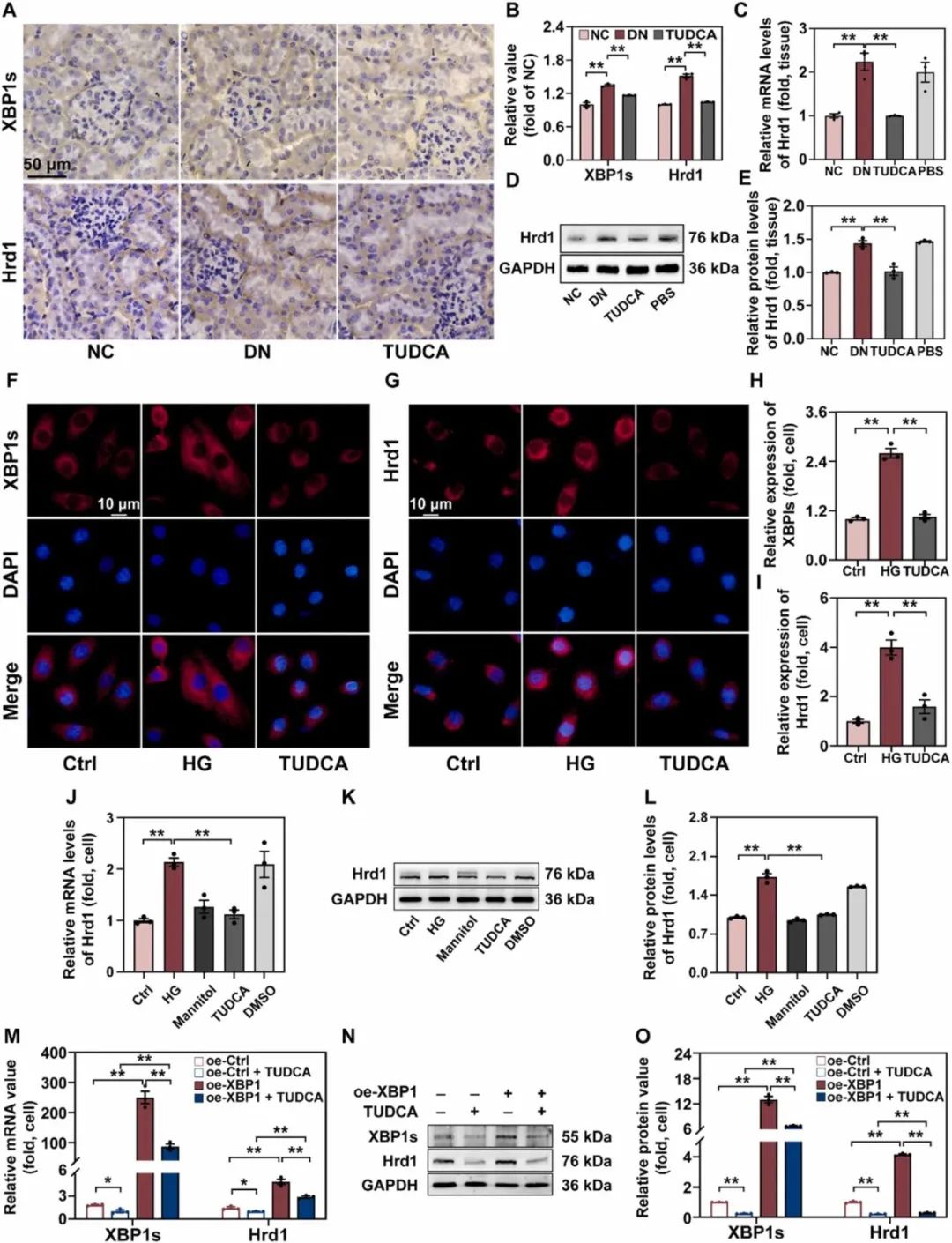
发生ERS时,XBP1 mRNA被剪接后产生XBP1s,进而促进Hrd1的转录。为了高糖时XBP1-Hrd1途径是否被激活,免疫组织化学方法检测糖尿病小鼠组织中Hrd1、XBP1表达。结果表明,糖尿病肾病小鼠中XBP1s和Hrd1表达显著上调,TUDCA可逆转这种变化(图6A-B)。作者评估了ERS时是否触发了糖尿病小鼠的Hrd1的表达上调。与NC相比,糖尿病肾病小鼠Hrd1在mRNA和蛋白水平显著上调,TUDCA治疗可缓解这一变化(图6C-E)。免疫荧光法检测不同处理对HK-2细胞XBP1s和Hrd1表达的影响。高糖培养的细胞XBP1s和Hrd1荧光表达比NC更强,而TUDCA处理的细胞XBP1s和Hrd1的免疫荧光强度比高糖处理的细胞弱(图6f-I)。在高糖暴露的HK-2细胞中也观察到Hrd1mRNA和蛋白的高表达,这些变化可以通过TUDCA治疗来逆转(图6J-L)。结果表明,XBP1和Hrd1的表达水平在糖尿病肾病时随ERS的反应而上调。为了进一步证实Hrd1是XBP1在高糖条件下的下游分子,作者构建了XBP1过表达载体。在高糖和TUDCA处理条件下,XBP1的过表达诱导Hrd1mRNA和蛋白表达增加(图6M-P)。以上数据表明,ERS时的XBP1-Hrd1途径在高糖环境中被激活。
Nrf2基因敲除通过铁死亡增强细胞对EMT的敏感性
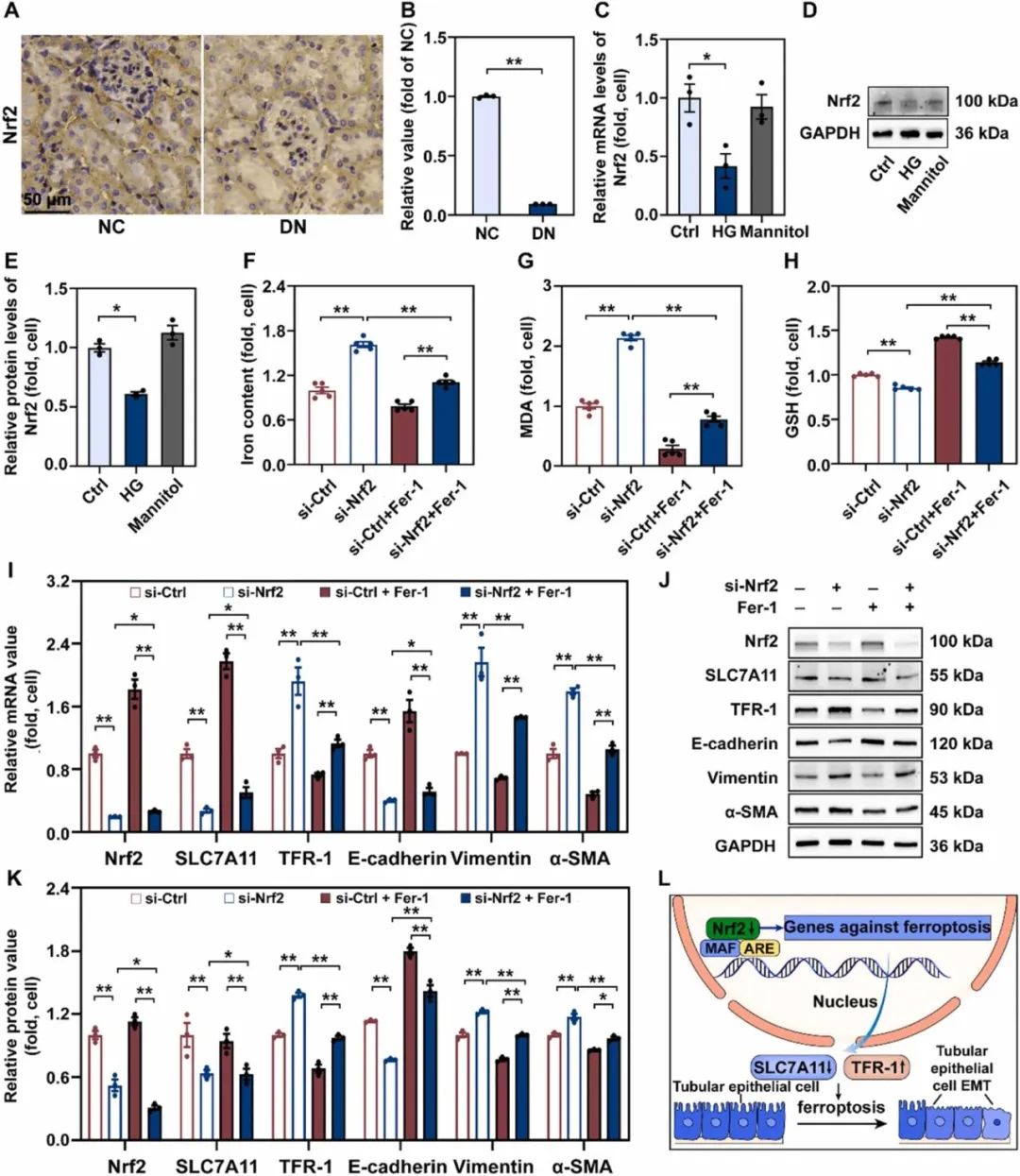
氧化应激是糖尿病肾病EMT进展的主要原因,且Nrf2在氧化应激中起重要作用。免疫组织化学显示,与对照组相比,糖尿病肾病组Nrf2的表达减少(图7A-B)。免疫荧光法检测HK-2细胞中Nrf2的表达水平。显示高糖组的荧光强度弱于对照组。QRT-PCR和WB分析也检测到在高糖培养的HK-2细胞中Nrf2低表达(图7C-E)。为了进一步研究Nrf2在铁死亡和EMT进展中的作用,作者在HK-2细胞中敲除了Nrf2基因。在高糖条件下,Nrf2沉默后,铁和丙二醛水平升高,GSH水平下降。同时这些由Nrf2沉默增强的铁死亡的变化可通过添加Fer-1部分缓解(图7F-H)。进一步检测Fer-1治疗前后Nrf2沉默对铁死亡和EMT相关分子的影响,以探讨Nrf2介导的EMT进程调节是否与铁死亡有关。数据表明,在高糖条件下或在Fer-1处理下,Nrf2沉默降低了SLC7A11和E-cadherin的mRNA水平,而增加了TfR-1、Vimentin和α-SMA的mRNA表达。有趣的是,这些由Nrf2沉默引起的EMT相关的E-钙粘蛋白、Vimentin和α-SMA表达的变化被Fer-1治疗挽救,表明Nrf2沉默通过铁死亡促进了EMT的进展(图7I)。WB结果显示出与qRT-PCR结果相似的趋势(图7J-K)。综上结果表明,HK-2细胞中Nrf2的沉默通过铁死亡增强了细胞对EMT的敏感性(图7L)。
NRF2基因敲除通过铁死亡增强细胞对EMT的敏感性
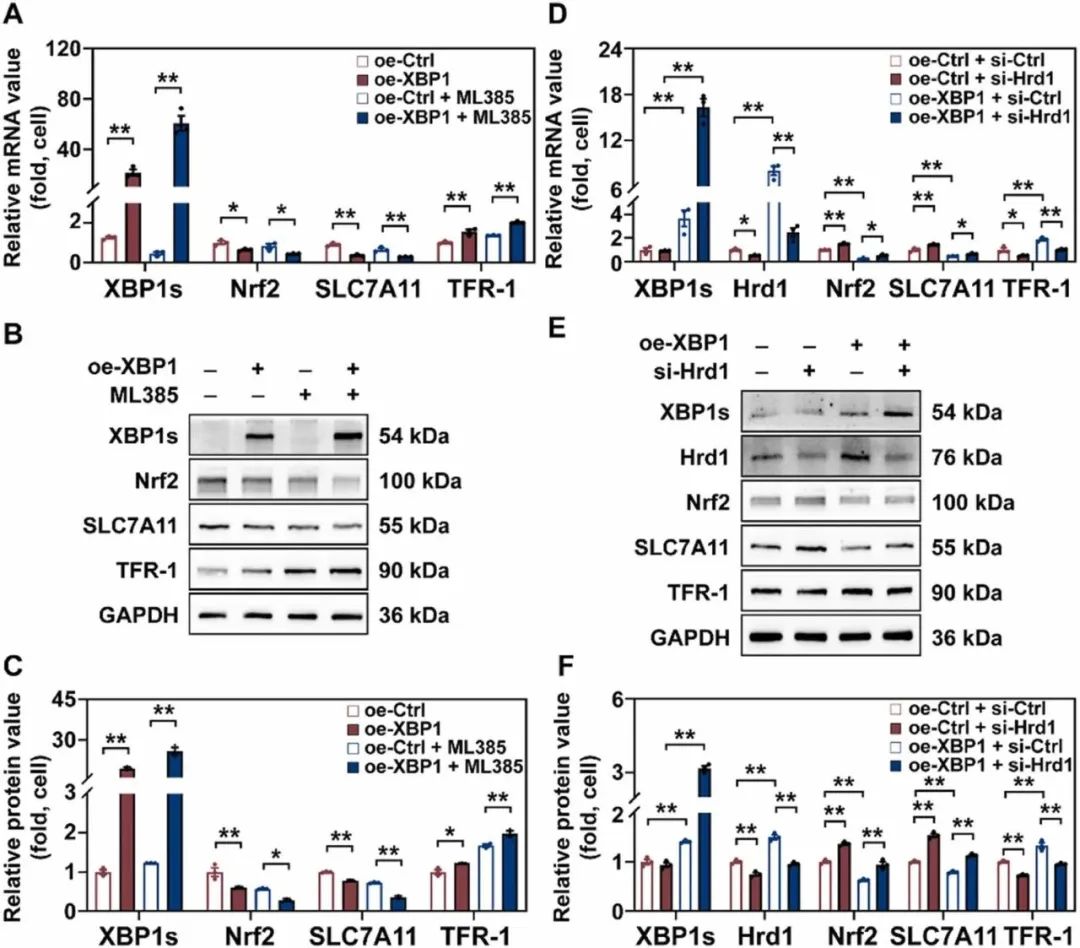
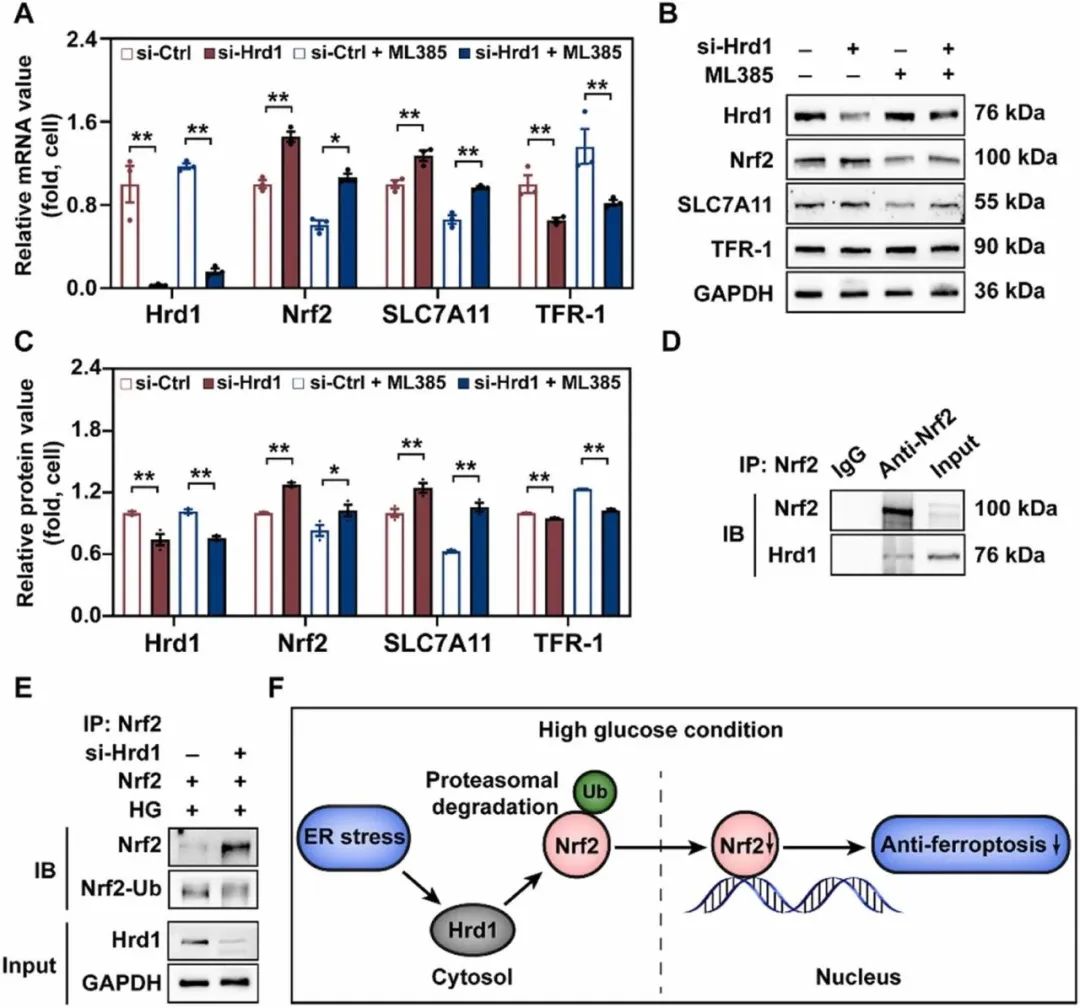
进一步探讨XBP1-Hrd1通路与Nrf2在高糖条件下对铁死亡的保护作用之间的关系。ML385是Nrf2的特异性抑制剂,可以抑制Nrf2的转录活性。如图8A所示,在使用或不使用ML385(10μM)治疗的情况下,XBP1的过表达改变了与铁死亡相关的NRF2和NRF2靶基因的表达。在高糖培养的HK2细胞中,XBP1过表达进一步促进了药物抑制Nrf2引起的SLC7A11基因表达水平的降低和TFR-1基因表达水平的升高。免疫印迹结果与qRT-PCR结果一致(图8B-C)。因此,这些数据表明,在高糖环境下,XBP1和Nrf2的表达呈负相关。随后进行了其他实验,以证实XBP1介导的Nrf2下调依赖于Hrd1。XBP1过表达可增加Hrd1和TFR-1mRNA的表达,而降低Nrf2和SLC7A11mRNA的表达。然而,通过转染si-Hrd1(图8D),Nrf2和参与XBP1过表达诱导的铁死亡相关的Nrf2靶向分子的mRNA表达的变化被有效地挽救。免疫印迹分析显示出与qRT-PCR结果相似的趋势(图8E-F)。这些结果表明,XBP1可能通过Hrd1下调高糖条件下HK-2细胞中Nrf2相关的铁死亡。
Hrd1通过泛素化Nrf2调节铁死亡
ERS的XBP1-Hrd1途径被激活,XBP1抑制Nrf2在高糖条件下对铁死亡的保护作用。作者进一步探讨了XBP1靶基因Hrd1与Nrf2通路的关系。在高糖条件下,转染si-Hrd1基因的细胞Nrf2基因表达上调。此外,参与铁死亡的Nrf2靶向分子的表达也发生了相应的变化,其中包括SLC7A11的上调和TFR-1的下调,这些变化可被ML385逆转。(图9A)。QRT-PCR结果进一步得到WB的证实(图9B-C)。这些结果表明,在高糖条件下,Hrd1负性调节Nrf2。由于Hrd1是内质网中的E3-泛素连接酶,泛素化内质网中积累的错误折叠蛋白,作者评估了Hrd1是否会在高糖处理后泛素化HK-2细胞中的Nrf2。Co-IP实验观察Hrd1与Nrf2在HK-2细胞中的相互作用,发现在高糖环境下Hrd1和Nrf2共存于HK-2细胞中(图9D)。另外,将si-Hrd1基因转染高糖培养的HK-2细胞,检测Nrf2的泛素化水平。与阴性对照siRNA转基因细胞相比,Hrd1沉默增加了Nrf2蛋白的表达,降低了Nrf2泛素化水平(图9e)。因此,这些结果表明,Hrd1,一种由ERS激活的E3-泛素连接酶,泛素化Nrf2,以抑制Nrf2在高糖条件下对铁死亡的保护作用(图9F)。
研究结论
铁死亡参与了糖尿病肾病的EMT进展,且ERS是铁死亡的触发因素,与暴露于高血糖引起的EMT密切相关。ERS可通过XBP1-Hrd1-Nrf2途径在高糖处理后的HK-2细胞中触发铁死亡相关的EMT。
原文出处:
Liu Z, Nan P, Gong Y, Tian L, Zheng Y, Wu Z. Endoplasmic reticulum stress-triggered ferroptosis via the XBP1-Hrd1-Nrf2 pathway induces EMT progression in diabetic nephropathy. Biomed Pharmacother.2023Aug;164:114897.doi:10.1016/j.biopha.2023.114897. Epub 2023 May 22. PMID: 37224754
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#糖尿病肾病# #内质网应激# #铁死亡#
21