引用本文
周昌明,王泽洲,郑 莹. 2023年美国癌症数据解读及对中国癌症防治的启示[J]. 中国癌症杂志, 2023, 33 (2): 117-125.
基金项目:上海市老龄化和妇儿健康研究专项(2020YJZX0206);中国癌症基金会科研项目(NH2018001)。
第一作者:周昌明(ORCID: 0000-0001-7863-428X),博士。
通信作者:郑 莹(ORCID: 0000-0002-6408-8510),主任医师,复旦大学附属肿瘤医院肿瘤预防部主任。
通信作者简介
郑莹,复旦大学附属肿瘤医院肿瘤预防部主任,主任医师,教授,硕士研究生导师,毕业于上海医科大学,医学硕士。长期从事肿瘤预防控制工作,涵盖肿瘤登记和监测、常见肿瘤社区防治干预、肿瘤筛查和早发现及肿瘤防治的健康教育和科普。开展肿瘤病因和预后研究,建立起了以人群为基础的乳腺癌患者队列和大肠癌筛查人群队列。指导健康人和癌症患者建立健康的生活方式,执笔的《中国乳腺癌患者生活方式指南》是我国第一个癌症患者预防指南。曾经担任上海市重点公共卫生项目《社区居民大肠癌筛查项目》的技术负责人,组织编写和发布上海市抗癌协会《居民常见恶性肿瘤筛查和预防推荐》,为医疗机构和个人的癌症早发现和筛查提供指导。共发表学术论文100余篇,其中第一作者或通讯作者的文章90余篇,主编和参编20余部专著,获中华预防医学科技奖2项,上海市科技进步奖1项,上海医学科技奖1项,上海抗癌科技奖1项。主要学术兼职:上海市抗癌协会常务理事,上海市抗癌协会癌症预防与筛查专业委员会主任委员,中国抗癌协会乳腺癌专业委员会康复学组组长,中国临床肿瘤学会(CSCO)肿瘤大数据专家委员会常务委员,中国抗癌协会多原发和不明原因肿瘤专业委员会常务委员,中国抗癌协会乳腺癌专委会、科普专委会、肿瘤流行病学专委会、筛查和早诊早治专委会委员,中国控制吸烟协会控烟与肺癌防治专业委员会常务委员。
作者解读
2023年美国癌症数据解读及对中国癌症防治的启示
周昌明1,2,王泽洲1,2,郑 莹1,2
1.复旦大学附属肿瘤医院肿瘤预防部,复旦大学上海医学院肿瘤学系,上海 200032;
2.上海肿瘤疾病人工智能工程技术研究中心,上海 200032
[摘要] 美国癌症协会发表的美国癌症统计数据预计2023年美国全年新发恶性肿瘤病例1 958 310例,死亡609 820例。美国的癌症死亡率在1991年达到峰值后持续加速下降,治疗的进步使得患者生存得到改善,减少吸烟人数、普及癌症筛查是其主要原因;2020年COVID-19大流行造成350 831人死亡,位列2020年死因第3位,同时造成包括癌症在内的其他多种死因显著增加,但疫情对癌症死亡的影响尚未被纳入评估。通过对2020年GLOBOCAN数据库中中国和美国数据进行对比分析发现,尽管中美癌症发病和死亡存在较大差异,但是美国癌症防治的经验值得中国借鉴,我们应努力提高肿瘤诊治规范化程度、提升医疗服务资源可及性以提升患者生存率,优化筛查模式、提升筛查效率,癌症筛查覆盖率,同时进一步提高HPV疫苗接种率将有效地降低癌症死亡。
[关键词] 癌症; 统计;死亡率;筛查;HPV疫苗
[Abstract] In the year 2023, 1 958 310 new cancer cases and 609 820 cancer deaths are projected to occur in the United States, estimated by Cancer Statistics, published by American Cancer Society. An accelerated decline in mortality rate of cancer continues since it reached the peak in 1991. The treatment advance brought survival benefit to patients which mainly contribute to the decline along with tobacco control and screening. COVID-19 pandemic caused 350 831 mortality and ranked 3rd in cause of death in 2020, and the mortality had a significant increase in multiple causes of death including cancer. By comparing the data of China and the United States released by GLOBOCAN database in 2020, it is found that, although the influence of the pandemic on cancer has not been evaluated. Although the incidence and mortality of cancer differ between US and China, the experiences are worth learning. Improving the standardization of diagnosis and treatment, enhancing the accessibility of cancer health care, upgrading the coverage of screening and increasing the human papillomavirus (HPV) vaccination rate are proven to be effective ways to reduce the mortality of cancer..
[Key words] Cancer; Statistics; Mortality rate; Screening; HPV vaccination
自1951年起,美国癌症协会(American Cancer Society,ACS)每年发表全美癌症统计数据,系统地展示美国癌症的发病率、死亡率及其变化趋势并探索其成因。2023年1月,其在CA: A Cancer Journal for Clinicians上发表了2023年美国癌症统计数据[1]。
美国和中国在癌症发病和死亡方面本身存在较大差异,比如瘤谱不同、医疗卫生服务的资源和防控策略也有较大差异。同时美国作为一个多移民、多族裔国家,有其独有的人群特征。美国在癌症方面的防治措施是持续有效的,本次发表的统计数据背后所反映的防治成效和经验,值得中国借鉴和学习。
1
从美国癌症数据看癌症防控效果
2023年,美国全年预计新发癌症病例1 958 310例,此外,还将有55 720例女性乳腺导管原位癌和89 070例皮肤原位黑色素瘤新发病例。同时,2023年,预计美国将有609 820人死于癌症,其中导致男性死亡人数最多的前三位肿瘤分别为肺癌、前列腺癌和结直肠癌,而在女性中则是肺癌、乳腺癌和结直肠癌。美国男性和女性一生中被诊断为浸润性癌的累计概率分别为40.9%和39.1%。男性前列腺癌、肺癌、支气管癌和结直肠癌占男性所有发病病例的48.0%,女性乳腺癌、肺癌和结直肠癌占所有新诊断癌症的52.0%。
需要注意的是,该报告记述的是2023年美国癌症数据的预测结果,实际发病和死亡数据由于数据收集、汇编、质控等原因,往往有2~4年的滞后。该报告中2023年的数据,实际上是基于高质量的历史登记数据(2005—2019年发病数据和2006—2020年死亡数据),通过模型计算得到的预测数据。
1.1 美国癌症死亡率持续加速下降
癌症的死亡率是反映癌症危害程度最为综合的指标。在20世纪的大部分时间里,美国癌症的死亡率都是在上升的,由于烟草流行导致的肺癌死亡人数的迅速增加,美国肺癌死亡中,81%是由吸烟直接导致的[2]。目前肺癌仍是美国导致死亡的头号原因,其每年导致的死亡人数是结直肠癌(第二大癌症死亡)的近2.5倍。控烟被证明是降低癌症发病率的有效方法[3]。通过禁烟运动,美国的吸烟率持续下降,2020年美国成年人吸烟率已经降至12.5%[4],与1965年的吸烟率水平(43.0%)相比下降了超过70.0%[5],从而使得以肺癌为主的恶性肿瘤发病率和死亡率持续下降。
美国的癌症死亡率在1991年达到峰值(215.1/10万),之后持续下降,整体下降到2020年的143.8/10万,下降幅度高达33%。同时也意味着自1991年来,癌症死亡人数比死亡率保持峰值时减少382.08万人(男性258.28万人,女性123.80万人)。减少吸烟人数、普及癌症筛查及治疗方法的进步是主要的原因。
美国癌症死亡率不仅在下降,下降速率还在不断加快。在20世纪90年代其死亡率以每年1.0%的速率下降,到21世纪初,下降速率为每年1.5%,而到了2015—2020年,下降速率增长到每年2.0%。这其中,肺癌作为死亡率最高的恶性肿瘤,其死亡率的快速下降对整体死亡率下降作出了最大的贡献。1995—2005年,美国肺癌死亡率的下降速率为每年0.9%,而2014—2020年,死亡率下降速率高达每年4.8%。
美国女性乳腺癌死亡率在1989年达到峰值,此后通过提高认知和乳腺X线检查进行早期诊断,再加上治疗的改进,至今死亡率已经下降了43.0%。近年来,美国乳腺癌死亡率的下降速率有所放缓,下降速率从20世纪90年代和21世纪初的每年2.0%~3.0%放缓至2011—2020年每年的1.0%,这可能反映了近年来乳腺癌发病率稳定轻微上升,而乳腺X线检查的筛查覆盖率却停滞不前。
美国前列腺癌的死亡率从1993年的峰值下降了53.0%,其死亡率下降速率从1994—2013年的每年下降3.0%~4.0%,降低至2013—2020年每年的0.6%。前列腺癌的发病率趋势则相对变化较大。2008年,美国预防服务工作组(US Preventive Services Task Force,USPSTF)建议对75岁及以上的男性,2012年对所有男性停止前列腺特异性抗原(prostate-specific antigen,PSA)筛查后,前列腺癌的发病率从2007—2014年下降了约40.0%,原因是通过PSA检测诊断的临床局限期肿瘤发病率下降。然而,从2014年到2019年,前列腺癌的发病率每年上升3.0%且晚期患者数量逐渐增多。
美国结直肠癌防控成效一直为全球认可。自2012年以来,结直肠癌总体发病率每年下降1.4%~1.5%。然而,这些发病率的下降主要是归因于在老年人群开展的筛查导致的癌症发病率下降,但是也掩盖了年轻结直肠癌的上升趋势。2014—2016年美国40~49岁人群的结直肠癌发病率相比2000—2002年增长了15.0%,目前,50岁以下人群的结直肠癌患者占所有结直肠癌患者的10.5%。美国50岁及以上人群的结直肠癌死亡率每年下降2.0%,而50岁以下人群的死亡率每年增长近2.0%。
1.2 美国患者生存率在半个世纪内提升近40%
与19世纪70年代诊断的癌症患者相比, 2012—2018年诊断患者的5年相对生存率已经从49.0%已经上升至68.0%。在1970年的基础上增加了近四成。目前美国生存率最高的是甲状腺癌(98.0%)、前列腺癌(97.0%)、睾丸癌(95.0%)和黑色素瘤(94.0%),最低的是胰腺癌(12.0%)、肝癌和食管癌(21.0%)。
在生存率改善的过程中起到最大作用的是治疗技术的进步,因此延长了患者的生存期,导致死亡率迅速下降。慢性粒细胞白血病患者的5年相对生存率从1970年诊断时的22.0%提升至2012—2018年诊断时的70.0%,大多数使用酪氨酸激酶抑制剂的患者甚至可以活到正常的预期寿命[6]。近年来,程序性死亡[蛋白]-1(programmed death-1,PD-1)抗体、程序性死亡[蛋白]配体-1(programmed death ligand-1,PD-L1)抗体、细胞毒性T淋巴细胞相关抗原4 (cytotoxic T lymphocyte associated antigen-4,CTLA-4)抗体以及BRAF和MEK抑制剂的使用也彻底改变了转移性黑色素瘤的治疗局面,使远处转移的黑色素瘤的3年相对生存率近乎翻番,从2004—2006年的20.6%提升至2016—2018的39.3%[7]。免疫治疗在非小细胞肺癌中的应用让更多晚期患者得到生存上的获益,也让接受新辅助治疗的患者更多地获得手术机会和生存获益。全阶段肺癌患者3年相对生存率从2004—2006年的22%上升至2016—2018年的33.0%,其中非小细胞肺癌患者(从25.0%提升至38.0%)的获益远大于小细胞肺癌(9.0%提升至12.0%)。当然,筛查在降低死亡率的同时也会通过领先时间偏倚(lead-time bias)和发现惰性肿瘤,从而影响乳腺癌、前列腺癌等患者的生存情况。
1.3 额外死亡增加数据还未真正体现COVID-19疫情对癌症的影响
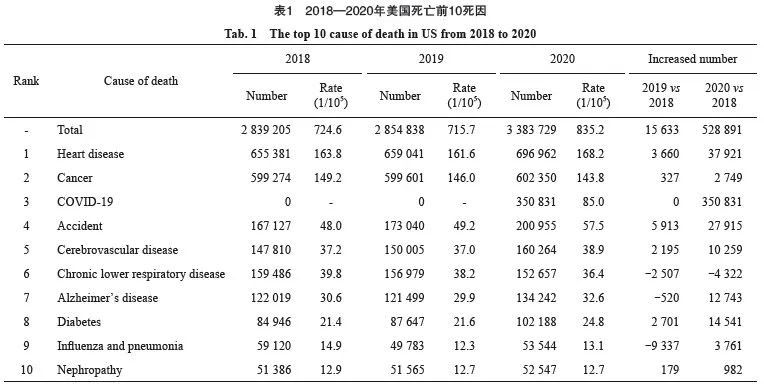
在本次报告中,首次公布了美国2020年前10位的主要死因。2020年,全美死亡人数3 383 729人,比2019年增加528 891例;2019年较2018年增量15 633人[1],2019—2020年的增幅较2018—2019年新超33倍。COVID-19在2020年导致了350 831人死亡,占全死因的10.0%,位列死因的第3位,也占美国2020较2019年死亡增量的2/3。同时,2019—2020年新增的死亡人数集中在心脏疾病、癌症、事故、脑血管疾病、阿尔兹海默病等,与2018—2019相比,均有显著的上升。以癌症为例,2020年美国癌症死亡人数为602 350人,位列死因第2位,占全死因的18.0%。2020癌症死亡比2019年增加2 749例,2019年较2018年癌症死亡新增的327例,前者的增幅是后者增幅的8.4倍(表1)。这一不同寻常的增长幅度无法用人口增长或老龄化来解释,间接反映了COVID-19除直接导致患者死亡外,额外提升了癌症患者死亡的风险。这类风险的提升可能是由于疫情导致癌症诊断和治疗延误所致[8]。但是,该研究也提到,并未将COVID-19大流行造成的就诊延误所导致的影响纳入模型计算。因此对2023年发病和死亡的估计,可能并不能真正地反映出COVID-19的影响。
2
中美癌症数据差异对中国防治策略的启示
2.1 推广筛查、规范治疗,使更多患者获益
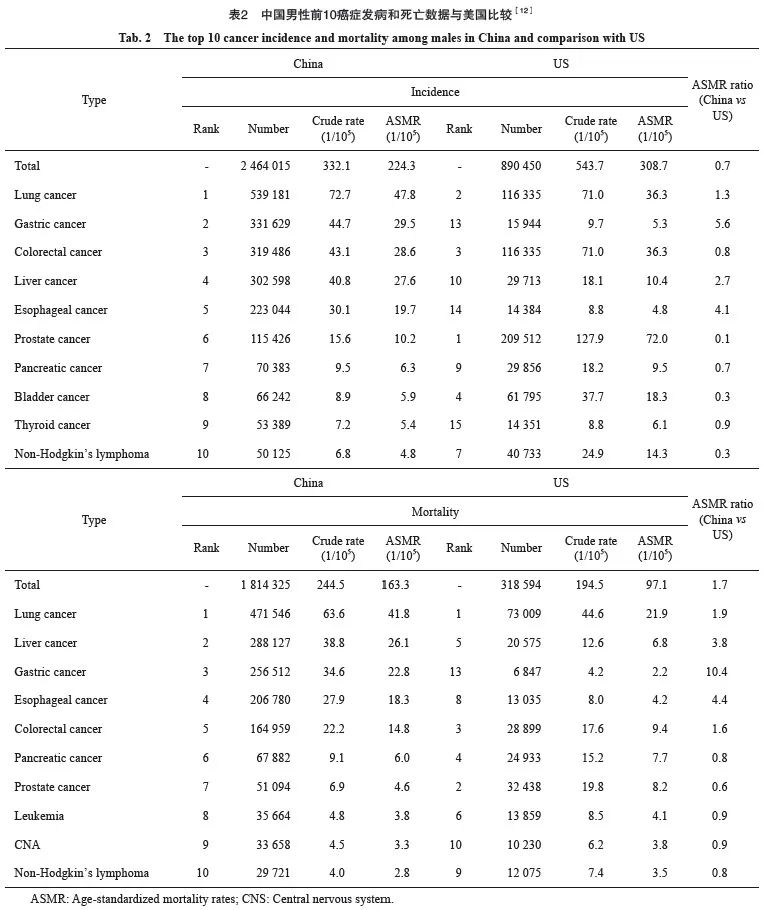
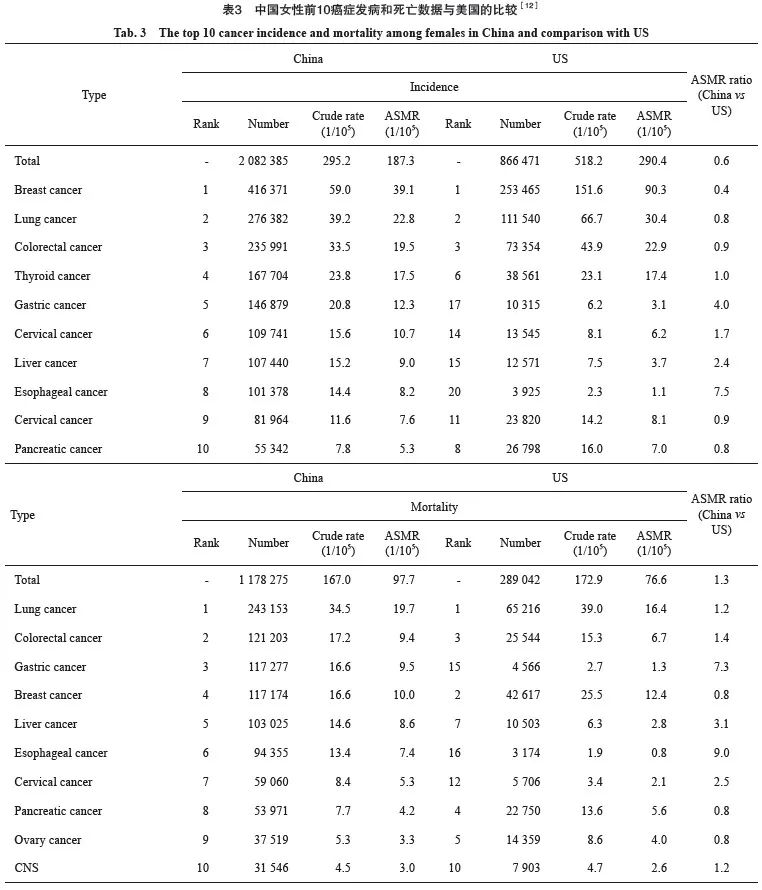
中国地域广阔,人口众多,医疗资源分布不均衡。经济发达地区的医疗卫生投入较多、医院诊疗水平较高、人群恶性肿瘤筛查普及率较高,这一系列因素能够提高肿瘤早诊早治率、改善肿瘤预后、降低肿瘤死亡率[9]。以肺癌为例,回顾性数据发现即使在同一省内,治疗也存在较大的异质性[10]。全面提高肿瘤诊治的规范化程度,缩小地区间肿瘤诊治水平的差异,同时提升医疗服务资源的可及性有助于提高患者的生存率。《健康中国行动(2019—2030年)》将中国2030年总体癌症5年生存率的目标设定在不低于46.6%[11],乍看这一目标甚至低于美国1970—1979年的癌症生存情况,然而在考虑整体5年生存率的同时,必须注意中美之间本身瘤谱存在显著差异。通过对2020年GLOBOCAN数据库中的中国和美国数据[12]进行对比分析发现,除肺癌外,美国乳腺癌、前列腺癌、恶性黑色素瘤的发病率远高于中国,而胃癌、肝癌、食管癌等美国发病率较低预后又较差的恶性肿瘤在中国又是高发瘤种,中国男性胃癌的发病率和死亡率分别是美国的5.6倍和10.4倍,在女性中分别是4.0倍和7.3倍;中国男性食管癌发病率和死亡率分别是美国的4.1倍和4.4倍,女性中分别是7.5倍和9.0倍(表2、3),因此加强消化系统恶性肿瘤的预防和筛查刻不容缓。中国恶性肿瘤患者的生存率也有了长足的进步,整体年龄标化5年相对生存率从2003—2005年的30.9%提升至2012—2015年的40.5%[13]。近年来靶向和免疫治疗给患者生存带来的获益让患者和医护人员倍感振奋,但是需要看到的是中国乳腺癌、前列腺癌患者的生存率与美国相比仍存在较大差距,中国胃癌患者的生存率仍远低于日本[14],这些差距的主要原因在于筛查覆盖率的不同。
2.2 筛查应以持续提高覆盖率为主
尽管对于前列腺癌、乳腺癌、甲状腺癌等相对预后较好的恶性肿瘤的筛查始终存在过度诊断的争议,但不可否认的事实是,中国恶性肿瘤的筛查覆盖率仍不尽如人意。中国仅1/3的初诊前列腺癌患者属于临床局限性前列腺癌,初诊时多数患者已处于中晚期[15];肝癌初筛的年度覆盖率在全国35~74岁人群中约为0.09%[16]。即使在上海这样全国卫生资源最为集中的区域,乳腺癌和前列腺癌的诊断时Ⅰ期的比例也远不及美国的平均水平[17]。同时中国还面对人员、设备等筛查资源匮乏的问题:目前中国人缺乏专业人员和设备,全国病理医师缺口达9万人,全国仅有2.5万台医用内镜设备,《2020中国消化内镜诊疗技术调查报告》显示,每百万人口拥有能开展消化内镜的医师仅28.12人,为日本的1/7。诸如美国前列腺癌筛查过度诊断的问题,可能在未来覆盖率达到一定程度后开始显现。因此提高肿瘤筛查覆盖率,仍是目前的重点工作。同时需要注意的是,由于胃癌、食管癌在美国并非高负担病种,上消化道肿瘤的筛查并未被USPSTF列为适宜筛查的病种。通过对2020年GLOBOCAN数据库中中国和美国数据进行对比分析发现,中国上消化系统肿瘤负担远高于美国,2020年中国人群无论在发病率还是死亡率方面,中国胃癌和食管癌的人数和率均远高于美国,提示中国针对上消化道肿瘤的筛查刻不容缓(表2、3)。当然,借助流行病学证据和模型进一步优化接受筛查的模式,可以进一步提升筛查效率和成本效果比。
2.3 警惕中国结直肠癌双重负担
全球50岁以下人群结直肠癌的发病率在上升[18],中国也面临年轻结直肠癌发病率上升的问题,中国结直肠癌的发病率和死亡率仍均保持上升趋势[19],但是负担最重的人群依旧为中老年人群。美国50岁以上人群死亡率的下降得益于美国肠癌的筛查,美国50岁以上人群做过肠镜检查人群的比例已经从2000年的20%提升至2018年的61%,不仅使得肠癌死亡率下降,也进一步使发病率下降[20],但50岁以下的人群并不在筛查的范围之内。尽管45~49岁之间的人群开展筛查的成本效果比不如50岁以上人群,但该措施仍能获得中等的净获益。因此2021年,USPSTF将推荐肠癌筛查的年龄提前至45岁[21]。
相比而言,中国在2012—2015年开展的多中心结直肠癌筛查项目中,高危人群中,肠镜的依从率也仅为14%[22]。对于中国众多的人口和相对有限和不平衡的卫生资源而言,全人口的肠镜筛查是不切实际的,建立精确的风险预测模型,准确识别筛查中受益最大的高危人群,是中国优化肠癌筛查的重要任务[23]。采用模型确立获益更高的人群、提高内镜服务供给、提升民众的防治意识、改善医疗保健的立法、推出创新的支付方式以及采用创新的无创筛查方法,都是进一步提升结直肠癌筛查依从性的手段,由此可望逆转中国结直肠癌发病和死亡上升趋势,挽救人群生命。
2.4 子宫颈癌防治需重视疫苗策略
得益于广泛的筛查,美国子宫颈癌的发病率自20世纪70年代中期起下降超过了50%。尽管在2015—2019年发病率仍保持稳定,但是其发病趋势在不同年龄、族群中有所不同。在大部分年龄段和族裔的人群中,均稳定保持下降,但是在年轻拉丁裔女性中每年却上升2%。至少有一部分是由于美国的移民状况所导致的。自美国针对HPV-16和HPV-18的疫苗上市以来,第一批接种的青少年已经进入了性活跃期。在20~24岁女性中,浸润性子宫颈癌的发病率下降速率在1998—2012年为每年3.0%,而2012—2019年的下降速率每年达11.4%,提示疫苗接种对进一步消除子宫颈癌起到积极的作用。同时有研究[24]发现,与2003年相比,2018年14~24岁性活跃期的女性HPV-16/HPV-18的感染率在接种者中下降了90%,在未接种者中下降了74%,也显示出了广泛接种疫苗所产生的惊人的群体免疫效果。尽管与其他收入更高的国家相比,美国女性全程接种3针HPV疫苗的比例已经有所落后,但是2021年美国79%的女性青少年至少接种过一剂HPV疫苗[25]。美国子宫颈癌的防治经验展现了疫苗接种的巨大作用,在青年女性中带来了每年两位数的下降速率,同时也显示出了疫苗的外部性作用。
与此相比,2016年,中国15~44岁女性中有2.7万人罹患子宫颈癌,并有超过4 600人因子宫颈癌死亡。更令人担忧的是,2000—2016年中国女性子宫颈癌的发病率和死亡率正以每年8.5%和5.4%的速率快速上升[19]。HPV疫苗于2016年正式进入中国市场,但是据研究[26]估计,2018—2020年中国9~45岁女性的HPV接种率仅为2.24%,在北京和上海等发达城市接种率也不足10.00%。巨大的接种率差异提示中国可能在短期内仍无法逆转子宫颈癌发病和死亡率的上升趋势。世界卫生组织《加速消除子宫颈癌全球战略》指出到2030年需实现以下3项目标:90%的女孩在15岁之前完成HPV疫苗接种;70%的妇女在35岁和45岁之前接受高效检测方法筛查;90%的确诊子宫颈疾病的妇女得到治疗(90%的癌前病变阳性妇女得到治疗,90%的浸润性癌病例得到管理)[27]。2023年1月,国家卫健委等10部门联合印发了《加速消除子宫颈癌行动计划(2023—2030年)》,提出到2025年,试点推广适龄女孩HPV疫苗接种服务[28]。为进一步提高HPV疫苗覆盖率提供了政策保障。目前子宫颈癌是中国女性第6位高发的恶性肿瘤,也是死亡率位居第7位的恶性肿瘤。而美国子宫颈癌相应排位分别为第16和第14位(表3),提示如果目前在中国尽快普及HPV疫苗接种,其覆盖人群在未来的获益将是巨大的。安全性也是民众颇为关心的问题之一,疫苗犹豫(vaccine hesitancy)是增加HPV疫苗覆盖率必须克服的障碍。事实上已经有充分且一致的全球证据表明HPV疫苗总体是安全的,且耐受性良好,局部注射症状是最常见的不良反应,严重的不良反应罕见,也与严重的后遗症无关联[29]。尽早对适龄女性高危型HPV实现首剂的广覆盖,可以使人群在资源有限的情况下实现最大化获益。
3
总结与展望
美国自1991年以来,癌症死亡率的稳步下降使人们对战胜癌症增强了信心,也积累了经验。控烟、筛查和治疗手段的进步是实现这一目标的主要途径[1,30]。中国在汲取国外经验的同时,应结合自身国情,拓展更适合于中国的肿瘤防治道路。肿瘤治疗的进步使更多的患者得到了生存获益,让患者和医护人员都备受鼓舞。肿瘤的预防、筛查服务,更多需要的是全社会多方资源的投入和协调,同时需要加强慢性病流行病学基础设施建设,推动基于人群的预防筛查研究,将证据进行转化,为政策决策提供依据。此外,政策的支持、创新的支付方式等,也都将有助于促进癌症防治策略的进一步落实,最终达到保障人民群众健康、降低癌症死亡率的目标。
利益冲突声明:所有作者均声明不存在利益冲突。
[参考文献]
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言