Cell Res:基因编辑CRISPR能成为新冠病毒利器?
2020-03-03 白露 医药魔方Pro
自新型冠状病毒(SARS-CoV-2)疫情爆发以来,随着专家们的竞相研究,目前已发现有作用的治疗药物包括核苷类似物瑞德西韦(remdesivir)、抗疟疾及自身免疫性疾病药物氯喹(chloroquine)、抗HIV药物洛匹那韦/利托那韦(lopinavir / ritonavir)等,然而这些药物对SARS-CoV-2的作用有限,且是否能有效对抗病毒的不同变体尚未知。 2月18日,来自哈佛医学院
自新型冠状病毒(SARS-CoV-2)疫情爆发以来,随着专家们的竞相研究,目前已发现有作用的治疗药物包括核苷类似物瑞德西韦(remdesivir)、抗疟疾及自身免疫性疾病药物氯喹(chloroquine)、抗HIV药物洛匹那韦/利托那韦(lopinavir / ritonavir)等,然而这些药物对SARS-CoV-2的作用有限,且是否能有效对抗病毒的不同变体尚未知。
2月18日,来自哈佛医学院的研究人员在 Cell Research 上发表的一篇文章介绍了一种基于CRISPR技术来对抗SARS-CoV-2和其他RNA病毒以及这些病毒变体的潜在疗法[1]。

图片来源:Cell Research
研究人员对来自中国、美国和澳大利亚19例患者的SARS-CoV-2 RNA基因组进行了分析,发现这些病毒在序列上存在差异(图a),这些差异主要是单核苷酸变异。文章还展示了导致 SARS-CoV-2中ORF8(与驱动冠状病毒从蝙蝠迁移到人类身上有关)的氨基酸62和84位改变的单核苷酸变异例子(图b)。

图片来源:Cell Research
这些患者样本的数据表明,SARS-CoV-2正积极获得新的突变,可能会使其具有逃避抗病毒药物的能力。这对传统药物和疫苗的开发提出了严峻挑战。其他致命的RNA病毒,如SARS病毒或MERS病毒也面临同样的问题。
CRISPR/Cas13d是一个RNA导向的RNA靶向CRISPR系统。在这里,研究人员建议使用该系统特异性“嚼碎”SARS-CoV-2的RNA基因组,从而限制其再生能力。Cas13d蛋白和包含与病毒RNA基因组特异性互补间隔序列的导向RNAs(gRNAs)被选择用来切割SARS-CoV-2的RNA基因组(图c)。
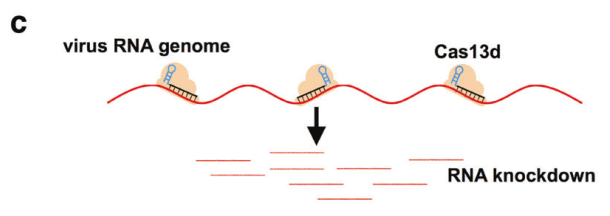
图片来源:Cell Research
为了在功能上破坏病毒,研究人员将特别采用同时靶向病毒ORF1ab和S基因的gRNAs。ORF1ab基因编码ORF1ab多聚蛋白,参与病毒RNA的转录与复制,并具有蛋白酶、甲基转移酶等多个功能;S基因编码冠状病毒的表面糖蛋白,也称为棘突蛋白(Spike Protein),这类蛋白如同皇冠般分布在病毒的包膜上,“冠状病毒”由此得名,它们通过与人体内的ACE2蛋白质结合,直接介导病毒对宿主细胞的感染及融合。这些功能性蛋白质对病毒的感染与复制有着重要作用,单独或同时干扰其中一个或多个蛋白质的功能,抑制其活性,便能阻断病毒感染宿主细胞或在宿主细胞内自我复制的进程,从而起到治疗的效果。
CRISPR/Cas13d系统的一大优点是设计gRNA的灵活性,因为Cas13d的RNA靶向切割活性并不依赖于特定的相邻序列(如DNA编辑效应物Cas9的NGG序列)的存在。这一特性满足了快速开发gRNA以针对可以进化并可能逃避传统药物的不同病毒变体的要求。
研究人员共设计了10 333个gRNA,它们特异性靶向SARS-CoV-2病毒RNA基因组的10个肽编码区,而不影响人类转录组(图d)。

图片来源:Cell Research
腺相关病毒(AAV)具有良好的安全性,可以作为载体将Cas13d效应物传递给SARS-CoV-2感染患者。而Cas13d效应物较小的体积也适合于带有gRNA阵列的“一体化”AAV递送,因为AAV的最大装载容量大约只有4.7KB左右。具体来说,多达3个靶向SARS-CoV-2 RNA基因组不同肽编码区的gRNA可被打包进一个AAV载体(图e),这样能使系统更有效地清除病毒、预防耐药性。
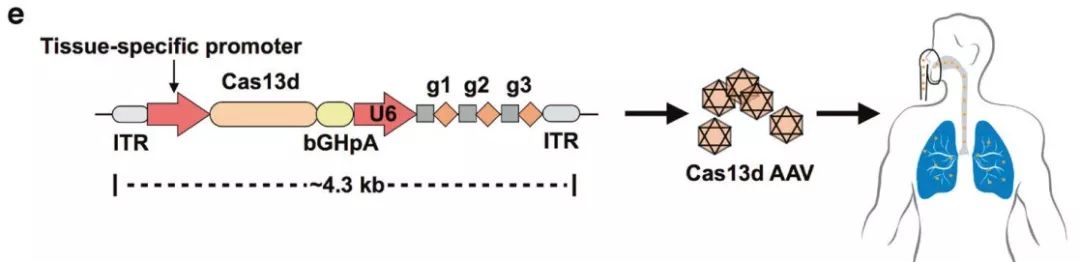 图片来源:Cell Research
图片来源:Cell Research
此外,肺部是SARS-CoV-2感染的主要器官,AAV具有对肺部高度特异性的血清型,因此可用于CRISPR系统的靶向传递。而Cas13d的表达可由组织特异性启动子驱动,实现对感染器官的精确治疗。类似的策略也适用于其他类型的RNA病毒。
综上所述,研究人员提议CRISPR/Cas13d系统可作为一种简单、灵活、快速的治疗和预防RNA病毒感染的潜在方法。不过,在将该系统用于患者治疗之前,需要进一步在动物模型中研究确定该系统清除SARS-CoV-2及其他RNA病毒的安全性和有效性。如果被证明是有效的,这种治疗方法将为全世界的患者提供更多的选择,以对抗那些有可能迅速进化和发展耐药性的威胁生命的病毒。
相关论文:
[1] Tuan M. Nguyen, et al. Virus against virus: a potential treatment for 2019-nCov (SARS-CoV-2) and other RNA viruses. Cell Research (2020). http://sci-hub.tw/10.1038/s41422-020-0290-0
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#CEL#
35
#Cell#
43
#CRISPR#
28
新冠肺炎,疫情何时才能消失
54