ANN ONCOL | TROPHY-U-01研究: sacituzumab govitecan用于铂类化疗和免疫检查点抑制剂后进展的转移性尿路上皮癌患者的安全性和疗效(Ⅱ期开放标签研究)
2024-01-25 daikun MedSci原创 发表于上海
该研究旨在评估 sacituzumab govitecan用于铂类化疗和免疫检查点抑制剂后进展的转移性尿路上皮癌患者的安全性和疗效,支持在铂类化疗和免疫检查点抑制剂治疗后的尿路上皮癌中使用SG。
Sacituzumab govitecan (SG)是一种抗体药物偶联物,包含伊立替康的活性代谢产物SN-38,可用于治疗转移性尿路上皮癌。基于TROPHY-U-01研究队列1的数据,SG在美国获得加速批准,用于治疗铂类化疗和免疫检查点抑制剂治疗后的局部晚期或转移性尿路上皮癌。UGT1A1基因突变与接受伊立替康类药物治疗的毒性增加相关,但UGT1A1状态对SG的毒性和疗效的影响尚不清楚。TROPHY-U-01研究是一项多队列、开放标签的II期注册研究。队列1包括接受铂类化疗和免疫检查点抑制剂治疗后进展的局部晚期或转移性尿路上皮癌患者。该研究报道了TROPHY-U-01研究队列1的更新安全性和疗效结果,以及按UGT1A1状态进行的安全性分析。

方法:TROPHY-U-01是一项国际多中心、开放标签、II期注册研究,包含多个队列,针对不可切除的局部晚期或转移性尿路上皮癌患者。队列1包括铂类化疗和免疫检查点抑制剂治疗后的转移性尿路上皮癌患者。患者接受10mg/kg的SG静脉注射,每21天为一个周期。主要终点为客观缓解率,次要终点包括无进展生存期、总生存期和安全性。
1.人群和基线特征
研究对象为TROPHY-U-01研究队列1中的患者,即接受铂类化疗和免疫检查点抑制剂治疗后的转移性尿路上皮癌患者,共入组113名患者,中位年龄为66岁,78%为男性,ECOG评分为0-1,96%为转移性尿路上皮癌,3%为不可切除的局部晚期尿路上皮癌,66%的患者存在内脏转移。所有患者既往接受铂类化疗,其中79%接受顺铂治疗,21%接受卡铂治疗,99%的患者既往接受免疫检查点抑制剂治疗。
2.疗效分析
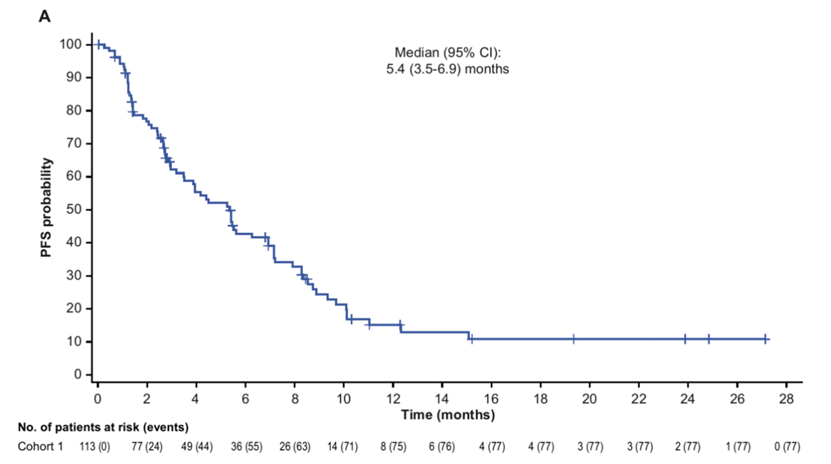
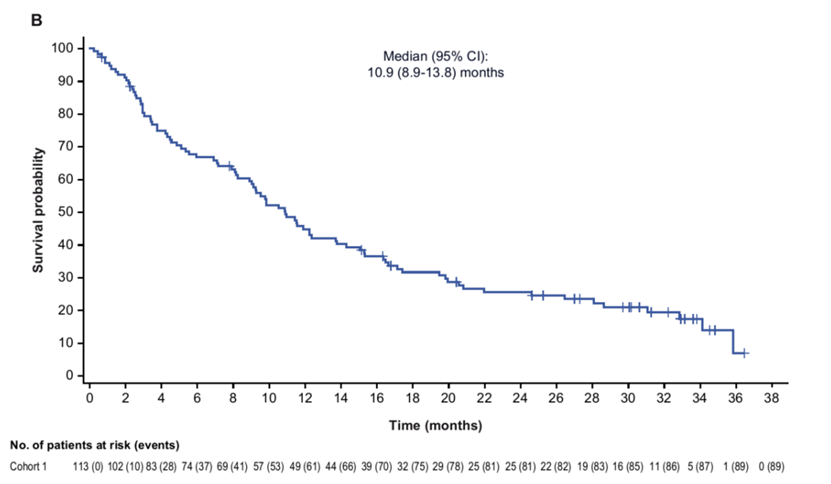
中位随访10.5个月后,客观缓解率为28% (95% CI 20.2-37.6),包括完全缓解6名患者和部分缓解26名患者。临床获益率 (包括完全缓解、部分缓解和稳定疾病≥6个月) 为38% (95% CI 29.1-47.7)。中位无进展生存期为5.4个月 (95% CI 3.5-6.9)。中位总生存期为10.9个月 (95% CI 8.9-13.8)。亚组分析显示,不同 UGT1A1 基因型的患者,客观缓解率无显著差异。大部分响应患者的肿瘤缩小幅度保持持久。

3.安全性分析
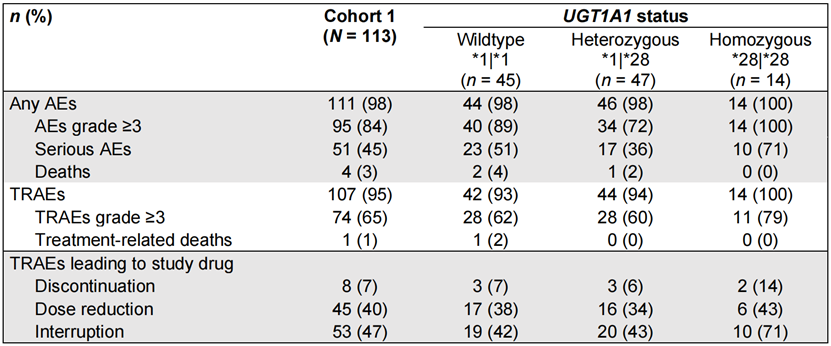
任何级别治疗相关不良事件发生率在总体队列1患者中为95%,治疗相关严重不良事件发生率为45%,因治疗相关死亡率为3%,因治疗相关不良事件停药率为7%。任何级别不良事件发生率在UGT1A1突变组为100%,严重不良事件发生率在UGT1A1突变组为79%,因治疗相关不良事件停药率在UGT1A1突变组为14%。所有患者根据给药说明和指南密切监测不良反应,无论UGT1A1基因型如何。SG治疗重度预治的晚期尿路上皮癌显示出可接受的安全性,且不良事件可管理。虽然不同UGT1A1基因型组的不良事件发生率有差异,但停药率均较低。
结论:在重度预治的晚期尿路上皮癌患者中,SG的疗效持续,客观缓解率保持在28%。安全性数据与SG已知的安全性特征一致,没有发现新的安全性信号。在晚期尿路上皮癌中,目前不推荐在SG启动前进行UGT1A1状态检测,因为所有患者都密切监测不良反应。TROPHY-U-01和TROPiCS-04试验的其他队列将继续研究UGT1A1状态对SG安全性的影响。数据支持在铂类化疗和免疫检查点抑制剂治疗后的局部晚期或转移性尿路上皮癌中使用SG。需要进一步评估SG在一线治疗中的效果,以及在其他线位治疗中的效果(在TROPHY-U-01的其他队列中)。
原始出处
Loriot Y, et al. 2024. TROPHY-U-01, a phase II open-label study of sacituzumab govitecan in patients with metastatic urothelial carcinoma progressing after platinum-based chemotherapy and checkpoint inhibitors: updated safety and efficacy outcomes. Annals of Oncology.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#尿路上皮癌# #Sacituzumab govitecan# #II期研究#
27