Lung Cancer:特异性97.9%,敏感性72.1%!吴一龙团队分析三项亚洲队列发现,通过FDA批准的液体活检可以作为肺癌组织检测的有力补充
2019-01-27 奇点糕 奇点网
2018年年末,我国肺癌领域的“大牛”吴一龙教授带领团队在Lung Cancer杂志上发表了一项研究[1],他们在三个亚洲人群队列中,对检测晚期非小细胞肺癌(NSCLC)患者表皮生长因子受体(EGFR)突变的COBAS®EGFR突变检测V2版在临床应用中的效果进行了评估。
2018年年末,我国肺癌领域的“大牛”吴一龙教授带领团队在Lung Cancer杂志上发表了一项研究,他们在三个亚洲人群队列中,对检测晚期非小细胞肺癌(NSCLC)患者表皮生长因子受体(EGFR)突变的COBAS®EGFR突变检测V2版在临床应用中的效果进行了评估。

吴一龙教授
在这次的研究中,研究人员对基于患者组织样本检测的COBAS® V1版和基于组织或血液样本检测的COBAS® V2版两种检测方法进行了对比。对三个队列的研究数据的汇总分析显示出了COBAS® V2版的高敏感性和高特异性,而且肿瘤负荷越大,检测的敏感性就越高。
这都没什么稀奇的,最让奇点糕觉得“奇妙”的,是他们发现,同样使用厄洛替尼进行治疗,与组织和血液检测均为阳性(T+/P+)相比,组织阳性/血检阴性(T+/P-)的患者居然无进展生存期和总生存期都明显更长!他们的肿瘤负荷也明显更低。真的有点出乎意料哦。
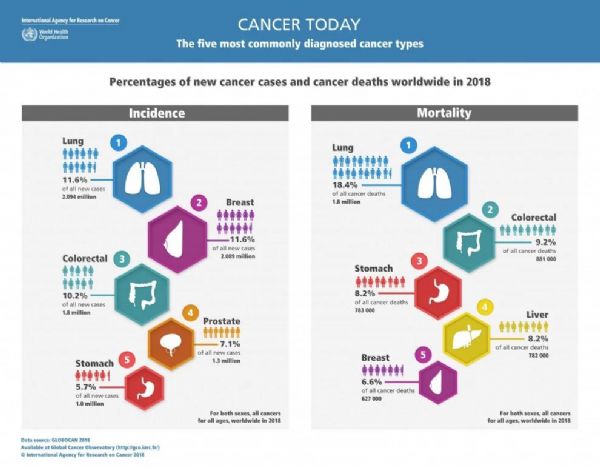
目前,在全世界范围内,肺癌的发病率和死亡率均高居榜首。在所有癌症类型中,肺癌造成的死亡占到18.4%,是第二名结直肠癌的2倍[2]。在肺癌中, NSCLC约占80%,大多数患者确诊时已处于晚期,手术治疗和放疗机会渺茫,化疗的效果也并不理想,中位生存期仅为8-10个月。
对于这部分患者来说,他们可以选择靶向治疗,比如说这个研究中所用的厄洛替尼,对于有EGFR突变的NSCLC患者,酪氨酸激酶抑制剂(TKI)能够明显延长生存期。患者携带的EGFR突变最常见的类型是19号外显子缺失或21号外显子L858R位点的突变。有这两种特定突变的话,TKI药物的效果才会好。
那么问题来了,如何对它们进行检测呢?其实可以选择的方法很多,例如免疫组织化学染色(IHC)、二代测序(NGS)、扩增组织突变系统(ARMS)和多种不同类型的PCR,这次研究的“重点观察对象”——COBAS® V2版所使用的技术就是荧光实时定量PCR(qRT-PCR),它的效率很高,可以检测出低频突变。
COBAS® EGFR突变检测V2版是一种伴随诊断,可以对石蜡包埋的肿瘤组织标本和液体活检(血液中循环游离DNA(cfDNA)的检测)标本进行检测,阳性结果的患者可以使用TKI药物厄洛替尼进行治疗。COBAS® EGFR突变检测V2版是首个通过FDA批准的液体活检,2018年也被CFDA批准在中国上市。
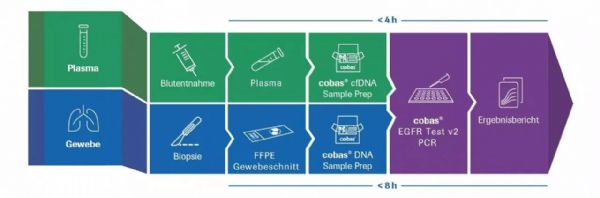
COBAS® EGFR突变检测V2工作流程
既然COBAS® V2版对肿瘤组织标本和血液标本都可以进行检测,那我们就有必要了解一下,不同标本的检测,区别在哪里?
目前,组织标本检测是比较传统的方法,也是“金标准”,它能够获取的癌细胞多,相对来说出现假阴性结果的概率更低。但是取肿瘤组织需要进行穿刺,对于患者来说比较痛苦,而且有可能会造成癌细胞的转移。另外,我们知道,肿瘤具有异质性,单一位点的穿刺不一定能够反映肿瘤的“全貌”。
而这些缺点恰好是液体活检可以弥补的,不仅如此,液体活检在患者接受治疗过程中对基因突变的动态监测,以及导致获得性耐药的基因突变的检测也是组织检测力所不能及的。不过,反过来说,液体活检则要担心一下血液中cfDNA量少的问题,这会拉低检测结果的敏感性,也会有更高比例的假阴性结果。
这样看来,组织检测和液体活检似乎是一对儿互补的搭配,那在实际应用中,COBAS® V2版的液体活检和金标准——组织检测的一致性究竟有多高呢?
吴一龙教授的研究给出了答案。研究选取的三个临床试验分别是ENSURE(NCT01342965)、FASTACT-2(NCT00883779)和ASPIRATION(NCT01310036),这三个临床试验的患者来自中国、菲律宾、韩国和泰国等亚洲国家及地区,试验均是探究厄洛替尼的疗效。
ENSURE试验的分析结果显示,EGFR突变检测结果为组织阳性/血检阳性(T+/P+)的患者接受化疗的中位无进展生存期(PFS)为4.6个月,厄洛替尼为8.3个月。而检测结果为T+/P-患者则分别为5.6个月和14.1个月!
中位总生存期(OS)的结果也是类似,接受厄洛替尼治疗的T+/P-患者达到28.7个月,比T+/P+患者延长了5.1个月。与ENSURE试验的分析结果相似,FASTACT-2和ASPIRATION试验中,同样是T+/P-的患者获得了更长的PFS和OS。
ASPIRATION试验中,T+/P+患者(蓝)和T+/P-患者(红)的PFS(左)和OS(右)的对比
对三个试验进行汇总分析后,研究人员计算出,液体活检的敏感性为72.1%,特异性为97.9%,组织检测和液体活检的一致性也高达84.4%。此外,研究人员还发现,与T+/P-的患者相比,T+/P+的患者在入组时总肿瘤的平均大小明显“更胜一筹”(49.8mm vs. 72.3mm),这也可能是T+/P-患者PFS和OS均长于T+/P+患者的原因。
除了影响两种检测的一致性之外,肿瘤的大小对液体活检的敏感性也有一定影响。研究人员将患者按照肿瘤大小划分为四组:50mm、100mm、150mm和200mm,液体活检的敏感性在各组间也不尽相同,分别为76.7%、92.1%、87.0%和100.0%。
不过研究人员指出,在他们选取的三个试验中,肿瘤>100mm的患者比较少,小样本量得出的结果可能不是非常准确。不过总的来说,这项研究表明,COBAS® EGFR 突变检测V2版可以作为基于组织的检测方法的有力补充。
当前,癌症的精准治疗已经成为了一个趋势,在非小细胞肺癌中,EGFR突变发生的几率相当高,尤其是亚洲的患者群体,可以达到40%-47%[5,6],这些患者都有可能从TKI药物中获益,所以,EGFR突变的检测是重要且必要的。未来,基于血液的液体活检的应用也会越来越广泛,它可以为患者提供更多的治疗选择,而且无创和快捷这些优点也能够为医生和患者争取更多的时间。
原始出处:Wu YL, Lee V, Liam CK, et al. Clinical utility of a blood-based EGFR mutation test in patients receiving first-line erlotinib therapy in the ENSURE, FASTACT-2, and ASPIRATION studies. Lung Cancer. 2018 Dec;126:1-8.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#FDA批准#
33
#特异性#
36
#活检#
34
#敏感性#
0