同济大学附属第十人民医院郑龙坡教授《AHM》:金属多酚网络改性的细胞外基质仿生骨支架有效改善骨缺损局部微环境
2024-03-13 BioMed科技 BioMed科技 发表于上海
本研究论文构建了一种金属多酚网络改性的细胞外基质仿生骨支架(图1),用于改善骨缺损局部微环境,旨在为骨缺损修复提供新的策略。
近期,同济大学附属第十人民医院骨科郑龙坡教授团队在国际生物材料领域权威期刊“Advanced Healthcare Materials”上发表了题为“ Metal–Phenolic Networks-Reinforced Extracellular Matrix Scaffold for Bone Regeneration via Combining Radical-Scavenging and Photo-Responsive Regulation of Microenvironment”的最新研究成果。

骨缺损修复在临床上一直是一项巨大挑战。骨缺损部位微环境是影响骨再生的关键因素之一。缺氧微环境导致局部炎性因子的增加和活性氧(ROS)的生成增加,ROS在微环境中的过度积累会阻碍新骨的生成,这是一个需要考虑的关键因素。
近年来,金属多酚网络(Metal-phenolic networks, MPNs)已被认为是一种有前景的生物材料。它融合了金属离子和多酚配体的多种性能,包括抗氧化、促成骨及促血管生成。此外,聚多巴胺(Polydopamine,PDA)改性的金属多酚网络(PMPNs)不仅具有光热性能,还通过近红外光激发的局部低温热刺激改善了成骨微环境。因此,金属多酚网络被可用于增强骨组织工程支架的性能,从而改善骨缺损微环境。
另外,猪脂肪组织细胞外基质(Extracellular matrix,ECM)具有良好的生物相容性和促血管生成能力,并含有大量活性基团,因此常被用于组织工程支架。而羟基磷灰石作为骨的无机成分,则常用于增强骨组织工程支架的力学和成骨性能。
基于以上背景,本研究论文构建了一种金属多酚网络改性的细胞外基质仿生骨支架(图1),用于改善骨缺损局部微环境,旨在为骨缺损修复提供新的策略。
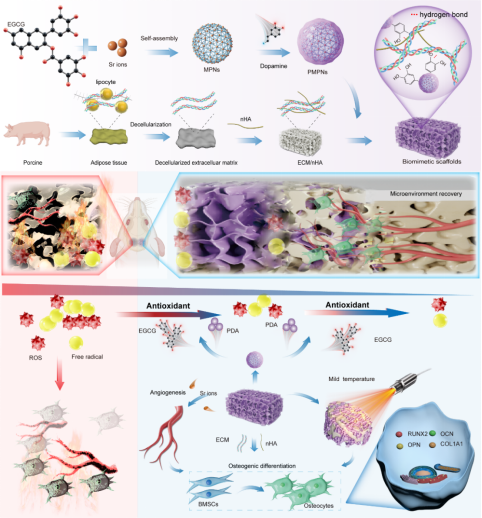
图1. PMPNs@ECM/nHAW仿生骨支架的构建及促进骨修复示意图
为了应对骨缺损微环境,课题组合成了具有多种性能的PMPNs纳米粒子。首先,通过水热法合成了MPNs, 然后,利用PDA修饰MPNs, 成功制备了大小均一的PMPNs纳米颗粒, 粒径大小 511.22 ± 164.99 nm(图2)。
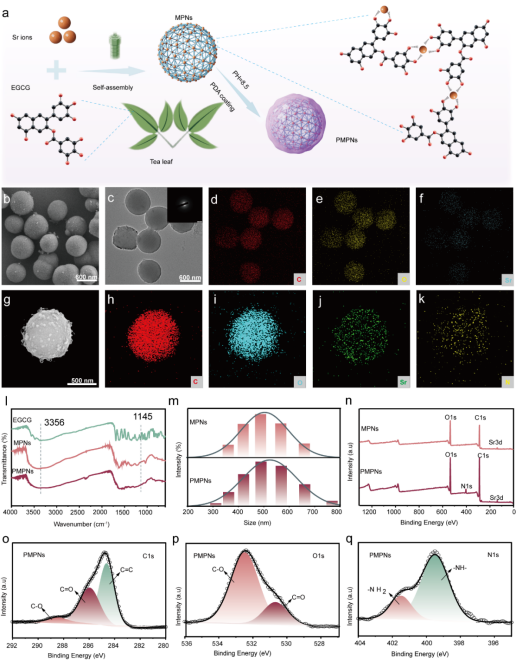
图2. PMPNs纳米粒子的合成及表征
将合成的PMPNs用于增强组织工程支架的性能。本研究选用了脂肪来源的ECM作为骨修复支架, 为了增强ECM力学性能及骨诱导能力,通过水热方法合成了羟基磷灰石纳米线,利用冷冻干燥技术将ECM及nHAW构建成复合支架,后续成功制备了PMPNs@ECM/nHAW仿生骨支架(图3)。
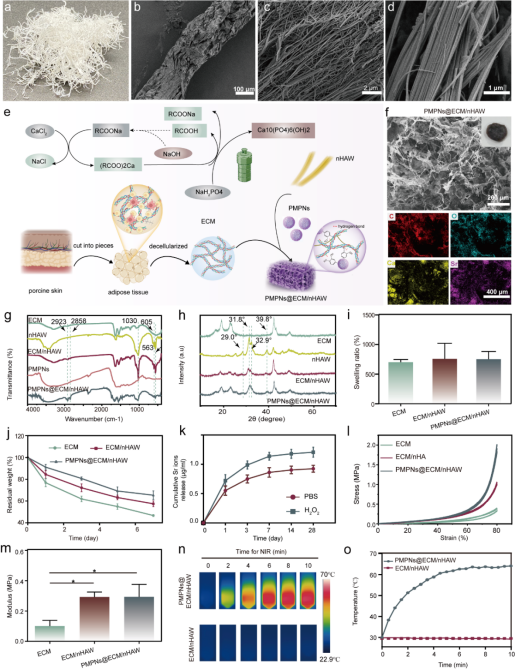
图3. PMPNs@ECM/nHAW仿生骨支架的构建及理化表征
接着,探究了PMPNs@ECM/nHAW仿生骨支架的理化性质, 结果表明,仿生骨支架具有良好的降解能力,ROS响应性Sr离子释放,另外也具有良好的光热性能(图3),展现出了多种优异的性能。
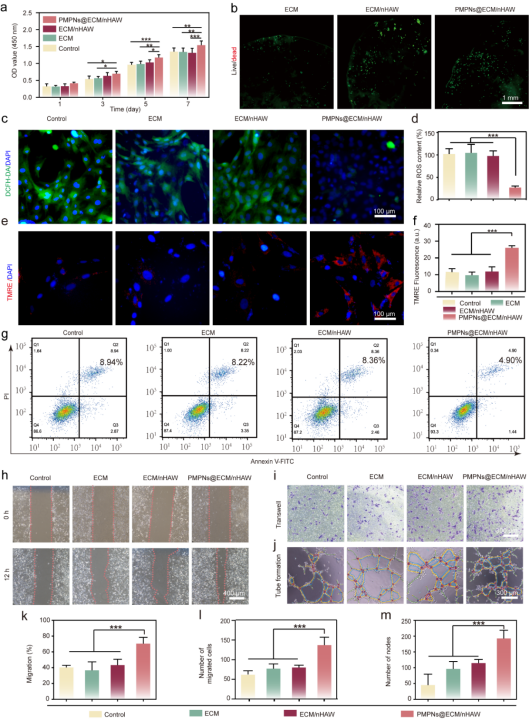
图 4. PMPNs@ECM/nHAW仿生骨支架的缓解细胞氧化应激、促进细胞迁移及成血管
通过活死染色及细胞增殖实验,证明了PMPNs@ECM/nHAW仿生骨支架具有良好的生物相容性;DCFH-DA荧光染色,Transwell实验,细胞划痕及成管实验证实了支架能够缓解细胞氧化应激、促进细胞迁移及小管形成(图4)。
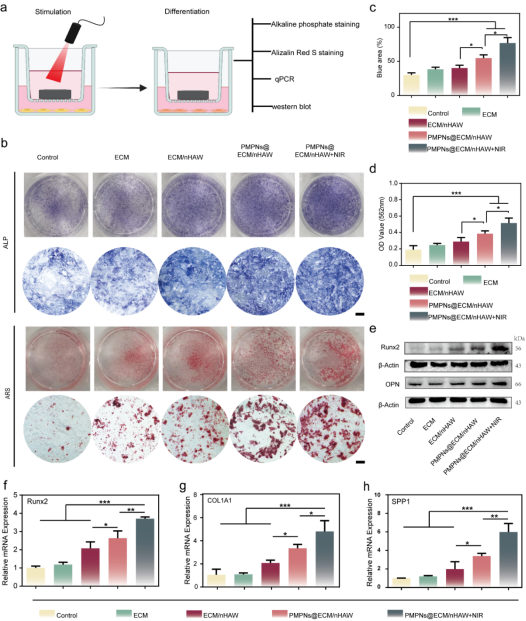
图 5. PMPNs@ECM/nHAW仿生骨支架联合NIR促进成骨分化
基于仿生骨支架的抗氧化性能与光热性能,本研究评估了仿生骨支架联合低温热刺激对骨髓基质干细胞(BMSCs)成骨分化的影响。通过碱性磷酸酶(ALP)染色和酸性磷酸盐(ARS)染色,结果显示在仿生骨支架联合低温热刺激条件下,能够显著促进BMSCs的成骨分化。此外,聚合酶链式反应(PCR)和Western blot(WB)进一步证实了仿生骨支架有助于促进成骨标志物的表达(图 5)。

图 6. PMPNs@ECM/nHAW仿生骨支架联合NIR促进大鼠颅骨缺损修复
最后,为评价PMPNs@ECM/nHAW仿生骨支架联合NIR促进大鼠颅骨缺损修复的效果,本研究构建了大鼠颅骨缺损模型。与体外实验结果一致,Micro-CT和组织学切片表明PMPNs@ECM/nHAW仿生骨支架联合低温热刺激能够促进缺损部位更多的新生骨组织的长入(图6)。
本研究构建的PMPNs@ECM/nHAW仿生骨支架具备良好抗氧化性能、光热性能和响应性离子释放性能,具有良好的生物相容性,能够促进细胞增殖、迁移及小管形成,联合NIR低温热刺激能够促进BMSCs的成骨分化。在体内,能够加速大鼠颅骨缺损修复。本研究不仅为骨组织再生提供了一种仿生支架,还引入了一种设计先进生物材料的新策略。
【论文通讯作者简介】
郑龙坡教授为该研究论文的第一通讯作者,同济大学附属第十人民医院为第一通讯单位,周子斐副研究员、陈峰研究员为共同通讯作者;同济大学2021级博士研究生刘志清、王天龙为本文的共同第一作者。本研究得到国家重点研发计划、国家自然科学基金面上项目、上海市自然基金面上项目等资助。
第一通讯作者郑龙坡教授,中共党员,医学博士、博士后、主任医师、教授,同济大学、上海大学、上海体育大学、南京医科大学博士生导师、博士后指导老师。现任上海市创伤急救中心(北区)主任,同济大学附属第十人民医院骨科行政副主任、创伤骨科主任,骨科智能化微创诊疗中心主任。研究方向为复杂骨盆髋臼及四肢骨折的微创治疗与智能化,骨科生物材料,关节成形术等。主持国家自然科学基金、科技部重点研发计划子课题等5项,上海市科委课题6项,上海市经信委人工智能重点专项1项,中央高校交叉学科重点项目1项、同济大学教改项目1项等,总科研经费达1800余万元;先后获上海市科技进步二等奖2项,国家教育部科技进步二等奖、一等奖各1项;获发明/实用新型专利31项。近年来郑龙坡教授团队在Adv Healthc Mater.(2024)、Sci Adv.(2024)、Adv.Funct.Mater.(2023)、Compos Part B-eng.(2022)、J Nanobiotechnol.(2020,2021)、Int J Nanomedicine.(2020)、Adv Sci (Weinh)(2019)等国际知名期刊上发表系列研究论文。
原文链接:
https://onlinelibrary.wiley.com/doi/abs/10.1002/adhm.202304158
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#金属多酚网络# #细胞外基质仿生骨支架# #骨缺损#
17