ESMO 2022:双艾组合卡瑞利珠单抗联合阿帕替尼可显著改善不可切除HCC的生存期(SHR-1210-III-310研究)
2022-09-12 MedSci原创 MedSci原创
根据2022年ESMO大会期间公布的一项III期研究(NCT03764293)的结果,在不可切除的肝细胞癌(HCC)患者中,与索拉非尼(多吉美)相比,采用卡瑞利珠单抗+阿帕替尼作为一线治疗可显著改善无
根据2022年ESMO大会期间公布的一项III期研究(NCT03764293)的结果,在不可切除的肝细胞癌(HCC)患者中,与索拉非尼(多吉美)相比,采用卡瑞利珠单抗+阿帕替尼作为一线治疗可显著改善无进展生存期(PFS)和总生存期(OS)。
与索拉非尼组的15.2个月(95%CI,13.0-18.5)相比,卡瑞利珠单抗和阿帕替尼组的中位OS为22.1个月(95%CI,19.1-27.2),相当于死亡风险降低38%(HR,0.62;95%CI,0.49-0.80;P<0.0001)。与索拉非尼组的3.7个月(95%CI,2.8-3.7)相比,卡瑞利珠单抗和阿帕替尼组的中位PFS为5.6个月(95%CI,5.5-6.3),进展或死亡风险降低48%(HR,0.52;95%CI,0.41-0.65;P<0.0001)。
“这是第一个阳性结果的国际3期研究,报告了在不可切除的HCC中,免疫治疗和小分子TKI联合治疗与索拉非尼相比具有显著的PFS和OS获益。”主要研究者、南京金陵医院秦叔逵教授在报告结果时表示。“此外,迄今为止,在晚期HCC一线关键III期研究中观察到的卡瑞利珠单抗加阿帕替尼的OS最长,为22.1个月。”
SHR-1210-III-310 研究是一项卡瑞利珠单抗联合甲磺酸阿帕替尼对比索拉非尼一线治疗晚期肝细胞癌(HCC)的随机、对照、开放、国际多中心 III 期临床研究,涵盖 95 家来自全球的研究中心,旨在评价卡瑞利珠单抗联合甲磺酸阿帕替尼对比索拉非尼在一线晚期 HCC 患者中的有效性和安全性。
研究纳入主要人群为年龄≥ 18 岁且经病理组织学或细胞学确诊的 HCC 患者;既往未接受过任何针对 HCC 的系统治疗;巴塞罗那临床肝癌分期(BCLC 分期)为 B 期或 C 期;Child-Pugh 肝功能分级 A 级;ECOG 评分:0~1;根据 RECIST v1.1 标准存在至少一个可测量病灶。
研究主要终点为总生存期(OS)和由盲态独立影像评审委员会(BIRC)基于 RECIST v1.1 标准评估的无进展生存期(PFS);次要终点包括疾病进展时间(TTP)、客观缓解率(ORR)、疾病控制率(DCR)和缓解持续时间(DoR);安全性;药代动力学和免疫原性分析。
在研究中,患者被平均随机分配至卡瑞利珠单抗(一种PD-1抑制剂)200mg静脉给药每2周一次加口服每日阿帕替尼(一种VEGFR2 TKI)250mg(n=272)或口服索拉非尼400mg每日两次(n=271)。联合治疗组患者的中位年龄为58岁,而索拉非尼组为56岁。两组中的大多数患者在亚洲入组(82.7%),每组47例患者为非亚洲人。
各组的基线特征相似。在卡瑞利珠单抗+阿帕替尼组中,大多数患者患有BCLCC期疾病(86.8%),大多数患者的ECOG体能状态为1(55.9%),35.3%的患者的AFP≥400ng/mL。73.5%的患者有可见的血管侵犯和肝外转移,最常见的病因是乙型肝炎病毒感染(76.5%)。略高于一半的患者在进入研究前接受过局部治疗(59.2%)。
盲态独立审查委员会和RECISTv1.1标准确认的客观缓解率(ORR)分别为25.4%(卡瑞利珠单抗+阿帕替尼)和5.9%(索拉非尼),表明联合治疗具有优效性(P<0.0001)。根据改良RECIST标准确定的ORR,这些结果相似,联合治疗组为33.1%,索拉非尼组为10.0%(P<0.0001)。根据RECISTv1.1,卡瑞利珠单抗+阿帕替尼组的中位缓解持续时间为14.8个月,索拉非尼组为9.2个月。
根据RECISTv1.1标准,卡瑞利珠单抗联合阿帕替尼组有3例完全缓解(CR),而索拉非尼组有1例CR。使用改良的RECIST标准,联合治疗组有14例CR,而单药治疗组有3例CR。当包括疾病稳定时,根据RECISTv1.1,联合治疗的疾病控制率(DCR)为78.3%,而单药治疗为53.9%。根据改良标准,这些发生率相似。
卡瑞利珠单抗+阿帕替尼组的6个月PFS率为44.6%,而索拉非尼组为22.7%。对于OS,在12个月时,卡瑞利珠单抗+阿帕替尼组有76.5%的患者存活,而索拉非尼组有60.8%的患者存活。第18个月时,联合治疗组的OS率为60.9%,单药治疗组为45.2%。
秦教授指出,这些获益在各亚组中都能看到,按地理区域分析时,OS的风险比为0.55,在非亚洲患者中有利于联合治疗。然而,由于人群样本量较小,统计分析有限,观察到的置信区间非常宽(95%CI,0.29-1.02)。在不同亚组中,PFS和OS支持卡瑞利珠单抗+阿帕替尼。
表 1 研究关键有效性结果总结(ITT集) [ 1 ]
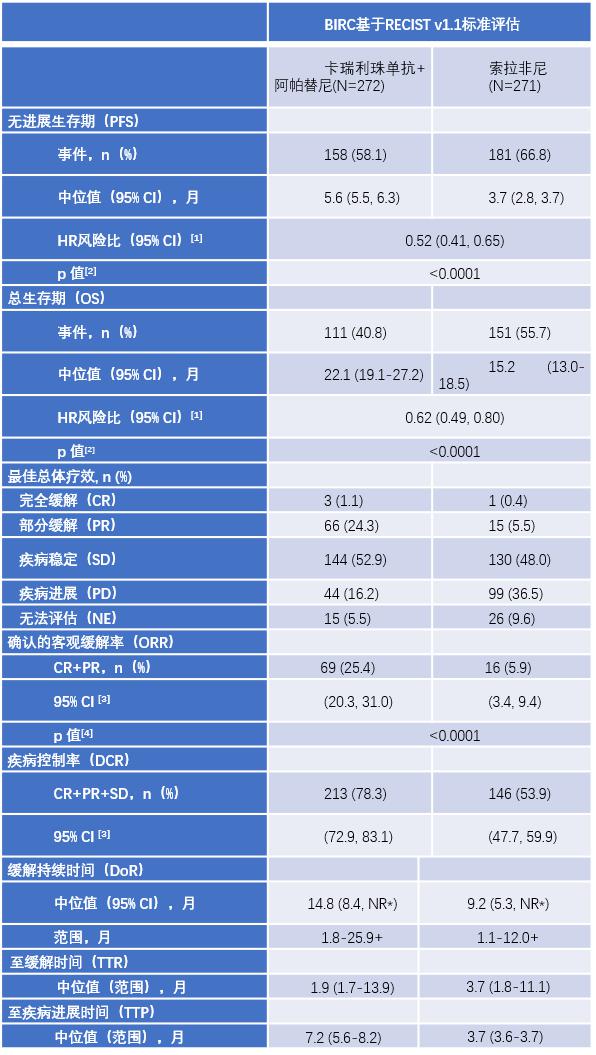
3/4级治疗相关不良反应(TRAE)的发生率:卡瑞利珠单抗+阿帕替尼组为80.5%,索拉非尼组为52%。每个治疗组发生1例5级TRAE。联合治疗组24.3%的患者发生严重TRAE,而单药治疗组为5.9%。联合治疗组80.5%的患者因TRAE需要调整剂量或中断治疗,而单药治疗组为50.2%;然而,两组之间所有治疗组分的治疗中止率相似,卡瑞利珠单抗+阿帕替尼组为3.7%,索拉非尼组为4.5%。
在卡瑞利珠单抗+阿帕替尼联合治疗组中,最常见的严重程度≥3级的TRAE为高血压(37.5%)、AST升高(16.5%)、ALT升高(12.9%)、掌跖红肿疼痛(PPE;12.1%)和血小板计数降低(11.8%)。对于索拉非尼组,最常见的≥3级TRAE为PPE(15.2%)和高血压(14.9%)。
“卡瑞利珠单抗+阿帕替尼的组合总体耐受性良好,安全性特征与每种单独药物和基础疾病一致,”秦教授说。“这些发现支持卡瑞利珠单抗+阿帕替尼代表了不可切除HCC的另一种新的一线治疗选择。”
在对研究结果的讨论中,来自加州大学旧金山分校Helen Diller家庭综合癌症中心的R. Katie Kelley教授描述了使用口服血管生成抑制剂的潜在优势,但也要考虑到联合用药时观察到的肝毒性,需要仔细选择患者。此外,她指出,将数据外推至非亚洲人群存在挑战,特别是考虑到在基础病因中观察到的乙型肝炎病毒感染率较高。
Kelley说:“多种一线和后期治疗选择的出现标志着HCC的巨大进展,并为个体化治疗决策提供了新的机会。区域和病因可能影响涉及免疫检查点抑制剂治疗的HCC试验的结果。全球试验需要与监管机构进行提前规划,以确定最低亚群阈值。”
恒瑞医药全球研发总裁张连山博士表示:" 此次 SHR-1210- Ⅲ -310 研究能够取得成功,药物本身特性是重要因素之一。本次研究选择的是恒瑞医药自主研发的 1 类新药甲磺酸阿帕替尼片和注射用卡瑞利珠单抗,两者联合具有机制协同、优势互补的作用。目前,卡瑞利珠单抗联合阿帕替尼的治疗策略已进一步在肝细胞辅助治疗和联合 TACE 等治疗领域分别开展了 III 期临床研究(SHR-1210-III-325 和 SHR-1210-III-336),其研究结果同样值得期待。未来,恒瑞医药将深入实施科技创新和国际化双轮驱动战略,持续加强创新药临床研究和应用,并稳步推进以‘双艾’为代表的自主创新产品积极走向国际,致力于为临床急需提供更多更优的解决方案,服务健康中国,惠及全球患者。"
参考资料:
LBA35 Camrelizumb ( C ) plus rivoceranib ( R ) vs. sorafenib ( S ) as first-line therapy for unresectable hepatocellularcarcinoma ( uHCC ) : a randomized, phase III trial. ESMO 2022
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#III#
48
#SMO#
37
#HCC#
52
#ESMO#
52
#生存期#
45
#卡瑞利珠#
50
期待再乳腺癌上的使用
36