Cancers:循环肿瘤细胞(CTCs)跟转移性结直肠癌患者的临床相关性:前瞻性COLOSPOT研究
2021-06-14 yd2015 MedSci原创
D28和D0-D28 循环肿瘤细胞(CTCs)检测跟结直肠癌患者的预后有关,可用于FOLFIRI–贝伐珠单抗治疗的疗效监测。
结直肠癌(CRC)是发病率和死亡率都较高的恶性肿瘤之一。对于转移性CRC,目前常用的一线治疗药物包括靶向药物(贝伐珠单抗/西妥昔单抗)联合化疗(奥沙利铂、伊立替康、氟尿嘧啶、希罗达等)。循环肿瘤细胞(CTCs)被称为实时的液体活检,可用于肿瘤治疗的监测。目前FDA批准的CellSearch ®system可用于转移性CRC中CTCs的检测,并且证实患者治疗前有≥3 CTCs时无进展生存(PFS)和总生存期(OS)较差。但是,CTCs会表现出表型特异性,某些可能不会表达或表达很弱的上皮细胞标志物,尤其处于上皮-间质转化(EMT)过程时,CellSearch ®system则很难检测出来。因此,来自法国的研究团队构建了CK19-EPISPOT assay,并且开展了一项前瞻性研究COLOSPOT,主要是应用CK19-EPISPOT assay和CellSearch ®system检测CTCs,并且评估CTCs在应用FOLFIRI-贝伐珠单抗治疗的转移性结直肠癌患者的预后价值。相关研究结果发表在Cancers杂志上。

该研究是在法国的11研究中心开展,患者接受FIOLFIRI-贝伐珠单抗治疗。应用EPISPOT assay在患者基线(D 0 ) ,第14天 (D 14 ), 第28天 (D 28 ), 第42天 (D 42 ) 和 第56天 (D 56 )检测CTCs;而应用CellSearch ®system在患者基线(D 0 ) ,和第28天 (D 28 )检测CTCs。评估不同时间点CTCs和PFS、OS的关系。研究纳入155例可评估患者,中位随访24.5个月(range, 0.99–75.04个月), 中位PFS 和 OS 分别为9.4个月 (95% CI, 8.1–10.2个月)和26.2个月(95% CI, 21.3–29.8个月)。
EPISPOT assay检测,D 0时,32/152 (21%) 患者有≥1CTC/sample 和18/152 had ≥2 CTCs/sample (11.8%) 。治疗期间,至少有1个CTC的患者数为15.4% (D 14), 12.3% (D28)9.6%(D42) , 和11.5%(D56)。而用 CellSearch ® assay检测时, D0和D28检测点分别有59/150 (39.3%)和13/138 (9.4%) 患者有≥3 CTCs/sample。
EPISPOT assay检测,D28时,≥2 CTCs的患者较<2 CTCs患者的PFS和OS更差,有统计学差异(中位PFS = 5.82个月, 95% CI (0.92–6.37个月) vs. 8.28个月, 95% CI (7.20–9.17个月); p = 0.0082;中位OS = 10.28 个月, 95% CI (4.63–14.26个月) vs 24.84个月, 95% CI (20.11–28.45个月); p = 0.0003)。CellSearch ® assay检测,D 28时 , ≥3 CTCs 患者较<3 CTCs 具有更差的PFS和OS,有统计学差异(中位PFS = 5.50个月, 95% CI (1.90–6.93个月) vs. 8.64个月, 95% CI(7.67–9.56个月); p < 0.0001;中位OS = 12.91个月, 95% CI (4.63–17.77个月) vs. 25.27个月, 95% CI (20.40–30.10个月); p < 0.0001)。
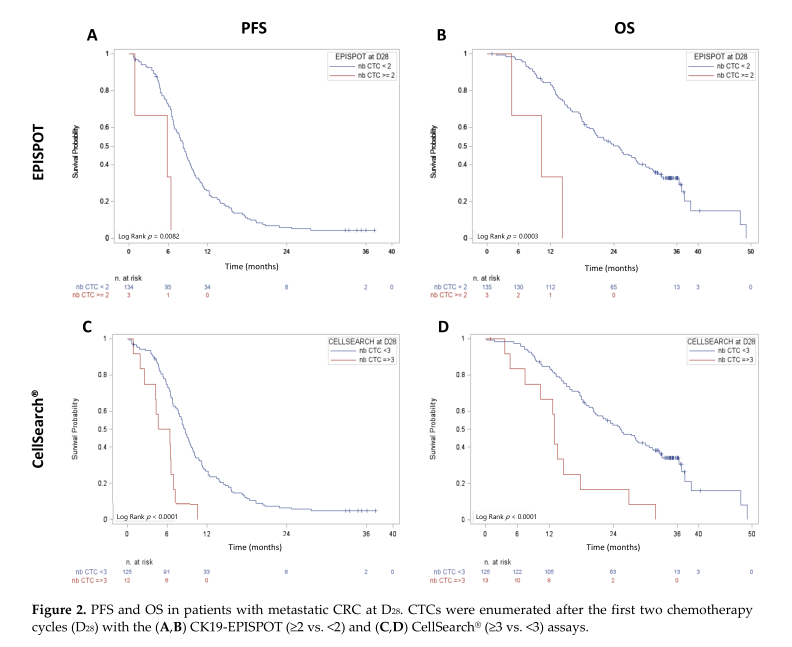
D28时两种检测方法分组的PFS和OS
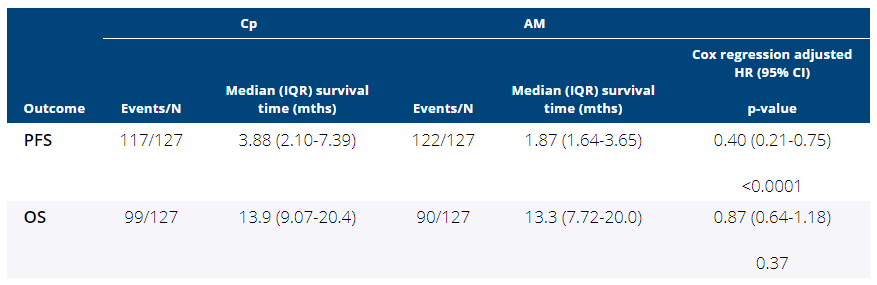
将D0和D28的结果分为两组:(1)为D0和D28 CTC都阳性(2)D0和D28都阴性,或只有D0或D28阳性。EPISPOT assay检测,第1组患者的PFS和OS更差(中位PFS = 7.36个月, 95% CI (1.84–8.97个月) vs.9.43个月, 95% CI (8.08–10.25 个月); p = 0.0161;中位OS = 13.83个月, 95%CI (5.55–31.63个月) vs. 25.99 个月, 95% CI (20.99–29.17个月); p = 0.0176)。CellSearch ® assay检测,同样第1组患者的PFS和OS更差(中位PFS = 6.6个月, 95% CI (1.84–7.85个月) vs. 9.46个月,95% CI (8.54–10.31个月); p = 0.0018;中位OS = 14.13个月, 95% CI (5.55–18.69个月) vs. 26.18个月, 95% CI (21.29–29.83个月); p = 0.0010)。
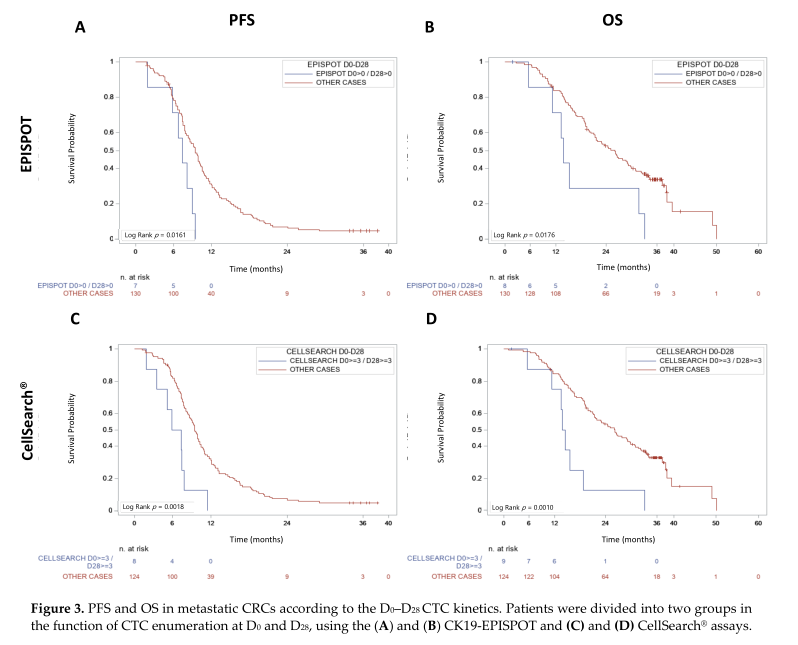
D0-D28时两种检测方法分组的PFS和OS
单变量分析,早期CTC动态(两种检测方法)、D0时ECOG PS,和BRAF突变状态是PFS和OS的预测因素。右侧结肠的原发肿瘤也与较差的OS显著相关。在多变量分析中,根据CK19-EPISPOT检测D0 - D28 CTC动态变化(HR 2.445, 95% CI (1.04-5.78),p = 0.0414)和CellSearch® system 检测D0 - D28 CTC动态变化(HR 2.461, 95% CI (1.06-5.74),p = 0.037)仍然是PFS的显著预测因子,但不是OS的显著预测因子。
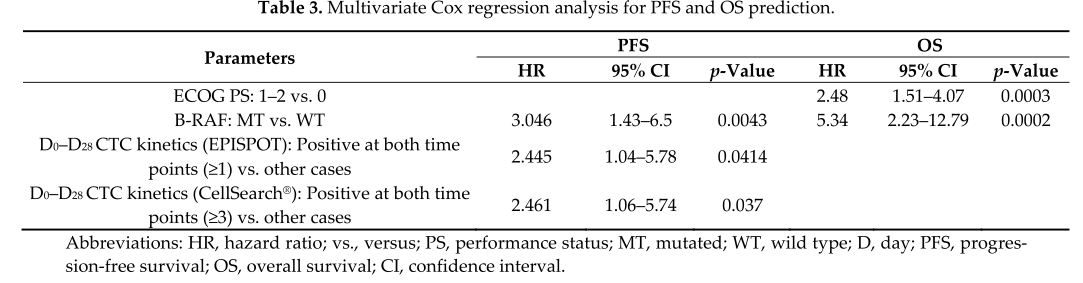
多变量分析PFS和OS相关因素
综上,D28和D0-D28 循环肿瘤细胞(CTCs)检测跟结直肠癌患者的预后有关,可用于FOLFIRI–贝伐珠单抗治疗的疗效监测。
原始出处:
Mazard, T.; Cayrefourcq, L.;Perriard, F.; et al. Clinical Relevance of Viable Circulating Tumor Cells in Patients with Metastatic Colorectal Cancer: The COLOSPOT Prospective Study. Cancers 2021, 13, 2966. https://doi.org/10.3390/cancers13122966.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#ERS#
48
#前瞻性#
27
#Spot#
32
#CTC#
25
#CTCs#
27
#相关性#
28
#TCS#
29
#肿瘤细胞#
0
#转移性#
33
#结直肠#
30