Cell: 里程碑!新化合物逆转帕金森氏病突变影响
2013-08-20 ebiotrade bio360
日前,来自加州大学旧金山分校等机构的研究人员利用在抗皱霜中发现的一种化合物,阻止了遗传性帕金森氏病致病突变损伤造成的神经细胞死亡。相似的方法有可能能够防治帕金森氏病患者大脑中的细胞死亡,研究小组将这项研究在线发表在8月15日的《细胞》(Cell)杂志上。【原文下载】 研究人员表示,这是第一次高度特异性地靶向提高而非抑制一种激酶的活性,这一成果标志着药理学的一个里程碑。新研究为有可能利用相似的
日前,来自加州大学旧金山分校等机构的研究人员利用在抗皱霜中发现的一种化合物,阻止了遗传性帕金森氏病致病突变损伤造成的神经细胞死亡。相似的方法有可能能够防治帕金森氏病患者大脑中的细胞死亡,研究小组将这项研究在线发表在8月15日的《细胞》(Cell)杂志上。【原文下载】
研究人员表示,这是第一次高度特异性地靶向提高而非抑制一种激酶的活性,这一成果标志着药理学的一个里程碑。新研究为有可能利用相似的制药策略来对抗糖尿病和癌症的等其他疾病带来了希望。
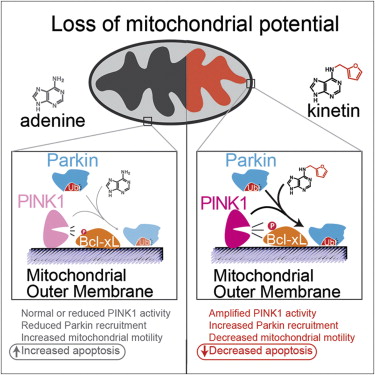
突变导致靶酶 PINK1 功能失常,是一些早发性帕金森氏病病例的直接病因。 PINK1 活性丧失会损害细胞的动力工厂:线粒体。众所周知,线粒体能够将食物能量转换成为细胞所利用的另一种化学能形式——分子 ATP 。
在帕金森氏病中,线粒体功能障碍与大脑黑质区域中多巴胺生成神经细胞死亡有关,黑质在控制运动中起重要的作用。多巴胺生成神经细胞死亡是帕金森氏病的一个标志,是导致强直和震颤等显著症状的病因。
在 Shokat 领导下,加州大学旧金山分校的研究人员利用一种称作为 kinetin 的化合物,将神经细胞中突变的 PINK1 酶活性提升至了接近正常水平。
“由于在人类 PINK1 突变导致了帕金森氏病,发现 kinetin 能够提高突变 kinetin 活性至接近正常水平,提出了利用 kinetin 治疗这些患者的可能性,” Shokat 说。
研究人员还发现,在具有正常 PINK1 的神经细胞中, kinetin 提高酶活性使其超出了标准水平。这一研究发现有可能与最常见的帕金森氏病形式相关,在这类疾病中 PINK1 没有突变,以往的研究证实类似的 PINK1 过度活化可以在果蝇帕金森氏病模型中减慢另一种缺陷造成的异常运动形成。这种缺陷提高了α-synuclein蛋白生成,这也是一些遗传性帕金森氏病病例的致病原因。
Shokat 说,新研究证实,可在缺乏 PINK1 突变的人类神经细胞中提高 PINK1 ,由此表明在无 PINK1 的常见帕金森氏病中 kinetin 有可能也具有治疗潜力。
帕金森氏病是仅次于阿尔茨海默氏症的第二常见的神经退行性疾病,根据美国疾病预防和控制中心的统计,它是美国第14位的主要死亡原因。当前的治疗主要针对性地提高多巴胺生成神经细胞丧失的大脑区域对多巴胺的利用率。
Shokat 说,尽管在过去的 10 年里研发了许多的药物来抑制激酶的活性,目前有15种药物获得批准用于治疗癌症,目前市场上尚没有直接促进激酶活性的药物。
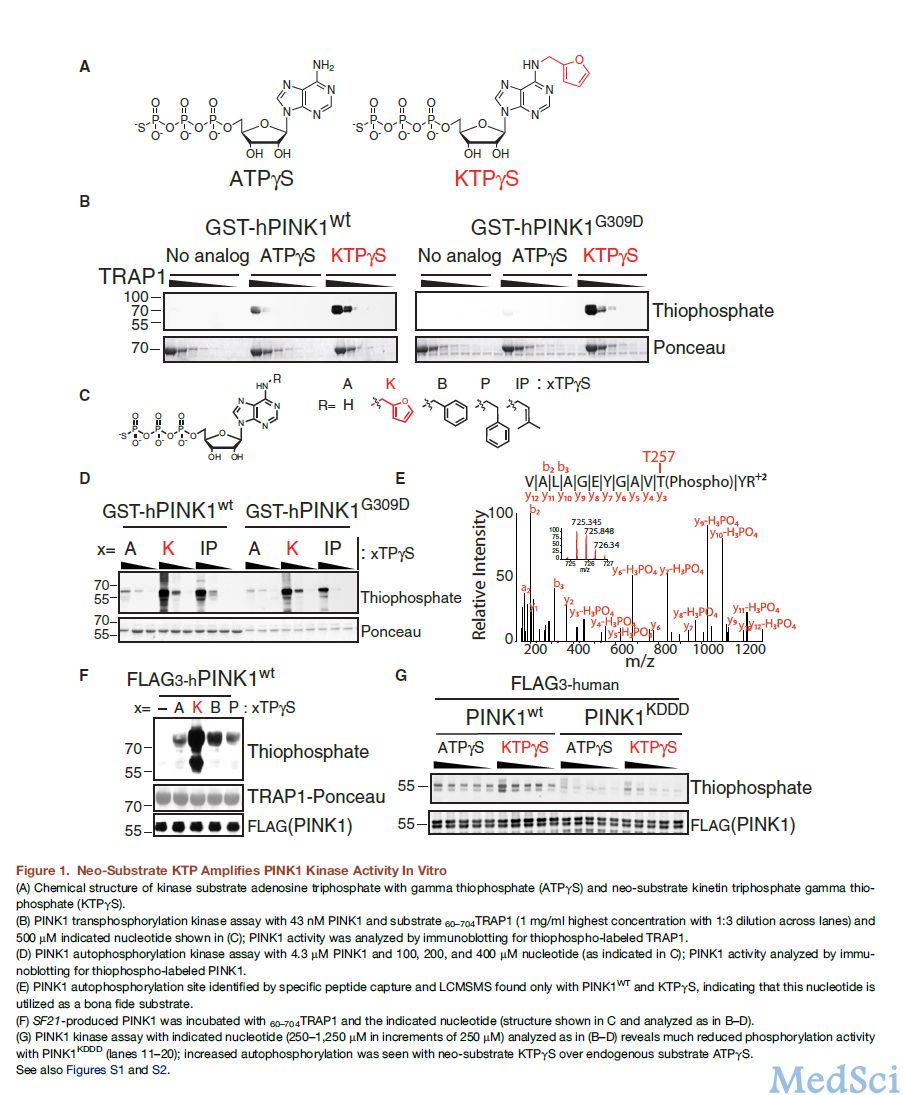
Shokat 采用了一种非传统的方法取得突破,用药物提高 PINK1 的活性。他靶向了该酶的“底物”,底物分子结合到酶上会发生快速的化学转变。
PINK1 所利用的底物是 ATP ,这一化学反应帮助 PINK1 转而驱动了另一种酶 Parkin 激活。
两种酶以往均证实与帕金森氏病密切相关。 PINK1 和 Parkin 共同作用,监控了线粒体的健康,帮助启动修复或清除细胞内的受损线粒体,由此促进了细胞存活。
“由于过去科学家们没有想到针对该酶开发一种新底物这一方法,因此没有考虑采用治疗方法来提高 PINK1 的活性,” Shokat 说。
“我们发现相比于天然底物 ATP ,称作为 KTP 的小分子能够加速 PINK1 催化的化学反应。这种优于自然的反应真是闻所未闻。”
Shokat 说, KTP 过大不适合其他的激酶,但 PINK1 具有一个较大的 ATP “口袋”可以容纳 KTP 。
在发现 KTP 的潜力后,研究确定了在细胞中 kinetin 可转化为 KTP 。实验表明, kinetin 可以通过血管进入到大脑中,当前 kinetin 已被用于口服给药治疗一种称作为家族性自主神经功能异常的罕见遗传性神经系统疾病。
原始出处:
Nicholas T. Hertz, Amandine Berthet, Martin L. Sos, Kurt S. Thorn, Al L. Burlingame, Ken Nakamura, Kevan M. Shokat . A Neo-Substrate that Amplifies Catalytic Activity of Parkin son's-Disease-Related Kinase PINK1. Cell, 15 August 2013; DOI: 10.1016/j.cell.2013.07.030 【原文下载】
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#里程碑#
42
#化合物#
0
#Cell#
32
#CEL#
36