拜耳启动Stivarga III期COAST研究
拜耳(Bayer)2月20日宣布,已启动抗癌药Stivarga(regorafenib)III期COAST研究的患者招募。COAST是一项随机、双盲、安慰剂对照试验,将招募750例已根治性切除肝转移且已完成所有已计划化疗疗程的结直肠癌(CRC)患者,研究中患者将以1:1的比例,随机接受160mg regorafenib或安慰剂
生物谷 - 新药,FDA - 2014-02-21
拜耳的Stivarga未被NICE纳入肝癌的治疗
现在看来,肝癌患者不太可能获得拜耳的Stivarga,因为成本监管机构发布了拒绝为该药物提供资金的最终草案。美国国家健康和护理研究所(NICE)坚持不推荐这种药物用于治疗已经扩散到全身的肝癌,不可手术的,而且之前也曾使用过Stivarga这种药物的患者。Stivarga是肝癌患者的首选治疗方案,但对于那些不能耐受或无应答的患者,唯一的选择是最好的支持治疗。在这些情况下,Stivarga(regor
MedSci原创 - 拜耳的Stivarga - 2018-02-09
拜耳Stivarga新适应症获日本批准
拜耳(Bayer)今天宣布,口服多激酶抑制剂Stivarga (regorafenib)新适应症申请获日本卫生劳动福利部(MHLW)批准,用于既往经系统性癌症治疗(systemic cancer therapy)后病情恶化的肠胃道间质瘤(GIST)患者的治疗。这是Stivarga在日本获批的第二个适应症。 Stivarga新适应症的批准,是基于关键性III期GRID试验的结果。数据表明,在既
生物谷 - 新药,FDA - 2013-08-21
CHMP支持批准拜耳抗癌药Stivarga用于GIST的治疗
拜耳(Bayer)6月27日宣布,抗癌药Stivarga(regorafenib)获得了欧洲药品管理局(EMA)人用医药产品委员会(CHMP)的积极意见。CHMP建议批准Stivarga用于既往经2种酪氨酸激酶抑制剂(Gleevec、Sutent)治疗后病情恶化或不耐受的不可切除性或转移性胃肠道间质瘤(GIST)患者的治疗。
生物谷 - 抗癌药,CHMP - 2014-07-02
拜耳的Stivarga被纳入NICE用于治疗胃肠道间质肿瘤
拜耳的Stivarga已经被国家健康和护理研究所(NICE)推荐用于一些胃肠道间质肿瘤(GIST)患者的治疗。具体地说,成本监督机构已经裁定,这种治疗方法可以在国民保健服务(NHS)中定期得到资助,以治疗那些不能进行肿瘤切除治疗或疾病进展发生转移的GIST患者,或者是那些对伊马替尼(imatinib)和舒尼替尼
MedSci原创 - Stivarga,NICE - 2017-11-20
拜耳向EMA提交Stivarga治疗GIST新适应症申请
拜耳(Bayer)9月5日宣布,已向欧洲药品管理局(EMA)提交了口服多激酶抑制剂Stivarga(regorafenib)的上市许可申请(MAA),寻求批准用于既往经2种酪氨酸激酶抑制剂(Gleevec、Sutent)治疗后病情恶化或不能手术切除的胃肠道间质瘤(GIST)患者的治疗。此前,Stivarga于2013年8月30日获EMA批准用
生物谷 - 新药,FDA - 2013-09-09
拜耳抗癌药Stivarga肝细胞癌III期临床大获成功
拜耳抗癌药Stivarga近日在关键III期临床试验中获得积极数据,有望将肝细胞癌列入适应症名单。Stivarga是一种口服的多激酶抑制剂,能够抑制肿瘤发生发展中VEGFR 1-3、KIT、RET、PDGFR及FGFR等多种重要激酶的活性,目前已经在多个肿瘤中获批。这项名为RESORCE的III期临床试验数据表明,Stivarga (regorafenib)能够显着
生物谷 - 拜耳,Stivarga,抗癌药,肝细胞癌 - 2016-05-09
拜耳抗癌药Stivarga治疗肝细胞癌III期临床获得成功
德国制药巨头拜耳(Bayer)近日公布了抗癌药Stivarga(regorafenib,瑞戈非尼)治疗晚期肝细胞癌(HCC)的一项III期临床研究RESORCE的积极数据。该研究在接受拜耳抗癌药多吉美(Nexavar,通用名:sorafenib,索拉非尼)治疗期间病情进展的不可切除性肝细胞癌(HCC)患者中开展,调查了Stivarga联合最佳支持治疗(BSC)的疗效和安全性
生物谷 - 肝癌,Stivarga,Regorafenib,瑞戈非尼 - 2016-06-29
拜耳/强生拜瑞妥® 预防静脉血栓栓塞
一项最新3期临床试验显示和阿司匹林相比,拜耳和杨森的新型口服抗凝剂(NOAC)拜瑞妥 (利伐沙班片)可以更有效地防止复发性血栓,同时不会增加出血风险。
生物谷 - 拜瑞妥®,静脉血栓栓塞 - 2017-12-05
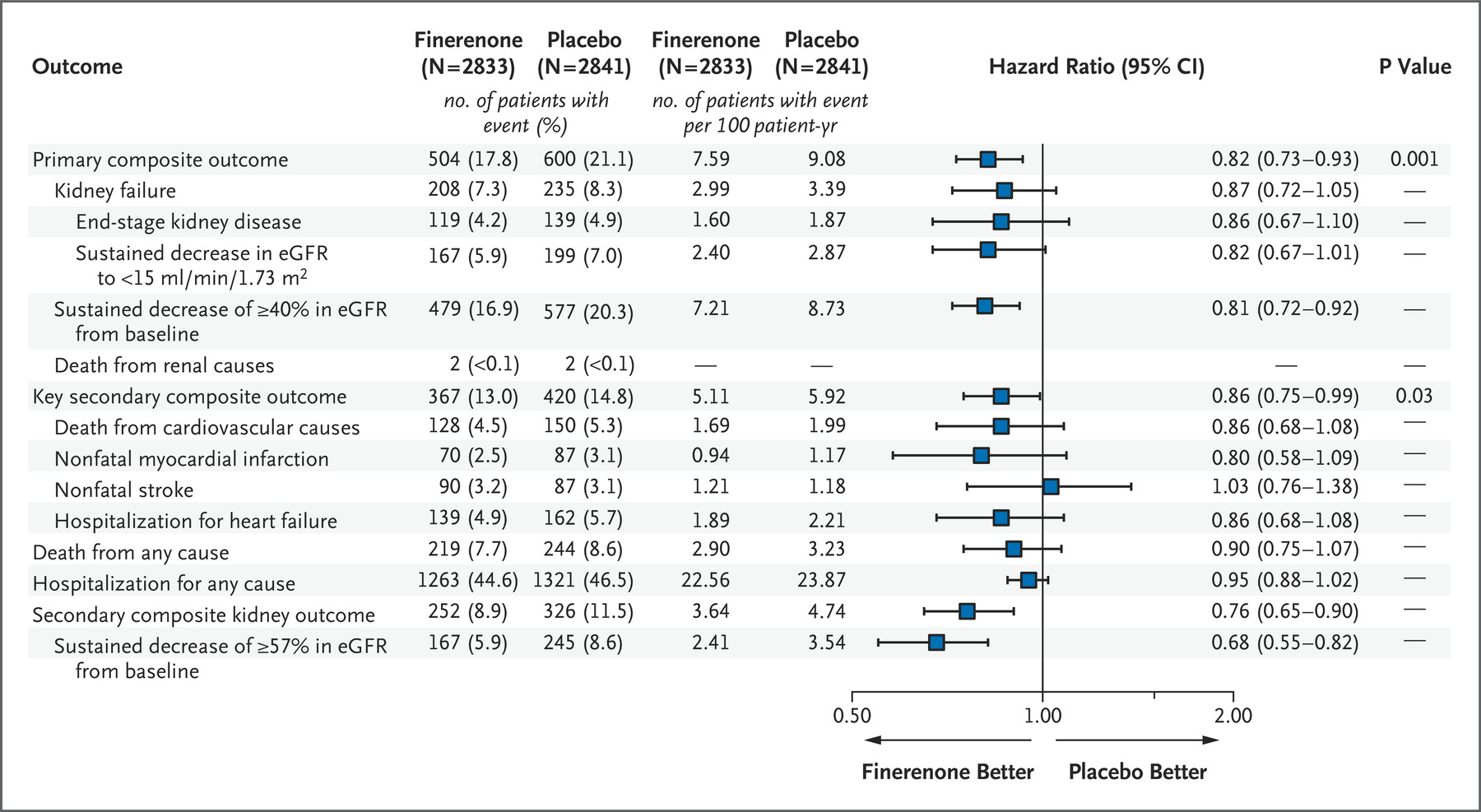
拜耳CKD药物Kerendia获得欧盟批准
拜耳近日宣布,欧盟监管机构已批准 Kerendia (finerenone) 用于治疗患有与 2 型糖尿病相关的慢性肾病(CKD)的成年患者。
MedSci原创 - 慢性肾病,慢性肾病患者,2 型糖尿病,Kerendia - 2022-02-28
拜耳,强生的Xarelto未能达到PhIII的目标
在静脉血栓栓塞和心力衰竭研究的两项研究中,拜耳和强生公司扩大血液稀释剂Xarelto应用范围的计划遭遇挫折。MARINER试验显示,Xarelto(利伐沙班)并未降低出院后急性医疗患者静脉血栓栓塞(VTE)或血栓和VTE相关死亡的复合终点。然而,该公司指出,该药物确实显着降低了VTE的安全性,增强了药物的正面利益风险。Janssen 研究与发展部心血管与代谢全球治疗领域负责人James List说
MedSci原创 - Xarelto,PhIII的目标 - 2018-08-28
拜耳肝癌治疗新药在华获批上市
3月18日是“全国爱肝日”,在当天召开的“中国肝癌领导力论坛”上,拜耳宣布口服多激酶抑制剂拜万戈(瑞戈非尼)肝癌适应症在华上市。拜万戈于2017年12月经国家食品药品监督管理总局(CFDA)优先审评批准用于既往接受过索拉非尼治疗的肝细胞癌(HCC)患者,是十年来在华首个获批并上市的肝癌治疗新药。这是继全球首个获批用于晚期肝癌系统治疗药物——多吉美之后,拜耳在肝癌治疗领域的又一重大突破,也是中国肝癌
中国科学报 - 肝癌,拜耳 - 2018-03-22
美国FDA授予拜耳靶向抗癌药Stivarga优先审查资格,二线治疗晚期肝细胞癌
德国制药巨头拜耳(Bayer)靶向抗癌药Stivarga(regorafenib,瑞戈非尼)近日在美国监管方面传来喜讯。美国食品和药物管理局(FDA)已授予Stivarga补充新药申请(sNDA)优先审查资格,该sNDA寻求批准Stivarga用于不可切除性肝细胞癌(HCC)患者的二线治疗。Stivarga是一种口服多激酶抑制剂,目前已获全球90多个国家批准治疗转移性结直肠癌(mCRC),并获
生物谷 - 拜耳,Stivarga,瑞戈非尼,结直肠癌 - 2017-01-05
拜耳制药新药Gadavist通过FDA批准
3月14日,美国食品药品管理局(FDA)批准Gadavist(钆布醇)——一个含钆的造影剂,用于患者中枢神经系统的磁共振成像(MRI)检查。据悉,Gadavist是FDA批准的用于中枢神经系统磁共振成像的第六个含钆造影剂(GBCAs),适用于两岁及以上的儿童和成人。Gadavist用于中枢神经系统MRI检查的对比增强成像,成像时可将大脑与血流分离,帮助检测和显现破坏细胞屏障的病变。此外,它还
MedSci原创 - FDA,Gadavist,拜耳 - 2012-04-14
拜耳抗癌药Xofigo获欧盟批准
拜耳(Bayer)11月15日宣布,抗癌药物Xofigo(radium 223 dichloride,镭223二氯)已获欧盟委员会(EC)批准,用于有症状骨转移(symptomatic bone metastases)及无已知内脏转移(no known visceral metastatic disease)的阉割性前列腺癌(CRPC)患者的治疗。Xofigo的获批,是基于关键性III期AL
生物谷 - 新药,FDA - 2013-11-20
为您找到相关结果约500个