总局发布了膀胱过度活动症药物临床试验指导原则
为指导和规范膀胱过度活动症药物临床试验,刚刚,食品药品监管总局发布了《膀胱过度活动症药物临床试验指导原则的通告(2017年第223号) 》。
CFDA官网 - 膀胱过度活动症,药物临床试验 - 2018-01-04
2016湖南省质子泵抑制剂的临床应用指导原则(试行)发布
质子泵抑制剂(proton pump inhibitor,PPI)是目前医院应用最为广泛的药物之一,我国有研究报道,PPI在医院消化系统用药约占75.5%的份额,PPI的用药频度呈快速上升趋势,尤其在外科领域使用量增长迅速伴随着PPI的长期、大量应用,以及应用人群的不断扩大,一些新的严重的不良反应逐步被发现。目前有关PPI的不良反应报道包括胃肠道症状、肝肾毒性、神经系统症状、内分泌
中南药学 - 质子泵抑制剂 - 2016-09-02
抗肿瘤新药可及性待提升,专家呼唤数据证据促临床应用
IQVIA联合财新健康点发布的《推动中国肿瘤价值医疗持续发展行业报告》显示,虽然抗肿瘤创新药上市加速,但仍存诸多挑战,精准医疗的应用对药物的准入机制提出了新的需求。专家呼吁推动医疗数据共享,为寻找高价值药物打造一把“尺子”。
健康点healthpoint - 抗肿瘤新药可及性,临床应用 - 2018-06-14
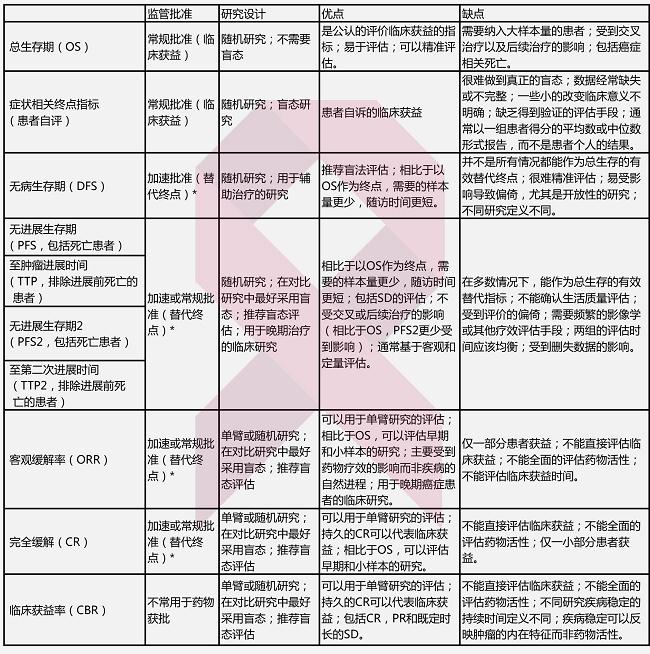
CFDA官网干货:抗肿瘤药物临床试验重要终点指标
美国FDA在公示抗肿瘤新药审批结果时,绕不开一系列的临床试验观察指标,如总生存期、无进展生存期、客观缓解率等,这些终点指标如何定义?作为研究终点各自有何差异?肿瘤资讯小编特整理CFDA官网的相关信息,带您了解抗肿瘤药物临床试验重要终点指标。
肿瘤资讯 - CFDA,抗肿瘤,药物,临床试验,终点指标 - 2017-08-30
中国原创抗肿瘤药物SNG1153获准美国临床试验
北京盛诺基医药科技有限公司近日收到美国食品药品监督管理局(FDA)通知,公司品种SNG1153获准在美国开展临床试验。SNG1153作为抗肿瘤药物开发,用于晚期癌症患者,是继阿可拉定之后公司又一具有完全自主知识产权的抗肿瘤创新药物。SNG1153是阿可拉定的化学合成衍生物,可以直接杀伤肿瘤,在体外实验观察到SNG1153可抑制肝癌、肺癌、黑色素瘤、多发性骨髓瘤等多种肿瘤细胞系的增殖,在动物实验中,
MedSci原创 - SNG1153,试验 - 2018-10-06
《以患者为中心的药物临床试验设计技术指导原则》(试行)解读
“以患者为中心”的药物研发是以患者的需求为出发点,让患者参与药物研发,该理念已经成为目前药物研发的核心指导思想,因此为了指导以患者为中心的临床试验设计, CDE于20
药融圈 - 临床试验,以患者为中心 - 2023-08-15
关于公开征求《药物临床试验适应性设计指导原则》意见的通知
为了促进药物临床试验各相关方对临床试验适应性设计的理解与合理应用,经广泛调研和讨论,我中心组织起草了《药物临床试验适应性设计指导原则(征求意见稿)》。
CDE - 临床试验,适应性设计 - 2020-05-15
国家药品审评中心发布药物非临床安全性研究技术指导原则
作为药审中心承担的十二五重大专项课题之法规科学的部分内容,2013年3月28日至29日,中心组织召开了药物非临床安全性研究技术指导原则合并修订/ 起草专题讨论会。按照工作计划,现公开征求意见,请广大药物研究相关人员提出意见和建议。 &
MedSci原创 - 药品审评中心,CDE - 2013-07-06
NMPA发布疫情期间药物临床试验管理指导原则征求意见稿
小编注:CDE发布了祖国版疫情期间临床试验管理指南征求意见稿,虽然略显迟些,但可以看到监管部门在应急管理方面的进步,该指南对于行业具有指导意义。该指南和EMA和FDA的指南中内容有很多相似之处,想必各
NMPA - 临床试验,指导原则 - 2020-05-05
CFDA拟推60天快速审批抗肿瘤创新药物临床研究申请
药物审批是所有医药开发者最为头痛的环节。而在中国,医药审批较为繁琐的过程也广为医药产业人士诟病。然而2015年来,中国医药相关部门的一系列举措似乎将要改变这一现象。最近,有消息人士透露中国CFDA正考虑以抗肿瘤药物为试点,推行临床试验新药(IND)60天内快速审批的政策。如果属实,中国将成为继新加坡、韩国之后第三个对临床早期研究进行快速审批的亚洲国家。
生物谷 - CFDA,审批 - 2015-09-01
为您找到相关结果约500个