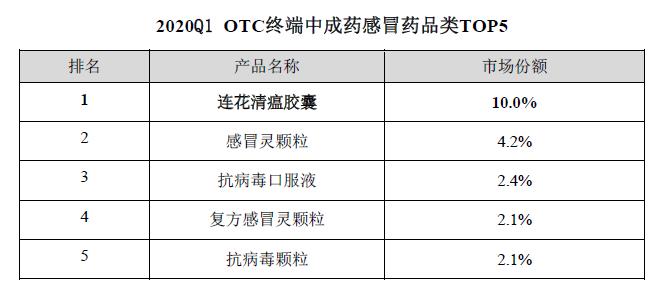
超20亿,连花清瘟上半年销售业绩公布
近日,以岭药业发布了2020年上半年销售业绩报告,其上半年取得营业收入44.87亿元,相较于去年同期实现了50.35%的增长,归属于上市公司股东的净利润7.14亿元,同比增长57.05%,超过去年全年
医谷网 - 连花清瘟 - 2020-09-23
FDA有关仿制药和抗肿瘤药说明书的2个指导原则介绍
详细介绍FDA参比制剂(RLD)说明书修订后简化新药申请(ANDA)说明书的修订,期望对中国RLD说明书修订后的仿制药说明书的修订以及联合用药方案中的抗肿瘤药的“交叉说明”的实施有帮助。
药物评价研究 - 仿制药 - 2023-06-20
罗氏抗流感病毒新药玛巴洛沙韦片上市申请纳入拟优先审评
CDE官网今日公示,罗氏进口化学创新药玛巴洛沙韦片(英文商品名:Xofluza)上市申请被纳入拟优先审评。
亿欧 - 优先审评,巴洛沙韦片,罗氏抗流感病毒 - 2020-11-05
药品审评审批信息公开办法征求意见:等效性试验数据应公开
1月16日,食药监总局发文公开征求《药品审评审批信息公开管理办法(征求意见稿)》意见,《办法》对药品神评审批受理、过程、结果等多个环节列出了信息公开要点。记者注意到,在受理环节,《办法》规定药审中心在受理药品注册申请后10个工作日内,应按照中药、化学药品和生物制品的分类,向社会公开注册申请品种的受理号、药品名称、受理日期等信息。
澎湃新闻 - 药品,审批,意见 - 2018-01-19
口服抗病毒疗法最新临床试验结果发布:对所有新冠变种有效
日前,Atea Pharmaceuticals在2021年第二季度财报中公布了该公司和罗氏(Roche)联合开发的口服抗病毒疗法AT-527的最新临床试验结果。目前正在进行的2期临床试验的中期分析显示
MedSci原创 - 药物治疗,新冠病毒 - 2021-08-16
FDA:审批了3款创新药获批,罕见病药物市场热潮涌动
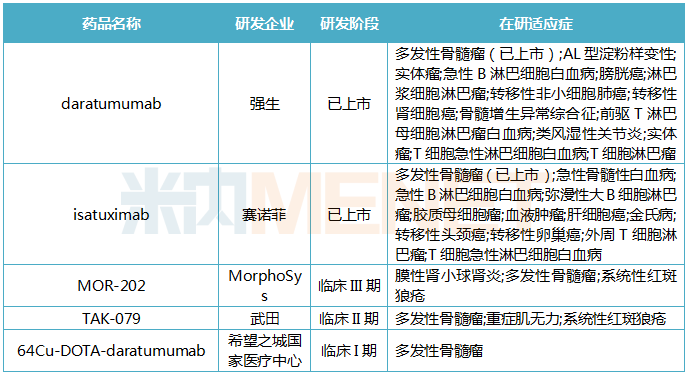
根据美国FDA官网公布的消息,2020年3月FDA批准3款创新药物,分别是赛诺菲公司的Sarclisa,Recordati公司的Isturisa,以及百时美施贵宝公司的Zeposia。2020年一季度
米内网 - 2020-04-04
GEN:2014华尔街生物医药股10大赢家
过去的2014年,是资本市场不平凡的一年,也是生物医药股勇攀高峰的一年。这一年,生物科技上升到了前所未有的高度,成为所有行业中最具投资价值的领域,生物医药股在这一年普遍表现非常出色并显著跑赢大盘。近日,国外著名网站GEN公布了2014年华尔街生物医药股十大赢家榜单。数据显示,2014年排进TOP10榜单的涨幅普遍比2013年要高。例如,2013年涨幅最高的一支股票(Insys The
GEN - 生物医药 - 2015-01-22
FDA 指南:人体处方药和生物制品--根据重量或可使用容器的体表面积对剂量进行标记--"剂量带"
本指南中的建议和例子与以下情况有关:申请人(1)提议为可注射药物产品开发具有各种不同长处的现成容器,以及(2)试图将剂量段幅信息纳入根据先前核准的药物产品的剂量信息而根据重量或BSA提供的处方信息。
FDA官网 - 生物制品,人体处方药 - 2023-10-08
2015获批上市新药哪些会成“重磅炸弹”?
2015年早些时候,汤森路透Cortellis竞争情报对“值得期待的药物”(Drugs To Watch)做出预测,预计2015年进入市场、有望成为“重磅炸弹”的药物超过2014年。2015年获批/上市药物中,2019年销售额预计超过10亿美元的共11种(2014年仅有3种)。而就目前情况看,除了预期所列药物外,还有其他几种2015年获批和(或)进入市场的药物有望在今后5年内跻身“重磅炸弹”药
汤森路透 - 汤森路透,新药 - 2016-01-07
详解2016年FDA批准的20款创新药(名称、活性成分、适应症……)
导读 12月14日,FDA公布了2016年批准的第20个新分子药物Eucrisa,而后朋友圈被“CDER新药办公室主任John K. Jenkins博士的FDA新药审评情况”一文刷屏了。到目前为止FDA仅批准20个新分子药物,远低于去年的45个。本文详细解析了这20款创新药物的名称、活性成分、适应症……截止至2016年12月14日,FDA下属药品审评与研究中心(CDER)共批准了20个创新药:包括
生物探索 - 2016年,FDA批准,20款创新药 - 2016-12-20
如何与FDA合作以取得临床试验的成功?
新药的开发,尤其是近年处于热潮的罕见疾病药物开发,临床开发阶段加强与监管机构的沟通必不可少。本文以Timber制药公司的案例,简要为大家介绍这家制药公司如何与FDA合作,以取得新药开发临床试验成功。
新药前沿 - FDA - 2022-03-27
2013年药物审批:制药业有理由乐观吗?
与制药商所秉承的漫长药品开发周期相比,仅仅以12个月的时间来洞察制药业是如何进展的只能是管中窥豹。然而,2013年批准的创新药物的评价确能为制药业关键的主题提供一些见解。从数字角度来说,2013年未能达到FDA于去年批准的39个新分子实体的数量。2013年批准27个新药更接近FDA最近的历史水平,也使得“2012年批准数量应被视为一个异常值,而非新药产出显著增长先兆”的说法得到进一步加强。无论正确
dxy - 药物审批,制药业有 - 2014-01-07
强生集团旗下杨森制药召开业务回顾大会 展现强劲创新医药产品线
不详 - 美通社 - 2017-05-23
为您找到相关结果约500个