最新临床试验专场试验揭晓
侯静波获CIT青年医师一等奖 刘健获CIT最具教育意义病例奖 昨日(3月16日)下午,第十届中国介入心脏病学大会(CIT)最新临床试验专场的四项研究在众人期待中揭晓,本报记者刘敏第一时间为您传递TRACK-D 与任何商业利益无关的TRACK-D研究通过大样本的前瞻性多中心随机对照试验纳入患者2998例。结果显示,瑞舒伐他汀可降低伴有慢性肾病2~3期的糖尿病患者对比
MedSci原创 - 临床试验 - 2012-03-23
手足口病中药临床试验设计与评价技术指南
《手足口病中药临床试验设计与评价技术指南》为中华中医药学会标准化项目《儿科系列常见病中药临床试验设计与评价技术指南》之一。
药物评价研究 - 手足口病,感染病病毒组 - 2022-01-22
小儿积滞中药临床试验设计与评价技术指南
《小儿积滞中药临床试验设计与评价技术指南》为中华中医药学会标准化项目《儿科系列常见病中药临床试验设计与评价技术指南》之一。其目的是以临床价值为导向,主要是在中医病证研究模式下,重点讨论具有病种、儿童和
药物评价研究 - 小儿积滞 - 2023-02-09
临床试验统计分析计划内容指南 2017
重要性:虽然存在有关临床试验统计原则的指南,但缺乏涵盖统计分析计划 (SAP) 所需内容以支持透明度和可重复性的指南。
JAMA. 2017;318(23):2337-2343 - 统计分析计划 - 2023-10-13
FDA 指导文件:行业临床试验指南中的多个终点
本指南为申办者和审评人员提供了 FDA 对研究结果分析和解释过程中多个终点所带来的问题的思考,以及如何在人用药物(包括作为生物制品获得许可的药物)的临床试验中管理这些问题。
FDA - 行业临床试验指南 - 2022-11-10
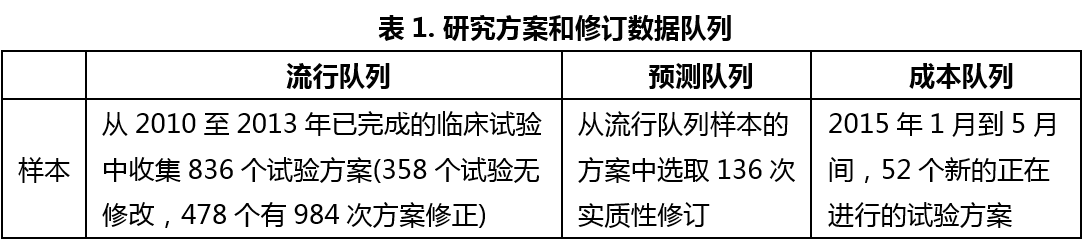
临床试验方案修订对临床试验结果和费用的影响
临床试验方案是保证临床试验顺利有序开展的前提,其一经制订并批准就应严格执行。在实际的临床试验开展过程中,有时对临床试验方案确有必要进行修订。但是,如果修订不够谨慎的话,就可能影响到试验结果、试验周期和试验经费。长期以来,对于制药公司和CRO公司而言,因临床试验方案的修订而导致的计划外的推迟、中断和花费都是很大的挑战。
国际药品检查动态研究 - 试验方案,修订 - 2019-12-26
COVID-19致临床试验受阻 FDA发布应对指南
3月18日,瑞士制药公司Addex Therapeutics宣布,受COVID-19影响已推迟Levodopa用于治疗帕金森氏病患者左旋多巴诱发的运动障碍的注册疗效和安全性研究(Study 301)启
网络 - 2020-03-19
临床试验用药品(试行)
根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,现发布《临床试验用药品(试行)》附录,作为《药品生产质量管理规范(2010年修订)》配套文件,自2022年7月1日起施行。
国家药品监督管理局官网 - 临床试验 - 2023-06-10
FDA指南:提交癌症临床试验中患者报告的结果数据
本文档提供了提交癌症临床试验中收集的患者报告结果(PRO)数据的技术规范,以支持肿瘤学医疗产品的营销申请,其中PRO是一种用于收集患者体验数据的临床结果评估(COA)。
FDA指南 - 癌症临床试验 - 2023-11-10
确证性临床试验中数据缺失的处理指南
1 前言 确 证性临床试验是在探索性临床试验基础上,通过开展多中心临床试验,进一步确证药物临床疗效,为获得上市许可获得充足证据。该阶段试验通常要求纳入较多的样 本例数,设计随机双盲对照试验,并在此基础上进行数据统计以客观评价新药疗效。然而,受各种因素影响,在确证性临床试验中出现数据缺失是不可避免的,例 如:患者拒绝继续研究、治疗失败/成功或出现不良事件导致退出试验、患者移居,以及观测指标
中国新药杂志 - 临床试验,数据缺失 - 2014-08-09
FDA行业指南:将老年人纳入癌症临床试验
本指南提供了有关将老年患者纳入癌症治疗药物临床试验的建议。就本指南而言,老年人是指 65 岁及以上的人。具体而言,本指南包括建议在癌症临床试验中充分代表老年人,以便更好地评估该人群中抗癌药物的效益-风
FDA - 癌症 - 2022-03-15
FDA工业指南:肿瘤临床试验中核心患者报告结局(草案)
本指南向申办者提供了收集癌症临床试验中患者报告的核心临床结果的建议,以及仪器选择和试验设计的相关考虑因素。尽管本指南侧重于患者报告的结果 (PRO) 措施,但其中一些建议可能与癌症临床试验中的其他临床
FDA - 患者报告结局 - 2022-03-16
为您找到相关结果约500个