百时美PD-1免疫疗法Opdivo斩获FDA第6个突破性药物资格——晚期膀胱癌
2016年5月中旬,肿瘤学巨头罗氏(Roche)肿瘤免疫疗法Tecentriq(atezolizumab)在美国监管方面实现重大里程碑,FDA提前4个月加速批准Tecentriq用于治疗最常见类型的膀胱癌——尿路上皮癌(UC),该药是FDA批准的首个PD-L1免疫疗法,同时也是获批治疗这类癌症的首个PD-1/PD-L1免疫疗法。此次批准对罗氏而言意义重大,一方面,这是该公司庞大的PD-L1临床项目
MedSci原创 - 百时美,PD-1免疫疗法,Opdivo,膀胱癌,尿路上皮癌 - 2016-06-28
FDA授予罗氏抗炎药Actemra/RoActemra第2个突破性药物资格,治疗巨细胞动脉炎(GCA)
FDA已授予Actemra/RoActemra治疗巨细胞动脉炎(GCA)的突破性药物资格(BTD),这也是该药在美国监管方面获得的第2个突破性药物资格,之前,FDA于2015年6月授予该药治疗系统性硬化症
生物谷 - 罗氏,Actemra,RoActemra,tocilizumab,托珠单抗,巨细胞动脉炎,突破性药物资格 - 2016-10-06
FDA授予RGX-181基因疗法孤儿药物资格以治疗2型神经元蜡样脂褐质沉积症
REGENXBIO是一家领先的临床阶段生物技术公司,近日,REGENXBIO宣布美国食品和药物管理局(FDA)已经将其基因疗法RGX-181认定为孤儿药,以治疗婴儿的晚期2型神经元蜡样脂褐质沉积症。
MedSci原创 - 神经元蜡样脂褐质沉积症,RGX-181,基因疗法 - 2018-11-15
FDA授予默沙东PD-1免疫疗法Keytruda第4个突破性药物资格:经典型霍奇金淋巴瘤(cHL)
本月中旬,FDA授予Keytruda治疗复发性或转移性头颈部鳞状细胞癌(HNSCC)的优先审查资格。如果不出意外,Keytruda将于今年8月26日获批治疗HNSCC适应症。
生物谷 - 默沙东,PD-1,免疫疗法 - 2016-04-21
诺华新一代IgE抗体ligelizumab获美国FDA突破性药物资格!
诺华(Novartis)近日宣布,美国食品和药物管理局(FDA)已授予ligelizumab(QGE031)突破性药物资格,用于治疗对H1抗组胺治疗应答不足的慢性自发性荨麻疹(CSU)患者。
生物谷 - 荨麻疹,慢性自发性荨麻疹 - 2021-01-16
FDA授予诺华新型抗癌药LEE011治疗HR+/HER2-乳腺癌的突破性药物资格(BTD)
美国食品和药物管理局(FDA)已授予LEE011突破性药物资格(BTD),联合来该公司激素疗法Femara(品牌名:弗隆,通用名:letrozole,来曲唑)用于激素受体阳性/人类表皮生长因子受体2阴性
生物谷 - 抗癌,乳腺癌,FDA - 2016-08-05
FDA授予罗氏抗癌药Alecensa第2个突破性药物资格,一线治疗ALK+NSCLC领域即将上演巅峰对决
美国食品和药物管理局(FDA)已授予口服靶向抗癌药Alecensa(alectinib)第2个突破性药物资格(BTD),用于之前未接受ALK抑制剂治疗的晚期间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌(NSCLCAlecensa是一种ALK抑制剂,之前,FDA于2013年首次授予该药突破性药物资格,用于既往
生物谷 - 罗氏,Alecensa,Alectinib,间变性淋巴瘤激酶,非小细胞肺癌,ALK,NSCLC - 2016-10-06
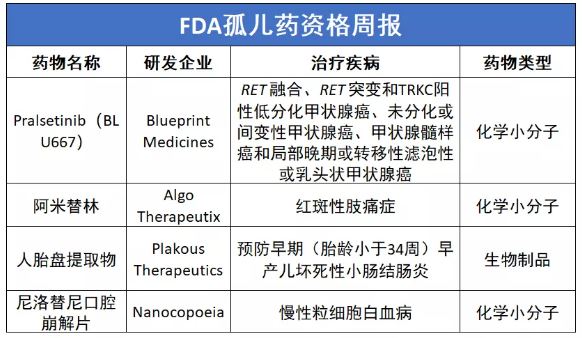
FDA:12项药物被认定为孤儿药资格
最近两周FDA共发出12项孤儿药资格,其中3款为治疗胃癌的在研创新疗法,包括安进(Amgen)公司开发的双特异性抗体。
药明康德 - FDA,孤儿药 - 2020-06-12
石药ADC药物获得FDA孤儿药资格认定
11月25日,石药集团发布公告称其自主研发的ADC药物(抗体-药物偶联物)SYSA1801用于治疗胃癌(包括胃食管交界处癌)的适应症获得FDA 孤儿药资格认定。
医药魔方 - 胃癌,孤儿药,石药计划 - 2020-12-04
世卫组织:生物相似性药物将接受资格审查
世界卫生组织近日发表声明表示,该组织今年将发布一项试点项目,对生物相似性药物资格进行预审,旨在让低收入和中等收入国家获得一些昂贵的癌症治疗方案。
科技日报 - 药物,审核 - 2017-05-08
EpiCept神经痛药物AmiKet获FDA快速审定资格
近日,EpiCept公司的AmiKet获得美国食品药监局(FDA)授予的快速审定资格,这是一种含有4%的阿米替林和2%的氯胺酮的药物。根据FDA的规定,获得快速审定资格的药物会获得有限审定权,比标准的审定时间要缩短大概一半。 EpiCept公司总裁兼首席执行官Jack Talley说:“我们希望通过这次
cyy123 - 新药,FDA - 2012-04-25
中科院中亚药物研发中心乌兹别克斯坦落成,聚焦药品植物资源
新华社塔什干11月24日电 中国科学院中亚药物研发中心落成仪式23日在乌兹别克斯坦首都塔什干举行。同一天,中国科学院大学中亚科教基地也在塔什干挂牌成立。中国科学院院长白春礼说,该中心将成为中乌两国科技和教育合作的重要平台,在中亚地区药品植物资源的研究和可持续发展领域的科研交流、资源共享和人才培养方面发挥积极作用,也将促进中国与“一带一路”沿线国家科技合作
新华社 - 中科院,中亚药物,研发中心 - 2018-11-25
《药物临床试验机构资格认定检查公告》发布:5家中医医疗机构获临床试验资格
国家药品监督管理局发布《药物临床试验机构资格认定检查公告》,认定北京中医药大学第三附属医院等87家医疗机构具有药物临床试验机构资格,发给《药物临床试验机构资格认定证书》。
中国中医 - 药物临床试验机构,资格认定,中医医疗机构,临床试验资格 - 2018-07-21
FDA使用组织病理学及其相关方法来支持行业生物标志物资格指南的注意事项
本指南旨在帮助生物标志物2的提交者进行资格鉴定,以进行组织学作为参考或真相标准的非临床研究(Zhou等,2011)。 在这些研究中,对与组织病理学变化相关的生物标志物性能进行科学严格的评估是至关重要的
FDA - 生物标志物 - 2020-11-16
FDA授予原发性胆汁性肝硬化治疗药物OCA优先审查资格
去年8月,全球医药市场预测机构EvaluatePharma发布《全球生物制药后期管线重磅药物TOP 15》榜单,有多个制药巨头的在研药物均成功上榜,其中百时美施贵宝和默沙东凭借各自的PD-1免疫疗法Opdivo和Keytruda分别夺得状元和榜眼,而夺得探花的药物obeticholic acid (OCA,一种鹅脱氧胆酸衍生物)竟然来自于一家名不见经传的美国小生物制药公司——Intercept P
不详 - FDA,肝硬化,OCA - 2015-09-01
为您找到相关结果约500个