NMPA:安进公司地舒单抗在国内有条件获批
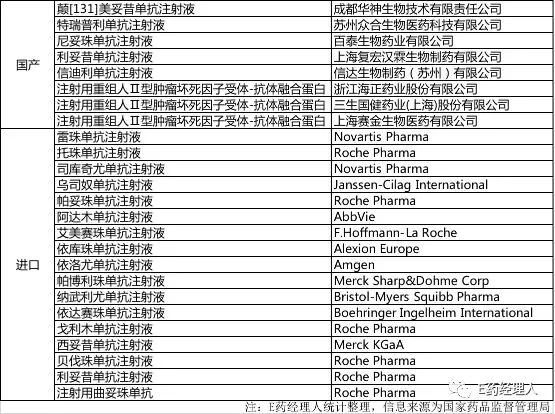
国家药品监督管理局官方发布消息显示,安进公司(AMGN.US)开发的地舒单抗注射液的进口注册申请目前已在国内有条件获批。这也意味着,目前国内上市的单抗类产品总数已达到26个。而第一批临床急需境外新药名
安进 - 地舒单抗,安进 - 2020-06-09
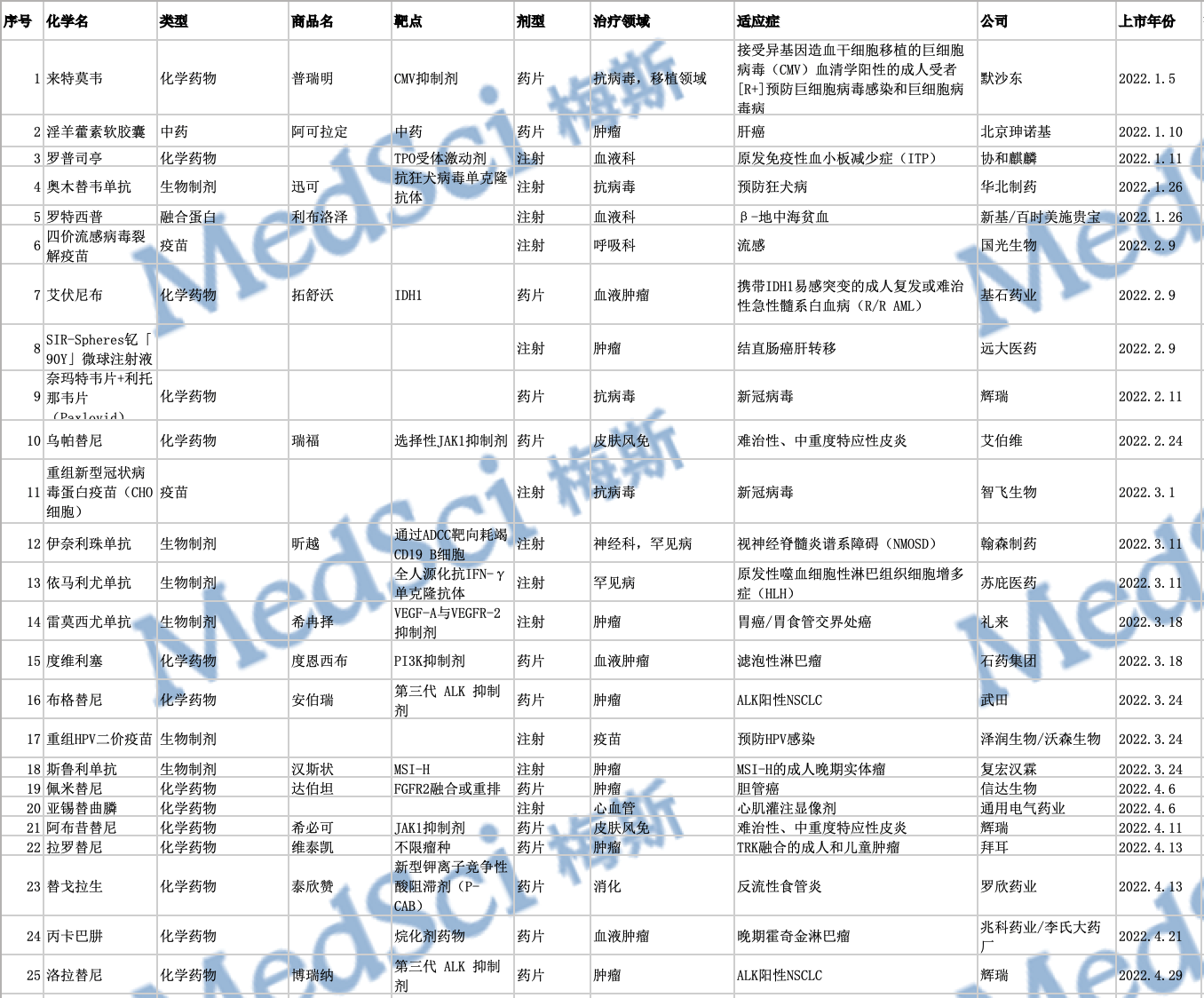
2022年中国NMPA批准上市的50款创新药物
2022年,中国药监局(NMPA)共批准了50款新药,其中进口新药有30款,国产新药有20款。从药物类型上看,包括28款化学药、13款生物药、5款疫苗以及4款中药。数量与2019年批准了51款新药,2
MedSci原创 - 创新药物,NMPA - 2023-01-13
不受制NMPA加速创新审评,药审、械审大湾区分中心挂牌成立
国家药品监督管理局(NMPA)药品审评检查大湾区分中心、医疗器械技术审评检查大湾区分中心正式挂牌。
亿欧 - NMPA,创新审评,挂牌成立 - 2021-01-11
中国NMPA授予Omadacycline优先审查:治疗社区获得性细菌性肺炎(CABP)等
中国创新型生物制药公司再鼎医药今日宣布,中国国家药品监督管理局(NMPA)药物评审中心已将Omadacycline的新药申请(NDA)授予了优先审查地位。
MedSci原创 - Omadacycline,社区获得性细菌性肺炎,NMPA授予优先审查 - 2020-05-07
卫材Halaven获NMPA批准 用于治疗局部晚期或转移性乳腺癌
卫材今天宣布,中国药品监督管理局(NMPA)已批准其内部开发的新型抗癌药Halaven(eribulin mesylate,甲磺酸艾瑞布林),用于既往已接受过至少两种化疗方案(包括蒽环素和紫杉烷)的局部晚期或转移性乳腺癌患者
新浪医药新闻 - 乳腺癌 - 2019-07-18
康希诺重组新型冠状病毒疫苗获NMPA附条件批准上市
2月25日,国家药品监督管理局附条件批准康希诺生物股份公司重组新型冠状病毒疫苗(5型腺病毒载体)注册申请。该疫苗是首家获批的国产腺病毒载体新冠病毒疫苗,适用于预防由新型冠状病毒感染引起的疾病(COVI
医药魔方 - 新型冠状病毒 - 2021-02-26
NMPA关于仿制药一致性评价的52个细节答疑
1. 在1622个品种里面,如何再次申报问题:答:临床生产和研制现场核查在本次一致性评价没有进行单独制定规则,规则一直是在注册生产现场检查、研制现场和临床核查里面使用的,所以执行标准应当是一个标准,不存在新标准和旧标准的问题,标准是一样的。2. 参比制剂的寻找:答:自制产品为胶囊,但参比为片剂,是否可行?这种改剂型的品种还需进一步研究。3. 处方工艺、包装是否必须与原研一致:答:任何讲解中都没
MedSci原创 - 仿制药,一致性评价 - 2018-11-01
百济神州宣布NMPA接受zanubrutinib新药上市申请及关键性研究数据
公司今天宣布,中国国家药品监督管理局(NMPA)已受理zanubrutinib,一款在研布鲁顿氏酪氨酸激酶(BTK)抑制剂,作为针对复发/难治性(R/R)慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(
美通社 - 百济神州,新药上市申请 - 2018-10-25
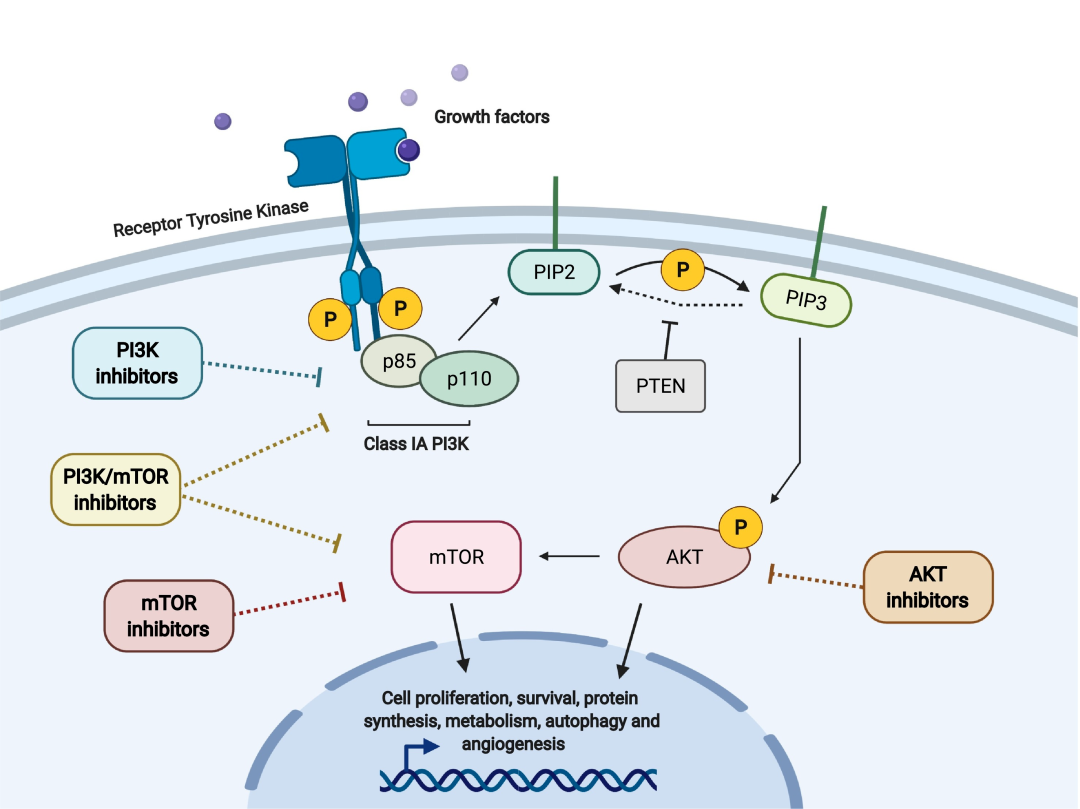
NMPA受理首个AKT靶点药物Capivasertib!乳腺癌患者治疗迎来新曙光
2023年10月10日,阿斯利康的Capivasertib片获NMPA上市受理。Capivasertib是一款靶向三种AKT亚型(AKT1/2/3)的高效选择性抑制剂,能阻止癌细胞用于分裂和生长的信号
梅斯肿瘤新前沿 - 乳腺癌,氟维司群,capivasertib - 2023-10-14
中国NMPA接受Envafolimab(KN035)治疗MSI-H / dMMR晚期实体瘤的NDA
生物制药公司TRACON今天宣布,中国国家药品监督管理局(NMPA)已经接受Envafolimab(KN035)治疗MSI-H / dMMR晚期实体瘤的新药申请(NDA)。
MedSci原创 - NMPA,Envafolimab(KN035),MSI-H / dMMR晚期实体瘤 - 2020-12-31
新型乳腺癌化疗药物艾立布林获NMPA批准上市
卫材株式会社(总部位于日本东京,现任社长为内藤晴夫,以下简称“卫材”)宣布,中国国家药品监督管理局已批准卫材原研抗癌药甲磺酸艾立布林(海乐卫®)上市,用于治疗既往接受过至少两种化疗方案(包括蒽环类和紫杉类)治疗的局部复发或转移性乳腺癌患者。该批准基于3041研究的结果,一项多中心、开放性、随机、平行对照的III期临床研究,旨在评价艾立布林和长春瑞滨对530例局部复发或转移性乳腺癌女性患者的疗效
卫材株式会社 - 乳腺癌,艾立布林 - 2019-11-27
HBM9161针对Graves眼病的临床试验获NMPA批件
和铂医药公司针对新生儿Fc受体(FcRn)的全人源抗体HBM9161再获中国国家药品监督管理局(NMPA)批准,拟对Graves眼疾(又称甲状腺相关眼病)开展临床试验。这是HBM9161在中国获得的第
和铂医药 - Graves眼病,和铂医药,HBM9161 - 2020-06-03
NMPA发布疫情期间药物临床试验管理指导原则征求意见稿
小编注:CDE发布了祖国版疫情期间临床试验管理指南征求意见稿,虽然略显迟些,但可以看到监管部门在应急管理方面的进步,该指南对于行业具有指导意义。该指南和EMA和FDA的指南中内容有很多相似之处,想必各
NMPA - 临床试验,指导原则 - 2020-05-05
为您找到相关结果约500个