2017上半年FDA批准的新药
2017上半年FDA共批准23个新药,包括16个新分子实体和7个新生物制品。这个数字已经超过2016年全年批准的新药数量总和。近20年来批准新药数量最多的年份是2015年的45个,上半年批准了14个新药。如果按此趋势持续下去,2017年批准的新药数量将创下历史新高。
新浪医药 - FDA,新药 - 2017-06-28
康希诺重组新型冠状病毒疫苗获NMPA附条件批准上市
2月25日,国家药品监督管理局附条件批准康希诺生物股份公司重组新型冠状病毒疫苗(5型腺病毒载体)注册申请。该疫苗是首家获批的国产腺病毒载体新冠病毒疫苗,适用于预防由新型冠状病毒感染引起的疾病(COVI
医药魔方 - 新型冠状病毒 - 2021-02-26
NMPA:多发性硬化的S1P靶向治疗药物西尼莫德批准上市
国家药品监督管理局通过优先审评审批程序批准Novartis Pharma AG(诺华制药)申报的1类创新药西尼莫德片(siponimod)(商品名:万立能)上市,用于治疗
MedSci原创 - 多发性硬化,西尼莫德 - 2020-05-14
美国FDA批准首个干眼症新药
Shire公司宣布美国FDA已经批准其新药Xiidra滴眼剂溶液(5%浓度的lifitegrast眼用溶液)上市,每日使用两次,治疗成人干眼症患者。目前,Xiidra是唯一一款可同时改善干眼症症状和体征的处方滴眼剂。Shire希望在2016年第三季度把Xiidra推入美国市场。干眼症是一种与眼球表面以及眼泪分泌相关的多因素疾病,表现为泪液质、量异常或动力学异常,并伴有如眼睛干涩、整体眼部
生物谷 - FDA,干眼症,新药 - 2016-07-13
五种新药获欧盟批准
五种新药获得欧盟批准,其中包括两种针对罕见疾病的孤儿药。首先,欧洲药品管理局人用药品委员会(CHMP)批准AMMTeK的Amglidia(格列本脲)用于治疗新生儿,婴儿和儿童中的新生儿糖尿病。新生儿糖尿病是在生命的头六个月中诊断出的极其罕见的糖尿病。由于高血糖水平和酮症酸中毒风险引起的症状会危及生命和衰弱。Amglidia是专为儿科使用开发的糖尿病药物格列本脲的一种新口服制剂,如果EMA遵循CHM
MedSci原创 - 新药,欧盟批准 - 2018-02-27
2013年FDA批准的27个新药汇总
今年FDA批准的新药数量上少于去年,但质量上却高于去年,其中10个有重磅潜力。 1. Nesina:苯甲酸阿格列汀片 阿格列汀(alogliptin)是Takeda研发的新型DPP-4抑制剂,用于治疗II型糖尿病,已获得FDA批准的同类药物还有西他列汀(sitagliptin)、沙格列汀
scifans - FDA,2013,27个新药 - 2013-12-26
卫材Halaven获NMPA批准 用于治疗局部晚期或转移性乳腺癌
卫材今天宣布,中国药品监督管理局(NMPA)已批准其内部开发的新型抗癌药Halaven(eribulin mesylate,甲磺酸艾瑞布林),用于既往已接受过至少两种化疗方案(包括蒽环素和紫杉烷)的局部晚期或转移性乳腺癌患者此次批准基于Study 304研究的结果。这是一项在中国开展的多中心、开放标签、随机、平行组III期研究,共入组了530例局部复发或转移性乳腺癌女性患者,这些患者之前接受过至
新浪医药新闻 - 乳腺癌 - 2019-07-18
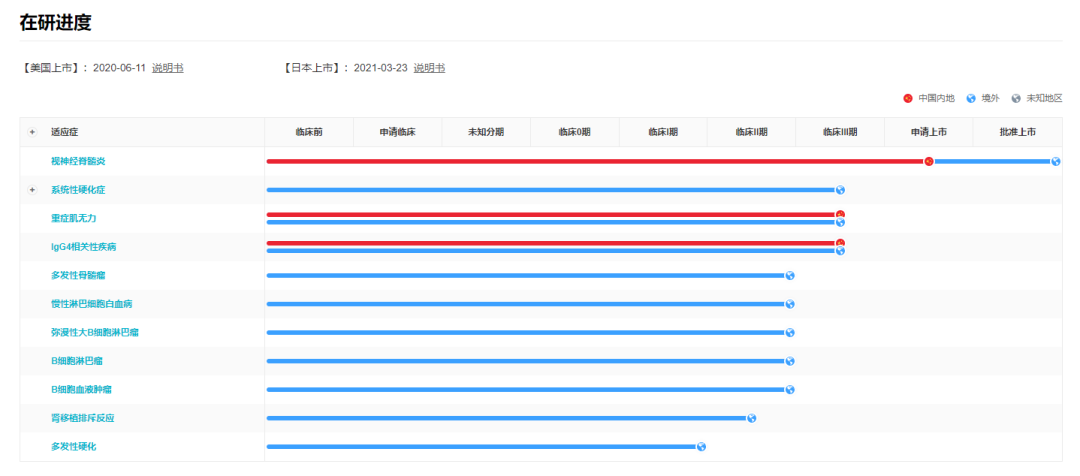
NMPA批准Uplizna(伊奈利珠单抗)治疗视神经脊髓炎谱系疾病(NMOSD)
2022年03月11日,中国国家药监局(NMPA)官网最新公示, 抗CD19单克隆抗体伊奈利珠单抗(inebilizumab)获批上市用于治疗视神经脊髓炎谱系疾病(NMOSD)患者。
网络 - 视神经脊髓炎谱系疾病 - 2022-03-14
百济神州宣布NMPA接受zanubrutinib新药上市申请及关键性研究数据
百济神州(纳斯达克代码: BGNE;港交所代码:06160),是一家处于商业阶段的生物医药公司,专注于用于癌症治疗的创新型分子靶向和肿瘤免疫药物的开发和商业化。公司今天宣布,中国国家药品监督管理局(NMPA)已受理zanubrutinib,一款在研布鲁顿氏酪氨酸激酶(BTK)抑制剂,作为针对复发/难治性(R/R)慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)患者潜在疗法的新药上市申请
美通社 - 百济神州,新药上市申请 - 2018-10-25
NMPA批准针对痴呆症的18F-APN-1607 Tau PET成像示踪剂的III期临床试验
中国国家药品监督管理局(NMPA)已批准启动III期临床试验,以评估APRINOIA的正电子发射断层扫描(PET)成像示踪剂18F-APN-1607。
MedSci原创 - tau蛋白,痴呆症,NMPA,18F-APN-1607 - 2020-10-29
信达生物的利妥昔单抗注射液HALPRYZA,获NMPA批准治疗恶性淋巴瘤
信达生物宣布其与礼来共同开发的重组人/鼠嵌合单克隆抗体HALPRYZA(利妥昔单抗注射液)获得中国国家药品监督管理局(NMPA)的正式批准上市。
MedSci原创 - 非霍奇金淋巴瘤,信达生物,HALPRYZA(利妥昔单抗注射液) - 2020-10-10
信达生物和礼来合作的双特异性抗体临床试验获NMPA批准
信达生物制药上周宣布其双特异性抗体(研发代号:IBI318),已于近期获得国家药品监督管理局(NMPA)颁发的药物临床试验批件,拟开展针对血液肿瘤和晚期实体瘤的临床研究。
GBIHealth - 信达生物,礼来,获批 - 2019-02-11
2012财年FDA共批准的35个新药
2012财年(2011年10月1日-2012年9月30日),FDA共批准了35个新药,和去年持平【FDA:2011财政年度批准的创新性新药】。其中,12个是优先药物,23个是常规药物[列表]。77%的药物是首轮评审即获批,75%的药物在美国得到第一个审核。这些新药中包括10个癌症药物,首个脐带血来源药物Hemacord,以及十年来首次获批的两个减肥药物:Qsymia 和Lorcaseri
MedSci原创 - FDA,新药 - 2012-12-09
FDA最新批准的呼吸道新药盘点
2011年8月至2012年3月期间FDA批准的呼吸科新药盘点: XALKORI:治疗ALK阳性的局部晚期或转移的非小细胞肺癌 (NSCLC) XALKORI (通用名:crizotinib capsule,克里唑蒂尼胶囊) 2011年8月26日,辉瑞公司的XALKORI?(crizotinib)胶囊获得美国食品药品管理局(FDA)批准,这是第一个对间变性淋巴瘤激酶 (ALK)进行靶向治疗的药
MedSci原创 - 呼吸,FDA - 2012-03-12
FDA批准治疗热带疾病新药
FDA日前批准Impavido(米替福斯)治疗热带病利什曼病(leishmaniasis),该病是苍蝇叮咬引起,由寄生虫传染给人类。Impavido由加拿大Paladin公司生产,被批准用于治疗3种主要类型利什曼病。 Impavido获得FDA快速审批,优先审查和罕用药资格认定。
医药经济报 - 新药,FDA - 2014-04-04
为您找到相关结果约500个