CDE新增14条常见一般性技术问题解答:化学药品仿制药能否直接申报上市许可申请?
CDE官网更新了“常见一般性技术问题解答”,新增了14条,目前常见一般性技术问题解答共计114条,以下为此次新增的解答。
医谷网 - 化学药品,上市许可,问题解答 - 2020-12-05
眼科LHON病基因疗法LUMEVOQ两年营收近千万欧元,治疗4年后,视力显著改善
基因治疗在眼科领域的需求可期。疫情期间,一款眼科基因疗法LUMEVOQ 在法国临时使用授权下,两年卖了970万欧元,研究结果显示,LUMEVOQ治疗4年后,视力显著改善。
生物药大时代 - 基因治疗 - 2022-02-02
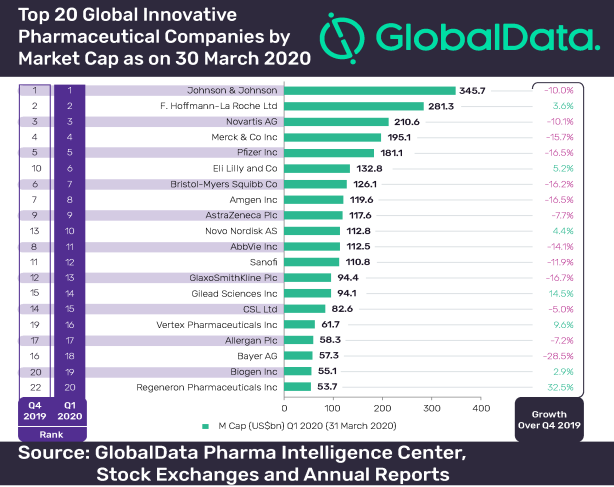
2020 Q1各大药企收入排名,强生,罗氏,诺华,默沙东,辉瑞,礼来,阿斯利康......
4月份,强生,礼来,GSK,辉瑞、诺华、默沙东相继发布了2020年第一季度财报。在疫情的笼罩之下,今年注定是不平凡的一年。而对于跨国药企而言,其开年业绩就上演了“王座更迭”的戏
MedSci原创 - 辉瑞,罗氏,药企,阿斯利康,强生,诺华 - 2020-05-03
礼来公司发布2021年第二季度财报
与2021年第一季度相比,礼来加快了全球最新药物的使用,实现了连续增长。
MedSci原创 - 心衰,新药,阿尔茨海默病,礼来,新冠抗体,新冠变异体 - 2021-08-05
欧盟批准诺华的IL-17单抗Cosentyx,用于治疗非放射线轴性脊柱关节炎
此次批准使Cosentyx(secukinumab)成为首个获准用于非放射线轴性脊椎关节炎的全人源IL-17A单抗。
MedSci原创 - 非放射线轴性脊柱关节炎,IL-17单抗Cosentyx - 2020-05-01
CD47单克隆抗体初露锋芒!天镜生物多项研发管线产品齐头并进
2020年11月,天境生物被《麻省理工科技评论》评选为“50家最聪明的公司”之一。
MedSci原创 - 美国FDA,艾伯维,CD38单抗 - 2021-04-09
医改40年巡礼:药审改革为患者用上新药好药持续发力
改革开放以来,伴随着从“富起来”到“强起来”的前进脚步,人民群众的用药水平也实现了从“有药治病”到“尽快用上新药好药”的历史性转变。党的十八大以来,人民群众用得上、用得起新药好药的获得感快速提升。
中国医药报 - 药审改革,新药好药 - 2018-11-30
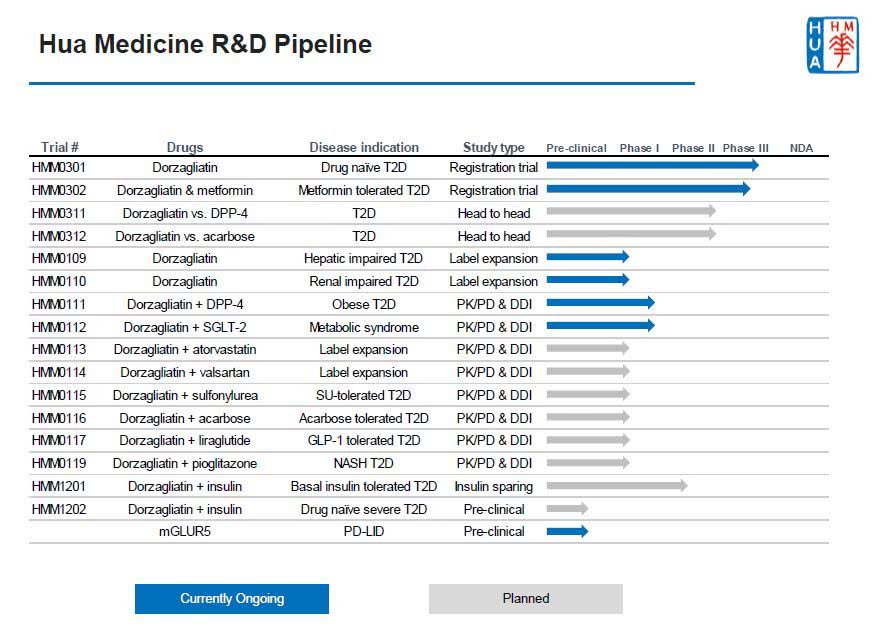
中国糖尿病创新药Dorzagliatin达到3期临床主要疗效终点,可降低HbA1c 1.07%
Dorzagliatin是基于葡萄糖激酶(glucokinase,GK) 作为血糖传感器,在血糖稳态调控中发挥核心作用的全球领先科学概念而开发。通过修复成年2型糖尿病患者下降的GK功能,重塑血糖稳态,而实现治疗2型糖尿病。Dorzagliatin分子结构式(图片来源:durgbank.ca) 华领医药在中国同时开展2项52周的3期注册临床研究,此次公布的是在从未接受过糖尿病药物治疗的
华领 - 糖尿病,Dorzagliatin - 2019-11-12
阿斯利康的心力衰竭药物SGLT2抑制剂Farxiga获得FDA优先审查
阿斯利康的心力衰竭药物SGLT2抑制剂Farxiga已获得美国FDA的优先审查,预计将在2020年第二季度获得批准。
MedSci原创 - 阿斯利康,心力衰竭,SGLT2抑制剂,Farxiga,FDA优先审查 - 2020-01-06
CFDA最新发布:药品注册流程新规则
食品药品监管总局关于进一步规范药品注册受理工作的通知 食药监药化管〔2015〕122号 2015年07月30日 发布 各省、自治区、直辖市食品药品监督管理局: 为进一步规范药品注册受理工作,现印发《药品注册形式审查补充要求》(见附件),请遵照执行,并将有关要求通知如下: 一、各省级局应严格按照《药品注册管理办法》及相关规定,在5个工作日内完成对申报资料的形式审查,一次性告
CFDA - CFDA,药品注册,新流程 - 2015-08-17
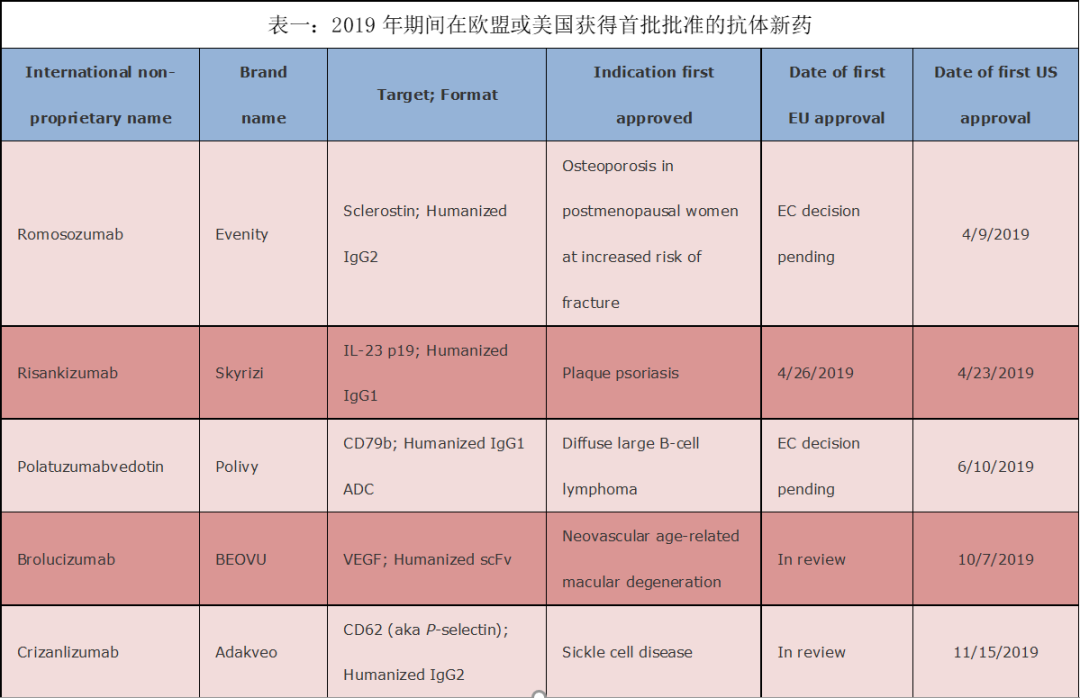
展望2020:抗体药物
感染或疾病的预防和治疗剂的开发是一个缓慢、昂贵的过程,需要在广泛的领域拥有丰富的知识和专长,包括相关的生物途径、药物分子的产生和表征、制造、临床研究和监管事务。据2020年美国或欧盟的首次批准药物来看,形成了将重点放在新型单克隆抗体的首次转变,以此作为创新和成功的衡量标准。截稿为止,美国或欧盟共批准了包括2019年12月获批的enfortumab vedotin-ejfv (Padcev)6种新型
生物制品圈 - 抗体,药物 - 2020-01-01
强生集团旗下杨森制药召开业务回顾大会 展现强劲创新医药产品线
不详 - 美通社 - 2017-05-23
肝药物获批上市 艾伯维开始逆袭
对于全球1.8亿丙肝患者来说,2014年12月19日有一则消息值得庆贺:美国FDA批准药物 Viekira Pak用于治疗一型丙肝治疗,包括有肝硬化的患者。这结束了此前吉利德旗下Harvoni独占丙肝市场的格局。 这一则以《颤抖吧!吉利德》为题的新闻,在短短一天内迅速覆盖了中国的社交网站。
中国财经网 - 肝药,艾伯维 - 2015-01-06
Camurus宣布FDA批准优先审核关于CAM2038丁丙诺啡注射液的新药申请
美通社 - 2017-09-22
FDA指南:以电子格式提交——上市后安全报告
本指南是一系列指导文件中的一份,旨在帮助行业以电子格式向 FDA 药物评价与研究中心 (CDER) 和生物制品评价与研究中心 (CBER) 提交某些监管文件。本指南根据以下规定提供了关于以电子方式提交
FDA - 上市后安全报告 - 2022-08-06
为您找到相关结果约500个