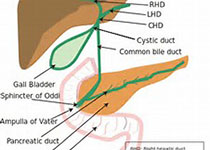
2018 日本指南:急性胆管炎和胆囊炎的抗生素治疗
2018年1月,日本肝胆胰腺外科学会(JSHBPS)更新发布了急性胆管炎和胆囊炎的抗生素治疗指南,抗生素治疗是急性胆管炎和急性胆囊炎患者的主要治疗措施,本文主要针对社区获得性和医院获得性感染合理应用抗生素治疗提供指导建议
J Hepatobiliary Panc - 急性胆管炎,胆囊炎,抗生素治疗 - 2018-01-21
J INTERN MED:房颤患者抗凝治疗,哪些因素与抗凝药物的选择有关?
由此可见,服用阿哌沙班的房颤患者卒中风险评分要高于服用VKAs的患者。有趣的是,对于服用达比加群的人群可以观察到相反的结果。
MedSci原创 - AF,抗凝,NOACs,VKAs - 2017-05-30
抗高血压药的用药禁忌
高血压病是中老年人常见的一种慢性疾病,除了改善患者的饮食习惯及生活方式外,应使用抗高血压药物进行长期或终生治疗。抗高血压药物种类较多,如应用不当不仅达不到治疗目的,更有可能引起多种副作用或不良反应。
上海药讯 - 高血压,药物,用药禁忌 - 2017-09-19
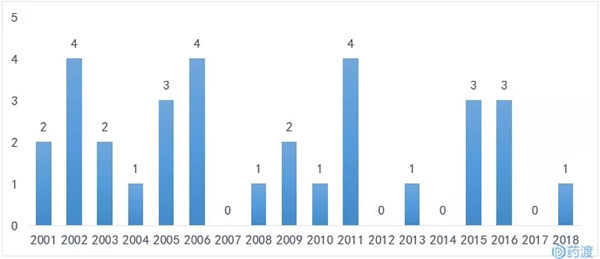
中国生物创新药发展现状
1.中国已上市药物生物药分析根据CFDA官方和药渡数据库显示,从2001年开始,截止至2018年8月,目前CFDA一共批准了32个中国1类生物新药(具体见表1:中国1类生物药批准情况)。
药渡 - 生物药 - 2018-11-01
羟氯喹的抗GBM肾炎治疗潜力
抗肾小球基底膜(抗GBM)肾炎,是由抗GBM抗体引起的自身免疫系统疾病,典型的临床表现为急进性肾小球肾炎,可伴有肺出血。在免疫学上,抗GBM肾炎患者血清学分析抗GBM抗体呈阳性,免疫组化肾小球膜上可见
网络 - 2023-01-31
急性胰腺炎诊治指南(2014)
中华医学会外科学分会胰腺外科学组于2000 年制定了我国《重症急性胰腺炎诊治草案》,在2004 年召开的第十届全国胰腺外科学术研讨会上,重点讨论了该草案的增补和修订内容,2006 年更名为《重症急性胰腺炎诊治指南自该指南发布以来,急性胰腺炎(acute pancreatitis,AP)的规范化诊治取得
中国实用外科杂志.2015,35(1):4-7. - 胰腺炎 - 2015-01-01
抗甲状腺药物的探索与突破
甲状腺功能亢进(简称“甲亢”)是内分泌科第二常见疾病,影响着全球约2%的女性和0.2%的男性健康。一项流行病学调查表明,中国甲亢总发病率为3%,其中女性为4.1%,男性为1.6%。中华医学会内分泌学分会甲状腺学组2010年组织的中国十城市甲状腺流行病学调查结果显示,我国十城市人群的甲亢患病率为3.7%。2013年国际甲状腺知识宣传周新闻发布会上数据显示,目前我国约有超过1500万的甲亢患者。面对如
中国医学论坛报 - 抗甲状腺,药物 - 2014-04-03
NEJM:新一代抗疟药物KAE609显示出强大的抗疟活性
实验性抗疟疾药物--螺旋吲哚酮类似物KAE609(cipargamin)一项概念验证临床试验的积极数据,有21例感染了恶性疟原虫 (P.falciparum)或间日疟原虫(P.vivax)但无并发症的疟疾患者参与了该项研究
MedSci原创 - 疟疾,cipargamin - 2014-08-01
印度斥巨资研制抗HIV疫苗
8月13日,印度启动了一间斥资1200万美元、由政府支持的实验室,其目标在于研制一种新的抗艾滋病病毒(HIV)疫苗。计划招募约30位科学家的HIV疫苗转化研究实验室隶属于转化健康科学与技术研究所,后者是一家正在新德里郊区建设的拥有2亿美元设备的机构。该实验室将同位于美国纽约市的国际艾滋病(AIDS)疫苗促进会(IAVI)展开合作,而运营成本则由两家均摊。 印度卫生部
中国科学报 - 印度,抗HIV疫苗 - 2012-08-17
2019 EFSUMB意见书:急性阑尾炎和憩室炎患者胃肠超声检查建议
2019年1月,欧洲生物医学超声学会联盟(EFSUMB,)发布了急性阑尾炎和憩室炎患者胃肠超声检查建议声明。全文共针对急性阑尾炎和憩室炎患者胃肠超声检查的相关内容形成了21条声明建议。
Ultraschall Med. 2019 Jan 7. - 急性阑尾炎,憩室炎,胃肠超声检查 - 2019-01-17
中药新药研发需降低政策风险
中药新药审批难的问题近年来显得日益突出。北京市中药研究所科研项目部主任战嘉怡表示,进行一个新药研发,首先要考虑几方面要素,包括立项可行性、审评通过率、临床利用率、市场前景性,而研发周期长、技术风险大、政策风险逐年提高等是新药审批遭遇的几大拦路虎从药品研发到推向市场至少十年 中药新药审批难的问题在近年来显得突出,有数据显示,新药研发申请中能拿到临床研究批件的几率很低,而这些获得临床批件的申请
不详 - 中药,新药,研发 - 2014-06-26
聚焦“重大新药创制”,聚焦武汉
“重大新药创制”科技重大专项双特异性抗体药物专题研讨会将于2018年5月26日在武汉光谷国际会展中心三楼小会议厅1举行。此次会议得到国家“重大新药创制”科技重大专项管理办公室支持,由中国药学会生物药品与质量研究专业委员会、武汉国家生物产业基地管理办公室联合主办,由武汉友芝友生物制药有限公司、武汉东湖国家自主创新示范区生物医药行业协会承办
medscizl - 2018-05-31
III期临床:新药研发的“麦城”
一个新药从开始研发到应用于临床需要一二十年时间,而III期临床试验十分耗时,一般需要3年以上的时间,同时也相当“烧钱”,通常会花费3亿~5亿美元。 今年,新药研发临床试验失败的比例再度提升。美国食品与药品监督局(FDA)审批数据显示,仅2014年上半年就有10个以上新药研发品种在Ⅲ期临床试验失败。那么,新药研发为什么难过III期临床试验呢?“通常,新药研发最终要经过药物临床试验,它是指任
中国科学报 - 临床试验,新药研发 - 2014-08-01
FDA批准治疗热带疾病新药
FDA日前批准Impavido(米替福斯)治疗热带病利什曼病(leishmaniasis),该病是苍蝇叮咬引起,由寄生虫传染给人类。 Impavido由加拿大Paladin公司生产,被批准用于治疗3种主要类型利什曼病。 Impavido获得FDA快速审批,优先审查和罕用药资格认定。
医药经济报 - 新药,FDA - 2014-04-04
为您找到相关结果约500个