FDA要求医生停止使用“三亲”婴儿技术
根据美国食品药品监督管理局(FDA)的说法,张说他的公司不会在未经许可的情况下在美国再次使用这种技术,但他们仍会继续推广。该方案在美国没有得到批准,国会甚至禁止FDA审查
MedSci原创 - “三亲”婴儿技术 - 2017-08-06
2017美国FDA哪五大举措足以影响未来?
我们很多人可能已经对自己个人过去的一年做了总结和评估,以下是我们对FDA过去一年的回顾。可以肯定的是,对于FDA来说,2017是忙碌的一年,在很多层面上,是一个改变游戏规则的时期。
药明康德 - FDA,2017,举措 - 2018-01-05
强生拜瑞妥(Xarelto)ACS适应症遭FDA拒绝
强生(JNJ)和拜耳(Bayer)2月14日表示,FDA已拒绝了抗凝血剂拜瑞妥(Xarelto)用于急性冠脉综合征(ACS)的新适应症申请。这已是FDA第三次拒绝批准Xarelto用于ACS适应症。 强生最初于2011年底提交了Xarelto用于ACS治疗的适应症申请,但遭FDA拒绝,FDA称疗效数据并没有强大到足以支持该适应症的获批。随后,强生提交了额外的数据,但遭FDA再度拒绝。 在强生第
生物谷 - 新药,FDA - 2014-02-17
FDA:机器人已经可以给人做手术了
来自卡耐基梅隆大学的公司Medrobotics Corp.于2015年7月下旬发表声明,称其公司生产的Flex®机器人系统已经得到美国食品及药物管理局(FDA)的放行,可以在市场上销售了。
环球科学 - 机器人,手术 - 2015-08-10
FDA批准默沙东单抗新药,降低耐药菌复发风险
而近日,它的一款新药ZINPLAVA(bezlotoxumab)也获得了FDA的批准,用于降低艰难梭菌(Clostridium difficile)的复发风险。
生物谷 - 单抗新药 - 2016-11-01
Midatech收到FDA对MTD201临床计划的反馈
Midatech是一家专注于为患者提供创新的肿瘤学和罕见疾病产品的研发公司,近日宣布它已于2018年12月20日收到FDA对其主要产品MTD201(Q-奥曲肽)的临床研究的反馈意见。
MedSci原创 - MTD201,FDA,奥曲肽 - 2019-01-29
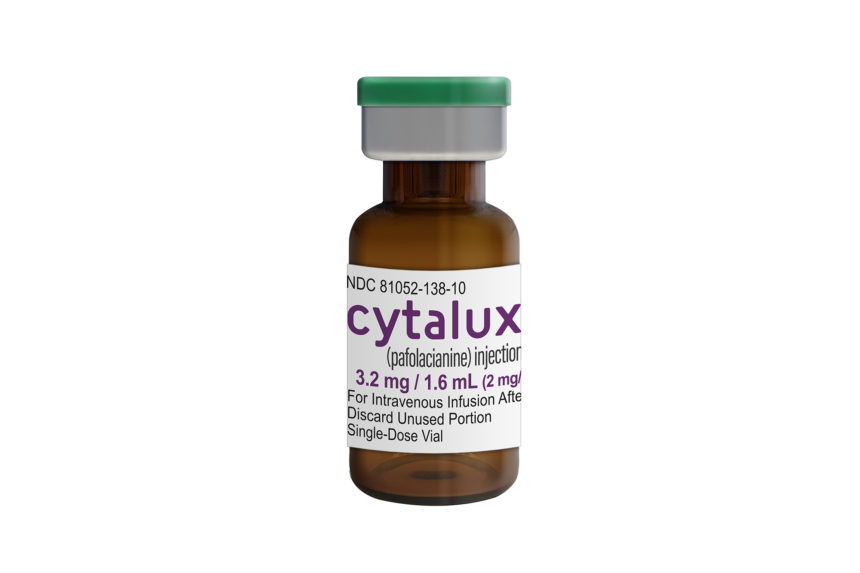
FDA批准Pafolacianine作为肺癌的术中分子成像剂
Pafolacianine(帕福拉西宁)是一种叶酸类似物/吲哚菁绿样结合物,靶向卵巢癌细胞显著表达的叶酸受体 (FR),是第一种经临床证实的靶向荧光成像剂,能在术中照亮卵巢肿瘤,为手术切除提供更准确的
MedSci原创 - 肺癌,Pafolacianine - 2022-12-20
FDA批准DANYELZA(naxitamab-gqgk)治疗神经母细胞瘤
DANYELZA(naxitamab-gqgk)与粒细胞巨噬细胞集落刺激因子(GM-CSF)联用用于治疗1岁及以上的骨复发或难治性高危神经母细胞瘤患者。
MedSci原创 - FDA,神经母细胞瘤,DANYELZA(naxitamab-gqgk) - 2020-11-26
FDA批准PaxVax公司口服单剂量霍乱疫苗研发申请
近日,PaxVax公司口服单剂量霍乱疫苗研发新药申请(IND)获得美国食品药监局(FDA)批准。PXVX-0200是一种对抗霍乱的活性疫苗,先前曾以商品名为Orochol在其他六个国家获得批准。
cyy123 - 新药,FDA - 2012-04-25
阿斯利康旗下的Imfinzi获得FDA批准用于肺癌治疗
阿斯利康于2018年2月19日宣布,美国FDA扩大了Imfinzi(durvalumab)的适应症范围,Imfinzi能够用于治疗铂类化疗和放疗同时进行后疾病没有进展的,不能手术切除的III期非小细胞肺癌
MedSci原创 - Imfinzi,PD-L1,非小细胞肺癌 - 2018-02-26
JAMA:FDA审批新药速度过快或存在安全隐患
FDA药物研究与评估中心负责人指出,医学团体和公众敦促FDA加快新药审批流程,而不是更谨慎地评估一种新药。 两位药物安全专家表示,FDA致力于加快审批预防中风、癌症和多发性硬化症新药上市,但这些新药没有经过全面的安全分析。
网络 - FDA,新药,安全隐患 - 2012-09-20
诺华治疗肢端肥大症长效药物获得FDA批准
美国FDA最近批准了诺华公司开发的用于治疗罕见疾病肢端肥大症的生长激素类药物Signifor登陆美国市场。这一药物也是继Sandostatin后,诺华公司在该领域开发的另一种主打产品。
生物谷 - 诺华,基因治疗 - 2014-12-18
FDA批准ruxolitinib用于骨髓纤维化治疗面临质疑
刚一进3月,NEJM就发表了评论文章针对第一个被FDA批准用于骨髓纤维化的药物ruxolitinib的质疑。同期NEJM发表促成该药物被批准的两个非常重要的临床试验的研究报告。
MedSci原创 - FDA,ruxolitinib,骨髓纤维化 - 2012-03-10
为您找到相关结果约500个