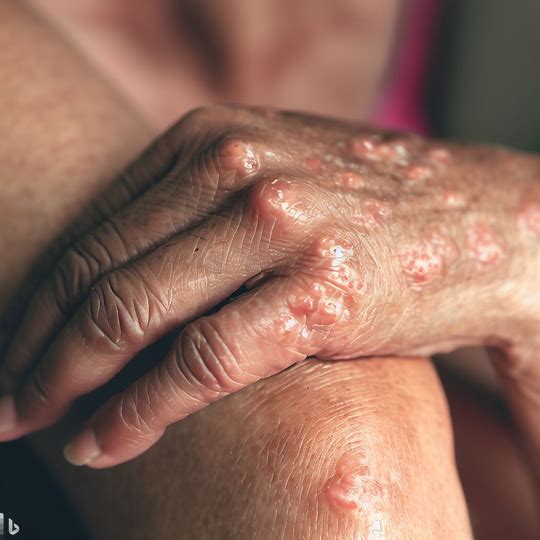
急性细菌性皮肤及皮肤结构感染抗菌药物临床试验技术指导原则
本文为国家药品监督管理局药品审评中心发布的《急性细菌性皮肤及皮肤结构感染抗菌药物临床试验技术指导原则》。
国家药品监督管理局药品审评中心 - 急性细菌性皮肤和皮肤结构感染 - 2024-02-13
与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《与抗肿瘤药物同步研发的原研伴随诊断试剂临床试验注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 抗肿瘤药物 - 2024-03-29
微卫星不稳定性(MSI)检测试剂临床试验注册审查指导原则
本文为国家药品监督管理局医疗器械技术审评中心发布的《微卫星不稳定性(MSI)检测试剂临床试验注册审查指导原则》。
国家药品监督管理局医疗器械技术审评中心 - 微卫星 - 2024-03-07
权威发布|临床试验中的药物性肝损伤识别、处理及评价指导原则
DILI是指由各类化学药品、生物制品、传统中药及其代谢产物乃至辅料等所诱发的肝损伤。
临床肝胆病杂志 - 药物性肝损伤 - 2023-08-25
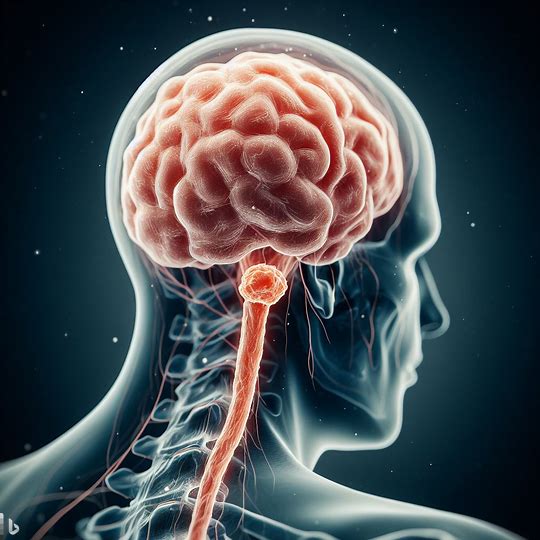
脑膜炎球菌疫苗临床试验技术指导原则(征求意见稿)起草说明
流行性脑脊髓膜炎是由脑膜炎奈瑟氏球菌(简称脑膜炎球菌)感染引起的一种严重的急性呼吸道传染病,由于疾病早期阶段识别和诊断缺乏特异性,疾病进展后的病死率较高。
国家药品监督管理局官网 - 流行性脑脊髓膜炎 - 2023-12-09
慢性肾脏病治疗药物临床试验技术指导原则(公开征求意见稿)
为进一步规范和指导慢性肾脏病治疗药物临床试验,提供可参考的技术规范,我中心起草了《慢性肾脏病治疗药物临床试验技术指导原则》,经中心内部讨论,已形成征求意见稿。
国家药品监督管理局药品审评中心 - 慢性肾脏病 - 2022-11-21
FDA指导原则:校正药物和生物制品随机临床试验中的协变量(草案)
本指南代表了 FDA 当前在药物开发项目随机临床试验统计分析中调整协变量的想法。本指南为在随机、平行组临床试验分析中使用协变量提供了建议,这些试验适用于优效性试验和非劣效性试验。该指南的主要重点是使用
FDA - 统计,临床试验 - 2021-10-22
FDA指导原则:细胞和基因治疗的早期临床试验中研究多形态问题
本指南的目的是为有兴趣在单一疾病的早期临床试验中研究多个版本的细胞或基因治疗产品的申办者提供建议。申办者表示有兴趣在单个临床试验中使用多个版本的细胞或基因治疗产品收集安全性和活性的初步证据。尽管可以在
FDA - 基因治疗 - 2021-10-22
药物临床试验数据管理与统计分析计划指导原则(征求意见稿)
为进一步明确药物临床试验中数据管理和统计分析计划相关技术要求,我中心起草了《药物临床试验数据管理与统计分析计划指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议。
CDE - 数据管理,统计分析计划 - 2021-09-03
关于公开征求《抗肿瘤药联合治疗临床试验技术指导原则》意见的通知
合理的联合治疗可以为肿瘤患者带来更好的治疗选择,但是不恰当的联合开发将增加受试者的风险、降低临床研发效率,浪费时间、财力和医疗资源,反而阻碍了真正有效的联合治疗药物开发
CDE - 临床试验,指导原则 - 2020-07-17
以患者为中心的临床试验获益-风险评估技术指导原则(征求意见稿)
“以患者为中心”的药物研发理念已成为当前药物研发的核心指导思想。为了指导以患者为中心的临床试验的获益风险评估,将患者需求纳入到药物的获益-风险评估体系中,我中心起草
CDE - 以患者为中心 - 2022-08-09
流行性感冒治疗和预防药物临床试验技术指导原则
为指导流行性感冒治疗和预防药物科学研发和评价,提供可供参考的技术标准,药审中心制定了《流行性感冒治疗和预防药物临床试验技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序的
NMPA - 感冒 - 2021-02-10
儿童用化学药品改良型新药临床试验技术指导原则(征求意见稿)
为鼓励以我国儿科临床需求为导向,根据儿童生长发育特点和儿科临床实践需要,开发儿童用化学药品改良型新药,在已发布的《化学药品改良型新药临床试验技术指导原则》基础上,药审中心起草了《儿童用化学药品改良型新
CDE - 临床试验 - 2021-05-13
为您找到相关结果约500个