首款纳米抗体药物Cablivi®
首个纳米抗体药物Cablivi获批继EMA批准之后,2019年2月,FDA批准Cablivi?Cablivi?是FDA批准的首个专门用于治疗aTTP的疗法。预计将会为赛诺菲 (2018年收购Ablynx)带来5~6.5亿美元的收入。Sheridan C. Nature Biotec
生物制药小编 - Cablivi - 2019-05-10
纳米抗体药Cablivi获FDA批准 治疗罕见凝血障碍
近日,FDA批准 Cablivi(Caplacizumab-Yhdp),用于治疗成人获得性血栓性血小板减少性紫癜(aTTP)。Cablivi是首个特异性的aTTP治疗药物,也是首个获批上市的纳米抗体药。aTTP是一种罕见的导致血液凝结的危及生命的疾病, Cablivi是第一种将血浆交换与免疫抑制疗法结合用于该种疾病的药物。
健康界 - 纳米抗体药 - 2019-02-20
全球首款纳米抗体Caplacizumab继FDA、EMA之后,再次获得NICE批准治疗罕见病患者的凝血障碍
Caplacizumab是靶向血管性血友病因子(vWF)的纳米抗体(VHH),通过阻断vWF聚集体与血小板的相互作用,进而降低血小板的粘附和消耗。
MedSci原创 - 纳米抗体Caplacizumab,获得性血栓性血小板减少性紫癜(aTTP) - 2020-11-16
CAR-T疗法获得欧盟批准
在诺华的Kymriah和Gilead的Yescarta都获得人类医疗产品委员会(CHMP)的支持之后,该阶段已获欧洲首批嵌合抗原T细胞疗法(CAR-T)的批准。委员会建议批准Kymriah治疗B细胞急性淋巴细胞白血病(ALL)和弥漫性大B细胞淋巴瘤(DLBCL),以及Yescarta治疗DLBCL和原发性纵隔B细胞淋巴瘤(PMBCL)。CAR-T疗法提供了一种新的治疗方法,因为它是专门为每个患者制
MedSci原创 - CAR-T疗法,欧盟批准 - 2018-07-02
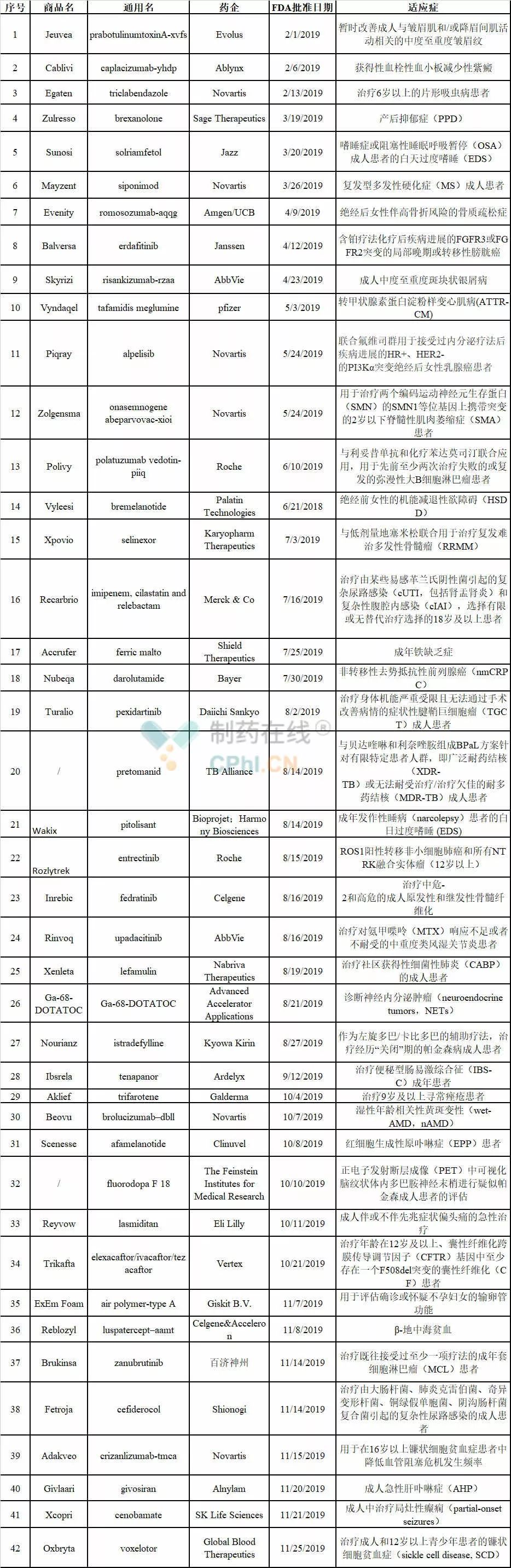
FDA 2019:批准45款新药,9款生物类似药
美国FDA的药物评估与研究中心(CDER)已经批准42款新药,9款生物类似药,3款在路上,而生物制品评估与研究中心(CBER)也批准了诺华公司的基因疗法Zolgensma和首款登革热疫苗。另外还有3款新药的PDUFA时间在12月,预计2019年将有45款新药获得FDA批准。相较于2017年和2018年,2019年会是FDA批准新药数量最低的一年,但质量不差,比如Skyrizi、Zolgensm
MedSci - FDA,新药 - 2019-12-24
柳达:罕见病与孤儿药是行业范式转移的必由之路,将为人类健康作出巨大贡献
蔻德罕见病中心创始人主任黄如方也在把科研人员、患者、药企三方资源通过基金会进行整合,发挥各自专业所长,降低罕见病药物研发成本、提高效率。
深究科学 ID: deepscience - 孤儿药,罕见药 - 2023-03-04
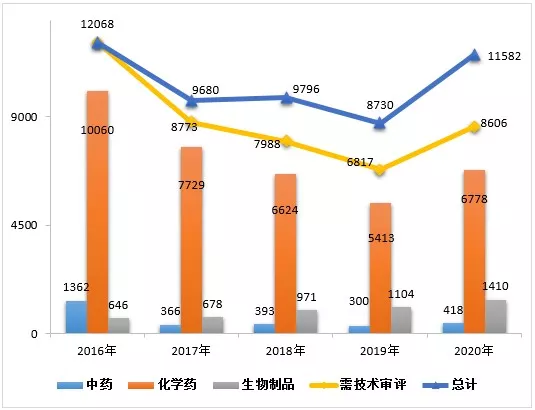
2020年度药品审评报告
2020年是极不平凡的一年,面对突如其来的新冠肺炎疫情,中国国家药品监督管理局药品审评中心(以下简称药审中心)在中国国家药品监督管理局(以下简称国家药监局)的坚强领导下,贯彻《药品管理法》《疫苗管理法
CDE - 药品审评报告 - 2021-06-23
为您找到相关结果约7个