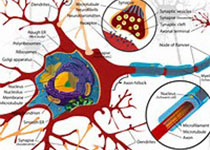
Neurology:Eteplirsen治疗杜氏肌营养不良长期疗效研究
研究证实,Eteplirsen长期治疗可诱导肌细胞穿透、外显子跳跃并促进新的肌萎缩蛋白表达
MedSci原创 - 杜氏肌营养不良,DMD,Eteplirsen - 2018-05-12
治疗杜氏肌营养不良症的首个新药Eteplirsen获FDA批准
FDA与9月19日宣布了这一决定,在经过了一年多的考虑和争论后,随着FDA不断地去平衡病人巨大的需要和临床资料的不足,如今他们终于批准了这种名为eteplirsen的药物进行广泛的临床试验。病人的倡导者对这项决定表示非常高兴,很多人都非常想使用药物eteplirsen,该药
生物谷 - 新药Eteplirsen - 2016-09-26
FDA终于批准首个杜氏肌营养不良新药eteplirsen
已有4个DMD新药在半年内接连遭到FDA的拒绝,而近日,FDA终于批准首个新药eteplirsen。
医药魔方数据 文章链接:中国制药网 - 杜氏肌营养不良,遗传病,新药 - 2016-09-21
FDA批准首个杜氏肌营养不良症(DMD)治疗药物Exondys 51(eteplirsen)
Exondys 51(eteplirsen)专门适用于抗肌营养不良蛋白基因(dystrophin gene)中存在确证突变可导致51号外显子跳跃(exon 51 skipping)的DMD患者;据估计,
生物谷 - Sarepta,杜氏肌营养不良,Exondys,51,Eteplirsen - 2016-09-26
杜氏肌营养不良症首个新药获批
杜氏肌营养不良症患者会慢慢出现肌无力。 图片来源:Eric Kruszewski 日前,美国食品药品监督管理局(FDA)批准了首个治疗杜氏肌营养不良症的药物,相关试验数据主要来自于对12名男孩儿的研究结果。 该机构在经过了一年多的考虑和争论后,于9月19日宣布了这一决定。《自然》杂志报道称,随着FDA不断平衡巨大需要和临床资料不足间的矛盾,终于批准了这种名为ete
科学网 - 杜氏肌营养不良症,突变 - 2016-09-28
GSK治疗杜氏肌营养不良药物drisapersen三期研究失败
制药巨头葛兰素史克公司开发的用于治疗杜氏肌营养不良的药物drisapersen上周宣布失败。公司表示在分析数据后发现,此次三期研究未能达成任何有价值的研究结果。在这次长达48周的研究中,使用drisapersen的患者相比于安慰剂组未能有明显改善。尽管此次三期临床试验结果不尽理想,公司研究人员表示仍将深入分析研究结果以确定drisapersen是否仅对特定群体有效。 详细英文报道: O
生物谷 - 杜氏肌营养不良,GSK - 2013-10-11
SCIENCE:重磅:又是CRISPR!全球首个大型动物研究证实,基因疗法有望根治肌萎缩
谁都希望自己的宝宝健健康康,但有些时候,偏偏会发生一些事与愿违的意外。遗传病就是这样的例子。看起来健康的夫妇二人,生下的宝宝却会出现奇怪的症状。直到做了基因检测才发现,宝宝是得了先天性遗传病。
学术经纬 - CRISPR,大型动物研究,基因疗法,根治肌萎缩 - 2018-08-31
PTC杜氏营养肌不良症药物被拒
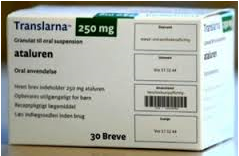
今天美国生物技术公司PTC Therapeutic的杜氏营养肌不良症(DMD)药物Translarna(ataluren)被FDA拒绝受理。Translarna已经在欧盟有条件上市,但如果三期临床失败仍可能被撤市。在去年的一个三期临床试验中Translarna未能显着改善DMD儿童6分钟走,但PTC认为亚组分析显示该药对部分病人可能有效。PTC前总经理说她不能肯定Translarn
生物谷 - 基因治疗 - 2016-03-02
CHMP对Sarepta的DMD治疗持负面看法
根据与CHMP代表的讨论,我们了解到CHMP没有得出eteplirsen对于51号外显子患者无效的结论,而是Sarepta尚未达到有条件批准的监管门槛,部分原因是由于在研究中使用外部控制作为比较对象。"
MedSci原创 - CHMP,Sarepta的DMD治疗 - 2018-05-05
【盘点】2016年与我们密切相关的“孤儿药”研发动态
导读 由于罕见病患病人群少、市场需求少、研发成本高,很少有制药企业关注其治疗药物的研发,因此这些罕见病患者的用药被形象地称为“孤儿药”。虽然患者群体少,但每一位罕见病病友对孤儿药的需求却是百分百的。在国内,受罕见病政策缺失、市场不成熟、研发技术欠缺等因素的制约,罕见病药物在国内的市场研发几乎是空白。但随着国家对罕见病领域的关注,这一现状,或许在不久的将来会有所改观。2016年2月14日,国务院总理
中国罕见病/罕见病发展中心 - “孤儿药”,研发动态 - 2016-12-30
这些新药或将改变这4种疾病的治疗用药格局
Tharaldson指出即将在2015年后期及2016年批准上市的几种专科药将可能对以下4种疾病的治疗产生深深影响,下面我们来详细看一下是哪四种疾病。10月27日在佛罗里达奥兰多召开的一个医药行业学术会议中,快捷方药(Express Script)公司新兴疗法资深临床顾问、药学博士AimeeTharaldson在会议上就处于研发中的几种专科药做了相关介绍。她指出了几个可能在2016年被批准的专
新康界 - 新药,治疗 - 2015-11-04
FDA 发布关于渤健用于阿尔茨海默氏症的 Aduhelm 的内部辩论详细信息
近日,美国食品和药物管理局(FDA)有争议地批准Biogen公司的Aduhelm(aducanumab)治疗阿尔茨海默病的更多细节。
MedSci原创 - 阿尔兹海默症 - 2021-06-24
《自然》分析:美食药监管面临巨大挑战
FDA尚未决定如何监管转基因动物食品,例如这头没有角的奶牛。 图片来源:Courtesy of Recombinetics 美国当选总统唐纳德·特朗普希望加速药物批准及广泛减少政府监管。这对美国食品与药物管理局(FDA)意味着什么尚不清楚,但如果特朗普政府对其他岗位的选择可以作为参考,那么他将会寻找一位FDA行政长官改变现状。 下一任FDA局长或将改变该机构对从医疗检验到宣称提供
中国科学报 - 药物 - 2017-01-16
今天的RNA-based疗法,犹如1997年的单抗
近年来,RNA-based疗法在遗传病、罕见病领域的成效越来越显著。在过去的7年里,我们见证了3例反义寡核苷酸的获批,包括几个月前获批的Exondys 51和Spinraza。首个小干扰RNA(siRNA)疗法有望在下一年问世。
生物探索 - RNA,单克隆,抗体 - 2017-03-15
AAN 2014:Eteplirsen治疗杜氏肌营养不良安全有效
在某些杜氏肌营养不良症(DMD)患者中,Eteplirsen可以在超过2年的时间内安全地维持其对行走速度的有益作用,并且是首个能在这一时间段内稳定膈肌功能的药物。 Jerry R.Kaye博士深入报告了安全性和药代动力学数据:在这项小规模研究中,eteplirsen未引起明显的治疗相关不良事件。迄今尚无患者停止或
爱唯医学网 - AAN,Eteplirsen,杜氏肌营养不良症 - 2014-05-13
为您找到相关结果约25个