以治愈艾滋病为目标!FDA批准美国基因技术公司(AGT)推进HIV治愈计划的I期临床
2020-08-12 Allan MedSci原创
AGT103-T是一种基于慢病毒载体的基因疗法,旨在彻底清除HIV,该疗法可以修复HIV对免疫系统造成的损害,并允许自然免疫反应来控制病毒。
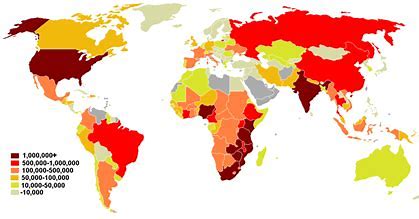
艾滋病已经影响社会超过四十年。在全球范围内,将近3800万人感染了艾滋病病毒,在美国,有超过100万人感染了艾滋病病毒。迄今为止,治愈该疾病的努力一直没有成功。
美国基因技术公司(AGT)今日宣布,已获得FDA的批准,将开始进行I期临床试验,以验证基因疗法AGT103-T治疗艾滋病的有效性和安全性,这也是AGT103-T的首次人体试验。AGT将在华盛顿健康研究所、马里兰大学、人类病毒研究所和乔治敦大学的临床中心进行其I期研究。这些中心预计将于2020年9月开始注册,AGT希望在年底之前报告初始数据。AGT的I期临床试验将研究AGT103-T的安全性、测量关键的生物标志物并探索功效的替代标志物。
AGT103-T是一种基于慢病毒载体的基因疗法,旨在彻底清除HIV,该疗法可以修复HIV对免疫系统造成的损害,并允许自然免疫反应来控制病毒。根据其研究,AGT认为AGT103-T可以治愈艾滋病。AGT103-T细胞产品是由血细胞经11天的过程制成的,该过程可增加对抗HIV的T细胞并使用基因疗法帮助这些细胞在体内存活。临床前研究表明,AGT103-T能够清除HIV。
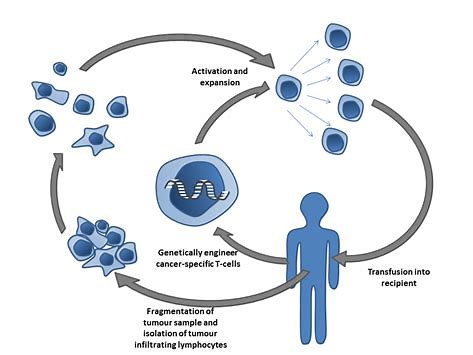
AGT对AGT103-T的表征是与美国国立卫生研究院(National Institutes of Health)的国家过敏和传染病研究所(NIAID)合作完成的。由AGT和NIAID科学家共同撰写的同行评议文章于2020年6月发表在《分子疗法》上,该文章描述了AGT103-T制造工艺的演变过程。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#I期临床#
35
#FDA批准#
36
#基因技术#
48
希望临床实验成功#艾滋病#
168
打破0评论
94