综述目的:描述因缺氧缺血性脑损伤(HIBI)导致心脏骤停复苏后昏迷患者可用的神经监测工具。
最近发现:
脑电图(EEG)可用于检测癫痫发作并指导抗癫痫治疗。此外,特定的脑电图模式可准确识别不可逆性HIBI患者。HIBI患者的脑血流量(CBF)下降,或者血流量没有恢复,则表明预后较差。在一些HIBI患者中,CBF自动调节曲线变窄并右移,其中大多数患者预后较差。来自近红外光谱(NIRS)、颅内压(ICP)和经颅多普勒(TCD)以及脑组织氧合的参数正在研究作为优化HIBI患者和脑自动调节改变患者的CBF的工具。脑生物标志物的血液水平及其随时间的变化趋势用于评估研究和临床中HIBI的严重程度,并预测心脏骤停后昏迷的结局。目前复苏后指南推荐神经元特异性烯醇化酶(NSE)作为HIBI的预后工具,但其他可能更准确的生物标志物,如神经丝轻链(NfL)正在研究中。
总结:
神经监测为HIBI患者发现并发症、个体化治疗和预测预后提供了重要信息。
引言:
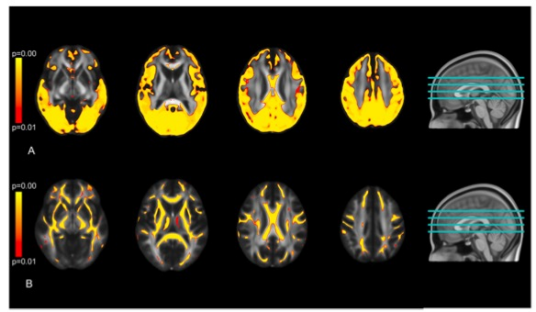
大约三分之二的心脏骤停复苏后入住ICU的患者死于缺氧缺血性脑损伤(HIBI)。限制脑损伤是复苏后管理的主要目标,因此,神经监测是必不可少的。目前有几种用于HIBI患者的神经监测工具(图1)。
监测脑电活动
脑电图(EEG)被广泛用于HIBI的神经监测。然而,其信号是复杂的,包括多种异常模式。这些已被美国临床神经生理学学会(ACNS)编成重症监护的标准术语。在自主循环恢复(ROSC)一开始,脑电图振幅常明显降低或不连续。抑制(脑电图振幅低于10 mV)或爆发-抑制(超过一半的记录被抑制,与电爆发交替出现)是重度HIBI的标志,特别是在ROSC后24小时出现的抑制几乎总是与较差的远期残疾或死亡相关。然而,在神经功能恢复的患者中,脑电图显示出持续的、正常幅度的背景改善。
心跳骤停后的脑电图背景也可以显示叠加的癫痫样放电。在孤立状态下,HIBI患者的放电意义不大。然而,如果放电是大量的和/或以有规律的方式重复出现,它们被称为节律性或周期性模式(RPPs),值得特别注意。癫痫发作是持续10 s或以上、频率超过2.5 Hz或有时空演变的RPPs。约30%的昏迷复苏患者出现癫痫或RPPs。然而,由于镇静和/或肌肉麻痹,这些异常通常缺乏临床表现,只能在脑电图上检测到。ROSC后24-48小时内脑电图癫痫发作表明重度HIBI,预后不佳。相反,迟发性癫痫发作并不排除恢复。
脑电图监测通常用于指导心脏骤停后的抗癫痫药物(AEDs)治疗。然而,AEDs在癫痫发作后的益处尚不清楚。在对172例心脏骤停后昏迷的RPPs患者进行的多中心随机开放标签TELSTAR试验中,与未接受治疗相比,包括AEDs、催眠药和巴比妥类药物在内的阶梯治疗并未提高6个月时良好神经系统存活率。然而,一项亚组分析显示,与RPPs较慢的患者相比,癫痫发作患者AEDs治疗的改善趋势并不显著。
HIBI后最常用的是20-30分钟的量化常规脑电图,大多数医院在办公时间都可以使用。与常规EEG相比,连续EEG监测有助于评估ROSC后的EEG演变,并提高癫痫发作检测的敏感性,但没有证据表明与间歇EEG相比它改善了预后预测。
要点
缺氧缺血性脑损伤(HIBI)是心脏骤停后死亡的主要原因,复苏后迅速进展。
HIBI可能与癫痫发作、脑水肿、颅内高压、脑血流自动调节改变和脑组织缺氧有关,这些可能进一步加重脑损伤。
EEG在HIBI中有助于检测癫痫发作,指导其治疗,并评估HIBI的严重程度以预测预后。
ICP、TCD、PbtO2和NIRS的监测可以提供有关脑氧合和灌注的有效信息,从而指导降低HIBI严重程度的治疗。
HIBI生物标志物(如NSE或NfL)的连续评估有助于预测心脏骤停后昏迷患者的预后。
监测动脉脑血流量
实验证据表明,在ROSC后最初短暂充血后,HIBI患者的脑血流(CBF)显著减少。虽然CBF不能在床边直接评估,但经颅多普勒超声(TCD)提供了脑血流速度(CBFV)的无创评估。如果动脉直径保持不变,TCD上CBFV的变化反映了CBF的变化。在两项早期研究中,ROSC后大脑中动脉(MCA)的平均CBFV立即下降,但在72小时内恢复正常,存活者和死亡者之间无差异。然而,在幸存者中,脑氧摄取分数(CEO2)略有下降,并在72小时内恢复到正常值,但在死亡的患者中,CEO2显著下降,并在72小时内保持在较低水平。最近的一项研究显示,在神经系统预后不良和脑损伤生物标志物升高的HIBI患者中,颈静脉血氧饱和度高于正常值(d>75%)。总之,这些发现表明,在心脏骤停后,CBF降低,同时大脑代谢降低,这在更严重的HIBI患者中更为明显。GOODYEAR试验正在研究ROSC后前12小时内TCD指导的早期目标导向血流动力学管理的可行性。
监测颅内压
HIBI常伴有神经元肿胀(细胞毒性水肿)和严重的神经炎症伴血脑屏障(BBB)破坏,导致血管源性水肿。这可能导致颅内压(ICP)增高[即颅内高压(ICHT)]和脑灌注压(CPP)降低。在一项对84例心脏骤停后昏迷患者的研究中,超过四分之一的患者在ROSC后的第二天经历了ICHT (ICP>25 mmHg),其中超过一半的患者CPP下降到50 mmHg以下。在一项生理学研究中(n = 10),通过脑实质内探针监测ICP,中位时间为ROSC后8.5h,中位持续时间为40.5h(四分位数间距为24-51h)。虽然平均ICP仅为14mmHg,但ICHT(ICP>20mmHg)发生在总神经监测时间的22%。2例患者尽管接受了最大限度的药物治疗,但仍发生了致死性难治性ICHT。此外,所有患者均表现出颅内顺应性下降,实时测量的ICP均值与ICP波形的平均脉冲压力的相关系数为颅内顺应性。在另一项生理学研究(n=10)中,通过脑实质内导管和脑微透析膜,在ROSC后的前72小时内每小时测量10名接受低温治疗患者的ICP和乳酸/丙酮酸盐比率(LPR),随后逐渐复温24-48小时,复温期间ICP持续升高。低温期间LPR正常,但在神经功能不良的患者复温后LPR显著升高,提示无氧脑代谢。
由于临床经验有限,且同时使用抗血小板和/或抗凝治疗,复苏患者的侵入性ICP监测并非常规使用。TCD可以根据脑水肿引起的动脉血管阻力增加的测量结果,提供一种替代的ICHT无创评估方法。在TCD上,血管阻力采用搏动指数测量,计算为(收缩期-舒张期CBFV)/平均CBFV。搏动指数≥1.20表明动脉阻力增加,提示在这种临床情况下存在ICHT。在一项11例HIBI患者的研究中,使用搏动指数测量的无创ICP与使用脑实质内探针测量的有创ICP呈线性相关(R = 0.30),并对ICHT具有良好的预测价值[受试者工作特征曲线下面积(AUROC) = 0.91 (95% CI 0.83 - 1.00)]。在最近的一项研究中(n = 42),虽然大多数患者ROSC后6 h的平均CBFV值在正常范围内,但神经系统预后不良患者的搏动指数显著升高(1.49 vs. 1.12,P = 0.01),其中6例患者死于脑死亡。
心脏停搏后监测ICP的基本原理是治疗可能加重HIBI的脑水肿引起的ICHT。心脏骤停后ICHT的最佳治疗策略仍不确定。虽然高渗疗法可减轻细胞毒性脑水肿,但由于渗透性活性颗粒在血管外蓄积,它们可能会加重血管源性水肿。然而,有证据表明渗透疗法对实验性心脏停搏后的脑水肿有益。此外,一项回顾性、单中心、匹配的观察性队列研究(n = 65)显示,在HIBI患者中,与标准治疗相比,在神经监测指导下对ICHT进行积极治疗与显著较高的神经系统预后良好率相关。迄今为止,尚未发表任何旨在治疗HIBI中ICHT或减轻脑水肿的临床试验。

监测脑氧合
脑组织氧分压
虽然TCD和颈静脉球血氧饱和度的研究提示HIBI患者的脑血流和代谢之间可能存在正常的耦合关系,但并没有直接评估脑组织的氧合水平。这是通过使用脑实质内探针在间质水平测量PbtO2来实现的。脑氧合不仅依赖于氧的输送(即脑血流量和动脉血氧含量),还依赖于微循环氧的扩散和脑代谢。PbtO2<20 mmHg被认为是识别组织缺氧和触发特异性干预的阈值。
脑组织缺氧的发生是HIBI再灌注损伤的潜在机制。一项针对18例HIBI患者的研究表明,低PbtO2与脑损伤生物标志物的活性释放和白细胞介素-6的脑内释放有关,后者表明HIBI中神经炎症的重要作用。在同一组的另一项研究(n=10)中,患者在38%的监测时间(743/1944 10分钟平均周期)中PbtO2低于20 mmHg。作者描述了该队列的两种病理生理表型。第一种是“扩散受限”表型,尽管优化了氧输送,但仍有持续的组织缺氧,这可能是由于血脑屏障破坏导致血管周围水肿或线粒体功能障碍;第二种是“灌注依赖性”表型,氧弥散完整。旨在减轻脑组织缺氧的疗法(如渗透性疗法或MAP增强)可能对后一种表型更有效。
近红外光谱
近红外光谱(NIRS)是一种非侵入性工具,使用红外光吸收率来计算氧合血红蛋白和去氧血红蛋白,从而监测局部脑氧合(rSO2)。在市售的NIRS监测器中,近红外光由一个二极管发出,由两个二极管接收,所有二极管都放置在前额皮层上方的头皮上。NIRS采样区域位于颅骨下方约2cm处。由于约70%的采样血液为静脉血,正常rSO2约为60-80%。
几项观察性研究对NIRS进行了研究,以评估HIBI的严重程度,但结果相互矛盾。2012年,日本的一项多中心研究纳入了596名因院外心脏骤停复苏后昏迷的患者,结果表明,入院时测得的rSO2比乳酸更准确地预测30天的神经功能结果(AUROC 0.91 vs.0.77;P=0.0001)。然而,随后的研究并未证实这些发现。NIRS的一个主要问题是来自脑外循环的污染。此外,NIRS是使用专有算法得出的,这使得很难比较不同监测器获得的结果。目前,不建议NIRS用于心脏骤停后的预测。与其他监测工具一样,rSO2趋势可能比绝对值更具信息性。
监测脑自动调节
正常情况下,脑循环在一定的平均动脉压(MAP)范围内维持稳定的CBF。这种特性被称为脑的自动调节。然而,在大约三分之一的HIBI患者中,自动调节平台变窄并右移。因此,心脏骤停后的动脉低血压可能导致脑灌注不足,加重HIBI。一项前瞻试验和一项更大规模的临床试验表明,心脏骤停后目标高MAP和低MAP并不会改变神经系统结局或用血液生物标志物测量的HIBI严重程度。另一方面,作者提倡个体化血压目标,旨在将MAP维持在个体患者完整的自动调节范围内,以优化脑灌注。为此,研究了脑氧合指数(COx)和压力反应指数(PRx)这两个衍生参数,分别是rSO2与ICP以及MAP的相关系数。随着MAP的增加,COx或PRx的增加表明自动调节的失调,而COx或PRx的接近零或负值表明自动调节得以维持。在该模型的基础上,“最佳MAP”是对应于COx或PRx的最低值的范围。
在一项前瞻性观察研究中,51例心脏骤停后昏迷患者中,18例有自动调节功能障碍,且低于最佳MAP的时间与较低的生存可能性相关[优势比(OR) 0.97 (0.96 ~ 0.99),P = 0.02]。在另一项前瞻研究中(n=23),心脏骤停后第1-3天的COx升高与3个月时的死亡率独立相关。在HIBI患者中,使用PRx也发现了自动调节失调与不良预后之间的类似关联。近年来,通过TCD对心脏骤停后常温和低温状态下的脑自动调节进行了评估。在一项对50例因院外心脏骤停而复苏的患者的研究中,Crippa等通过测量MCA平均血流指数(Mxa),即平均CBFV和动脉血压之间的Pearson相关系数,研究了低温治疗期间和复温后的脑自动调节。Mxa>0.3定义为大脑自动调节的改变。虽然各结局组在低温治疗期间的自动调节改变发生率相似,但在死亡或复温后神经系统结局不良的患者中,Mxa> 0.3的发生率显著较高[31/36 (86%) vs. 7/14 (50%);P = 0.02]。多变量分析显示,高Mxa与神经功能预后不良相关。
虽然通过COx或PRx检测到的脑自动调节功能失调与心脏停搏后的不良神经系统结局相关,但目前尚不清楚这是否只是HIBI严重程度的标志物或治疗靶点,而且迄今尚未发表对照试验评估以自动调节为目标的MAP是否可以减轻HIBI严重程度。
生物标记物
脑损伤的生物标志物是脑组织在受到损伤后释放的细胞成分。其用于评估HIBI的基本原理是它们的释放与细胞损伤的严重程度成正比。目前研究最多的生物标志物有神经元特异性烯醇化酶(NSE)、S-100B、神经丝轻链(NfL)、Tau、GFAP和UCH-1。其中,只有NSE被广泛应用于临床实践,并且是唯一被复苏后管理指南推荐的。NSE和UCH一样来源于神经元体,而NfL和Tau由轴突释放,S100B和GFAP由胶质细胞释放。
理解生物标志物的动力学对其正确的临床应用很重要。NSE血液水平在ROSC后48–72小时达到峰值,此时其评估HIBI严重程度的准确性最高。NSE半衰期为24–30小时,因此,在ROSC后4-5天及之后,在预后不佳的患者中仍能发现明显高水平的NSE。重度HIBI患者NSE水平在24-72 h升高,但恢复正常后NSE水平下降或保持稳定。在一项研究中,ROSC后48 h和24 h的NSE值的比值为1.7,72 h和24 h的NSE值的比值为1.3,对神经系统预后不良的特异性为100%。在其他研究中也发现了类似的结果。欧洲复苏委员会和欧洲重症监护学会(ERC-ESICM)复苏后指南建议在ROSC后24至72小时连续测量NSE,并建议在48–72小时使用60 μg/L的NSE阈值来预测HIBI的不良预后。
在最近研究的HIBI生物标志物中,NfL是最有前途的。在多中心生物样本库研究中,NfL比NSE更准确地预测不良的神经结局,其准确度早在ROSC后24小时就高[AUROC 0.94(0.92–0.95)]。NfL的主要局限性在于,由于其通过血脑屏障的扩散有限,其血浆水平非常低,需要特定的超敏测定。此外,用于识别不可逆HIBI的NfL截断值水平在不同研究中差异很大,其最佳阈值尚未确定。
结论
心脏骤停会导致不同程度的广泛脑损伤,其结局从完全恢复到严重残疾或死亡不等。在最初的缺血后,再灌注损伤随时间演变,可能导致神经元膜不稳定、脑水肿、颅内高压、脑灌注不足和自动调节降低。所有这些变化为心脏停搏后的神经监测提供了指征。在可用的工具中,EEG可用于预测癫痫发作的检测和治疗效果。ICP、TCD、PbtO2和NIRS可指导临床医生优化CBF和脑氧合灌注。生物标志物的系列评估有助于评估脑损伤的严重程度,并预测缺氧后昏迷恢复的可能性。除了潜在的临床应用外,这些神经监测工具都在进行积极的研究,旨在提高我们对HIBI病理生理学和最佳管理的理解。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言