2024 FDA指南:考虑在第564条宣布的紧急状态期间进行测试的执行政策
FDA发布本指南草案,以描述我们在决定根据《联邦食品、药品和化妆品法》(FD&C Act)第564条在未来宣布的紧急情况下发布有关测试制造商提供某些未经批准的测试的执行政策时打算评估的因素。
2024 FDA指南:人类同种异体细胞的安全性测试扩展到基于细胞的医疗产品中
人源的同种异体细胞可以在培养物中扩增,以制造由活细胞、灭活细胞、细胞裂解物或其他基于细胞的材料(如细胞衍生颗粒)组成的医疗产品。
涉及脑机接口临床研究的多学科伦理审查专家共识
在《脑机接口研究伦理指引》的指导下,对重大伦理风险防控等方面提出建议,厘清各方责任,从多维度为涉及脑机接口临床研究伦理审查的实质内容及程序提供参考。
2024 FDA指南:在细胞和基因治疗以及组织工程医疗产品制造中使用人类和动物源性材料的注意事项
使用人类和动物来源的材料来制造细胞和基因治疗 产品以及组织工程医疗产品 提出了几个需要考虑的关键问题,包括外源因子的传播、材料批次间的一致性和材料特性,以及一般材料资格考虑因素。
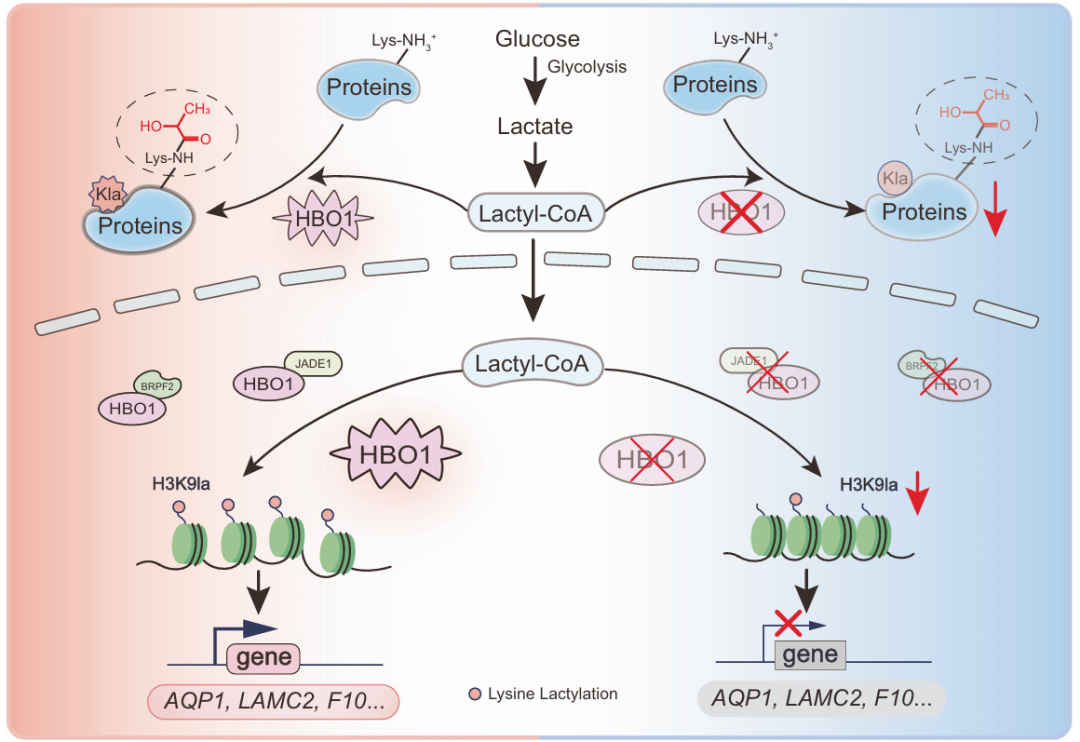
Nat Commun:天津医科大学张锴等发现HBO1介导组蛋白乳酸化调控基因转录的分子机制
该研究发现了HBO1可以催化乳酸化修饰的发生,并揭示了其介导组蛋白乳酸化调控转录的分子机制,为Kla发生机制和功能提供了新的见解。
2024 FDA指南:处方生物参考品和生物仿制药的促销标签和广告注意事项 行业问答指南
本指南讨论了在这些促销信息中提供有关参考产品或生物仿制药的数据和信息的注意事项,以帮助确保它们准确、真实且无误导性。