JHO:新诊断、未经治疗TP53突变AML的治疗结局:系统性回顾和META分析
2023-03-17 聊聊血液 网络 发表于上海
对于新诊断的未经治疗TP53m AML 患者,各治疗组(包括IC、HMA和VEN +HMA)的 CR 率、中位 OS 和其他疗效指标均较低。
急性髓系白血病 (AML) 多发生于45岁以上的成人中,诊断时的中位年龄为68岁,估计所有AML患者的5年生存率为29.5%。AML 的主要治疗方法是联合使用阿糖胞苷和蒽环类药物,例如“7 + 3”和“FLAG-Ida”(氟达拉滨、阿糖胞苷、伊达比星和粒细胞集落刺激因子)方案作为强化诱导化疗。对于无法耐受强化化疗 (IC) 的患者,多使用去甲基化药物 (HMA)。自口服BCL-2抑制剂维奈克拉(VEN) 上市以来,HMA(例如阿扎胞苷 [AZA] 或地西他滨 [DEC])常与 VEN 联合用于 AML 的一线治疗,尤其是75岁或以上或无法耐受 IC 的患者。
新发 AML 患者中5-15%和继发性 AML 患者中17.6%可检测到TP53突变(TP53m),而在治疗相关 AML 患者中约有30%检出该突变。与 TP53 野生型 AML 患者相比,由于对标准 AML 治疗耐药,TP53m AML患者的预后明显更差,总生存期更短(6.5 vs. 33.6个月);在 IC 或低强度化疗后,TP53m患者的结局同样比 TP53 野生型患者更差。即使使用HMA +VEN治疗的CR/ CRi率高达40-60%,但中位总生存期 (OS) 仍较低,仅5-6个月。总的来说尚未确定 TP53m AML 患者的最佳治疗。
对过去几十年中治疗特异性临床结局的全面了解,有助于阐明该患者人群中未满足的治疗需求的程度,并确立该领域的新型疗法和组合的历史预期。近日《Journal of Hematology & Oncology》发表了一篇系统性综述和荟萃分析,旨在评估新诊断、未经治疗TP53m AML患者IC、HMA和VEN + HMA治疗的结局。


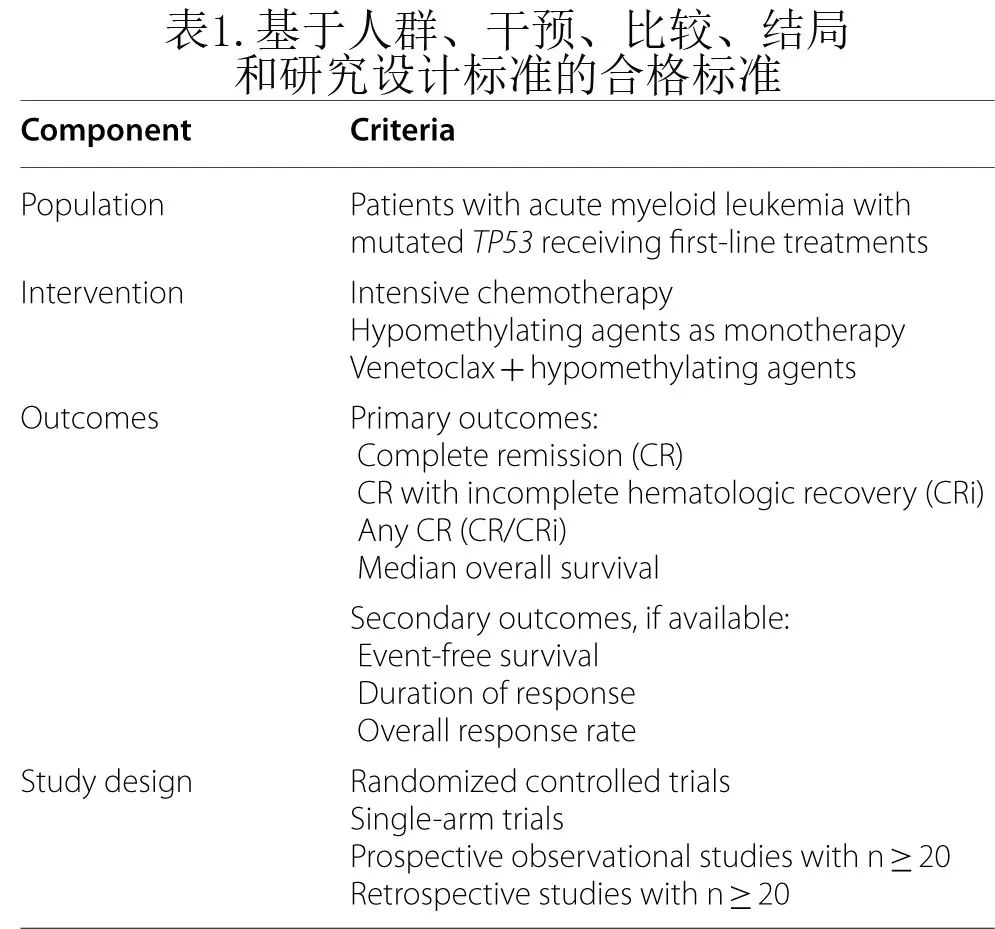
作者检索了 EMBASE 和MEDLINE从建库至2021年05月20日的报道,纳入接受IC、HMA或VEN + HMA的新诊断或未经治疗TP53m AML 患者的研究,且研究必须是随机对照试验 (RCT)、单臂或非随机临床试验、或前瞻性或回顾性观察性研究。详见表1。
所有研究均纳入了接受IC、VEN + HMA和/或 HMA 单药的患者,但研究之间的治疗剂量、频率和持续时间不同。在汇总研究之间的临床结局时也未考虑这些治疗差异以及治疗中断或退出信息。如果描述了多种给药方案,则选择一种给药方案的结果。例如对于评价 DEC 的2种给药方案(DEC-5天和 DEC-10 天)的一项研究,仅 DEC-10 天结果纳入该分析中,因为该组的患者数量更多,并且与分析中纳入的另一项 DEC 研究中使用的给药方案一致。

研究筛选
审查过程的结果总结见图1。总的来说12项独特研究的17篇出版物构成了本综述和荟萃分析的证据基础。

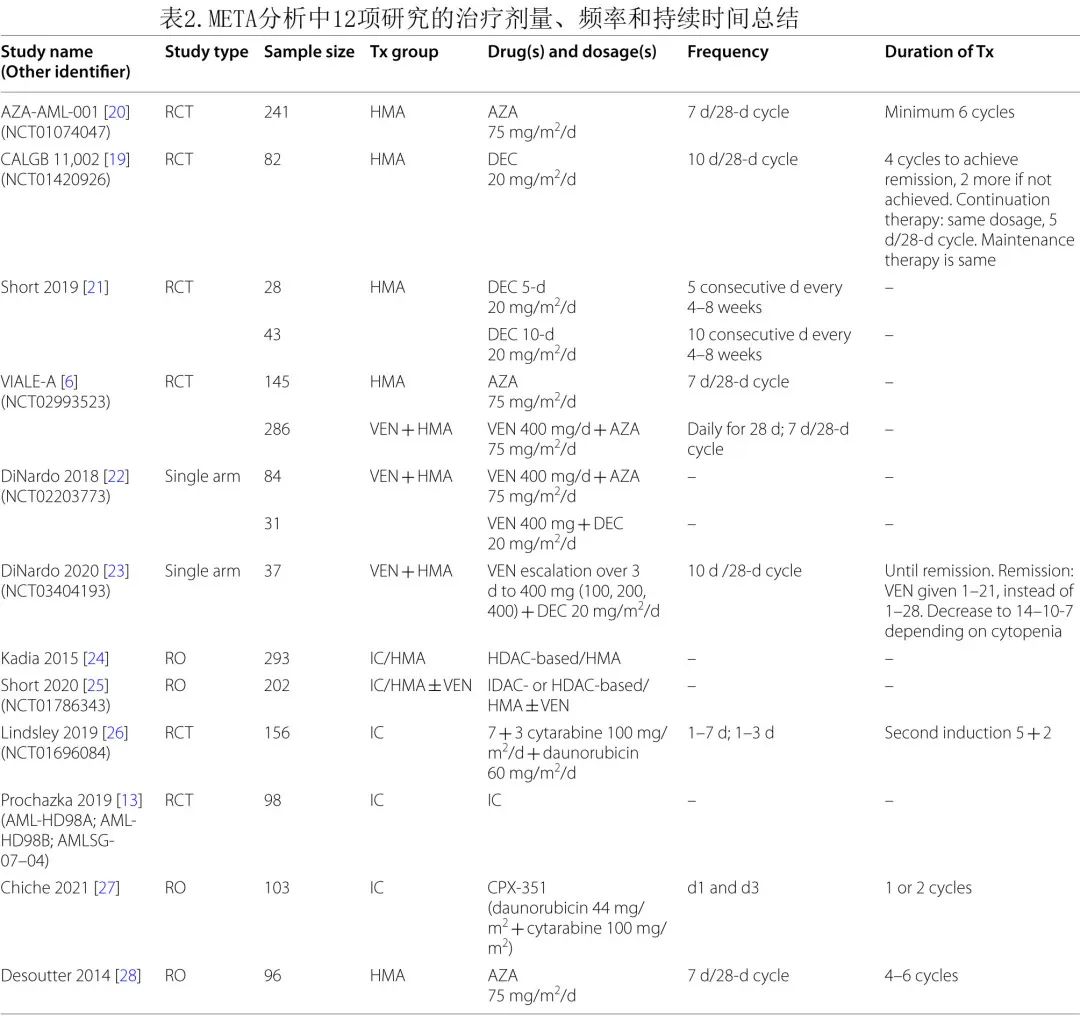
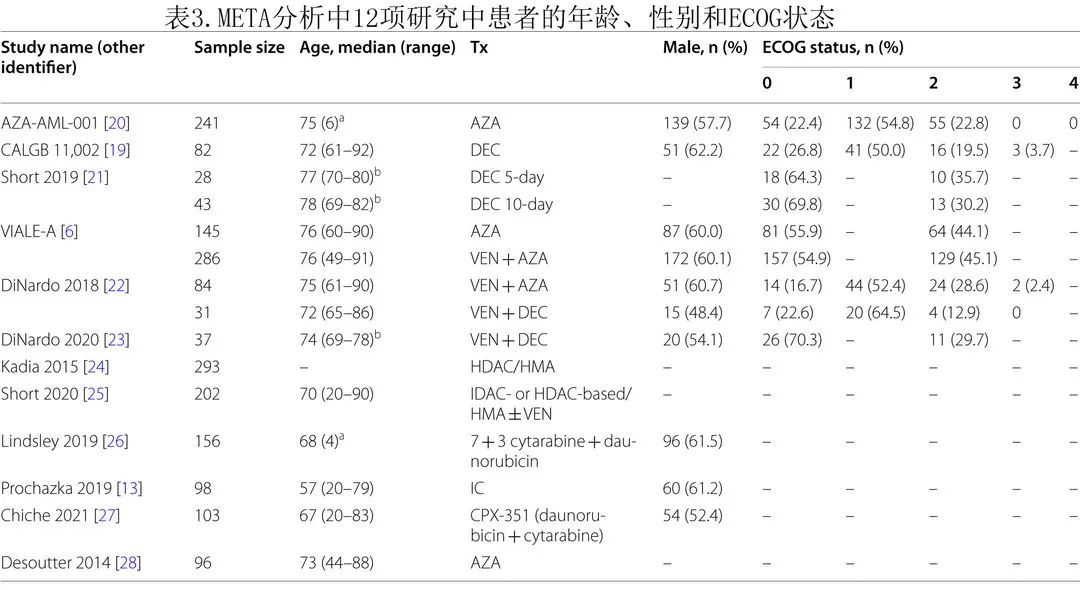
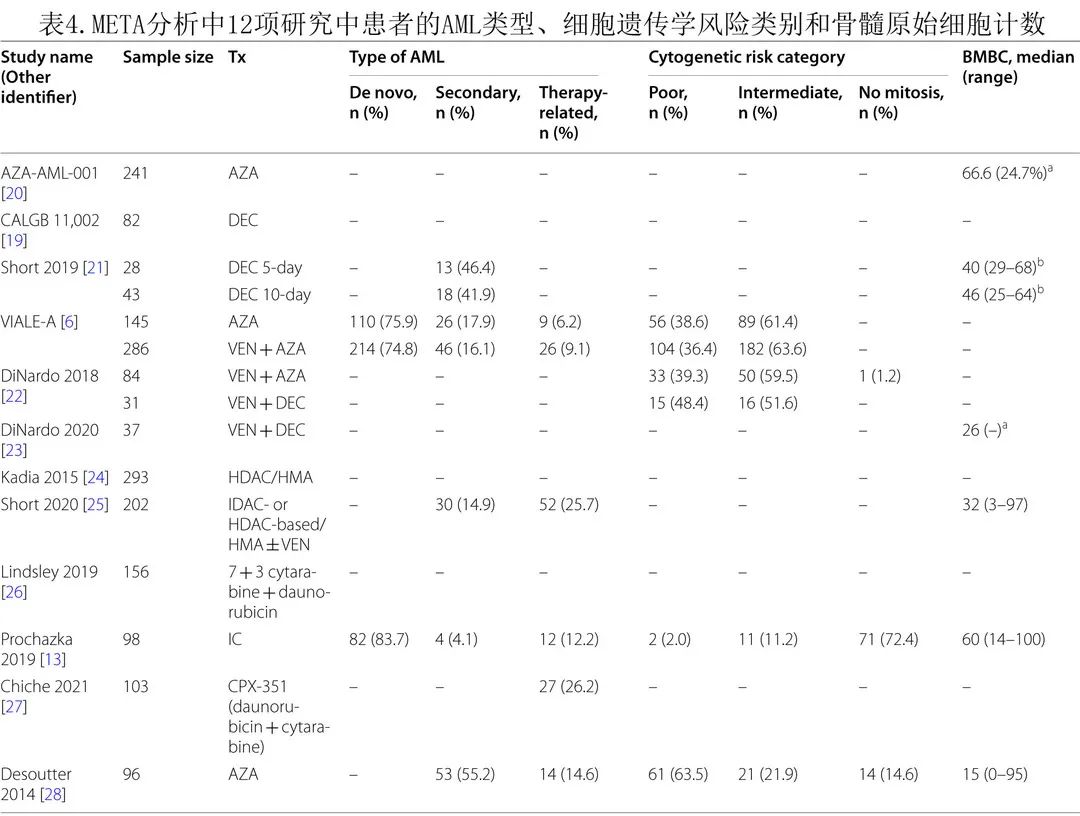
方案、剂量和入组患者人数的详细信息见表2;年龄、性别和ECOG状态见表3;AML类型、细胞遗传学和骨髓原始细胞见表4。
结局
CR:
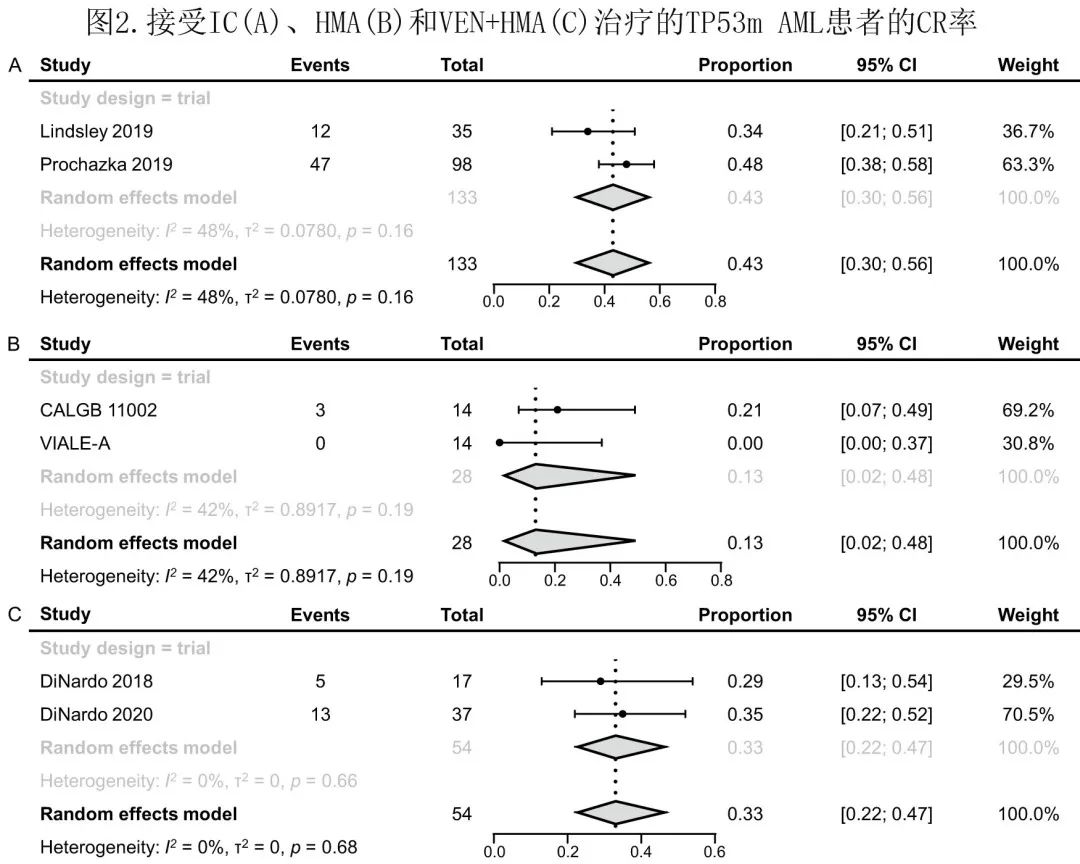
IC 治疗 TP53m AML 患者的两项RCT (N=133) 中 CR 率为34%(总病例N=35)和48% (总病例N=98) (图2A),IC治疗后 CR 的合并率为43%。
HMA 治疗 TP53m AML的2项RCT (N=28) 中CR 率为21% (总病例N=14)和0(总病例N=14),HMA 治疗的合并 CR 率为13% (图2B)。
VEN + HMA的2项RCT (N=54) 的 CR 率为29% (总病例N=17) 和35% (总病例N=37),VEN + HMA的合并 CR 率为33% (图2C)。
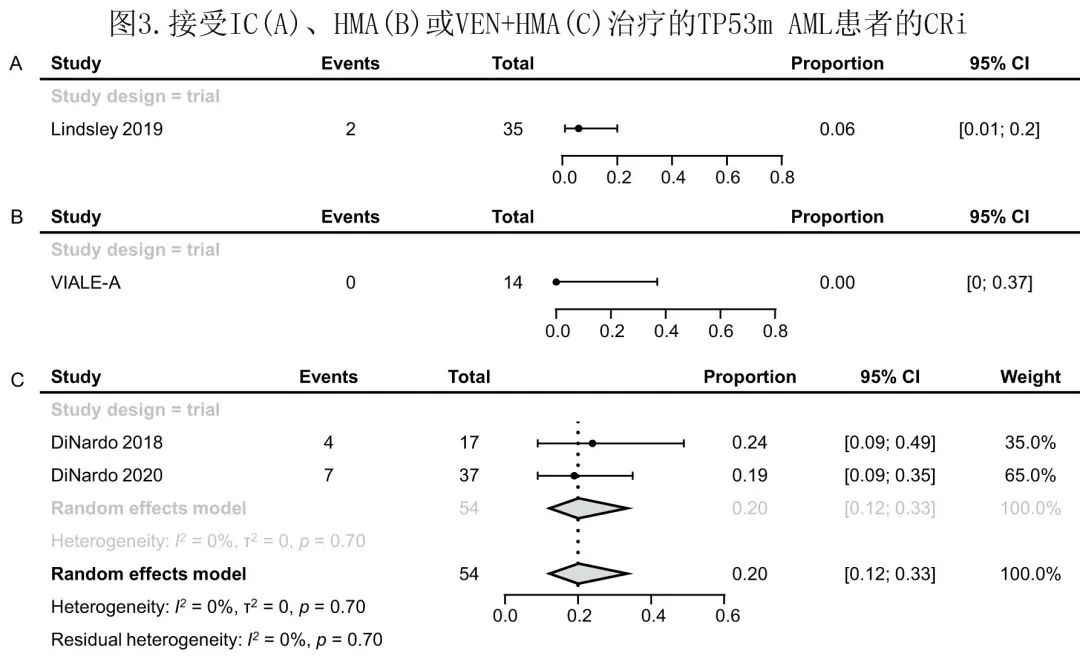
CRi:文献中接受 IC 或 HMA 治疗的患者的 CRi 结果有限。
在1项接受 IC 治疗的患者研究 (N=35) 中2例患者达到CRi (图3A)。
1项单独使用 HMA 治疗TP53m AML的RCT 报告 CRi 率为0 (图3B) 。
VEN + HMA的两项研究 (N=54) 中CRi 率:24% (N=17) 和19%(N=37;图3C),合并率为20%。
CR/CRi:
4项 IC 的研究报告了 CR/CRi 率,其中2项RCT (N=133)的CR/CRi率为40% (N=35) 和48% (N=98),合并率为46%(图4A);两项 IC 的回顾性研究获得了相似的 CR/CRi 率:41% (n=22) 和49% (n=45),合并率为46%;所有4项IC研究的合并 CR/CRi 率为46%。
在研究 HMA 治疗 TP53m AML 的2项RCT (N=28) 中 CR/CRi 率较低,为0(N=14)和21%(N=14;图4B),HMA研究合并CR/CRi 率为13%。
对于VEN +HMA,3项临床试验 (N=92) 的 CR/CRi 率介于53% (N=17) 至55% (N=38),合并 CR/CRi 率为54%(图4C),一项回顾性研究的 CR/CRi 率为31% (n=29),VEN +HMA4项研究合并 CR/CRi 率为49%。

中位OS:TP53m AML中3种治疗的中位 OS 估计值相当(图5)。
评估IC 的2项RCT (N=133) 的中位 OS 为5.1个月(N=35)和6.5个月 (N=98),RCT的合并中位 OS为5.8个月。一项 IC 回顾性研究的中位 OS 估计值较高:8.5个月(N=22)。3项IC研究中合并的中位 OS 为6.5个月。
在2项HMA的RCT (N=34) 中,中位 OS 估计值为4.9个月(N=17)和7.2个月 (N=17)。HMA研究合并的中位 OS 为6.1个月。
VEN +HMA的2项临床试验 (N=73) 的中位 OS 估计值为5.2个月(N=37)和7.2个月(N=36)。VEN +HMA研究合并的中位 OS为6.2个月。

EFS:
2项IC RCT (N=133) 报告了 EFS 估计值,分别为1.6个月(N=35)和5.7个月 (N=98)。IC的合并EFS为3.7个月。
接受 HMA 或VEN +HMA治疗的研究均未报告 EFS 结局。
ORR:IC、HMA和VEN + HMA的单项研究使用不同的定义报告了各研究的ORR,无 ORR 值超过65%。
在一项 IC 回顾性研究 (n=22) 中,ORR(定义为 CR 或CRi)为41%。
HMA RCT(n=17) 报告的 ORR (CR、CRp、CRi或PR)相似,为47%。
VEN +HMA研究 (N=37)的 ORR 为65%,但本研究未定义ORR。
DoR:所有纳入的研究中报告的 DoR 估计值均≤7个月。
一项IC RCT (n=35) 的中位 DoR 为3.5个月。
未发现 HMA 的研究报告中位DoR。
在VEN +HMA的2项临床试验 (N=54) 中观察到中位 DoR 的最高估计值:6.5个月 (N=17) 和3.5个月 (N=37),VEN +HMA的合并 DoR 为5.0个月。达到 CR 的患者的中位 DoR 为7.0个月,而达到 CRi 的患者的中位 DoR 为2.5个月。DiNardo 等的研究中VEN + HMA的 DoR 为3.5个月,但在干细胞移植时未删失患者,因此该信息不可用于其他研究。

对于新诊断的未经治疗TP53m AML 患者,各治疗组(包括IC、HMA和VEN +HMA)的 CR 率、中位 OS 和其他疗效指标均较低。
CR率介于13-43%,CRi介于13-49%,IC 和VEN +HMA的 CR 和 CR/CRi 率优于 HMA单药,但与TP53 野生型 AML 中报告的85%的 CR 率相比仍显较低。IC 的合并 CR/CRi 和 CR 率最高(分别为46%和43%),但可能有选择偏倚。VEN + HMA的合并 CR 率仅为33%,但高于单独 HMA 的 CR 率21%。
尽管与 HMA 单药相比,在 HMA 中添加 VEN 改善了 CR 和 CR/CRi 率,但中位 OS 仍未延长;单用HMA、VEN + HMA和 IC 的中位 OS 仍不理想,分别为6.1、6.2和6.5个月,表明 IC 和VEN + HMA治疗反应的改善并不能转化为 OS 的改善,突出了该髓系恶性肿瘤人群中亟待满足的需求。
基于研究的发现,对于能够有效治疗新诊断、初治 TP53m AML 并改善结局的新疗法仍存在较大需求。
参考文献
Naval G Daver,et al. Treatment outcomes for newly diagnosed, treatment‑naïve TP53‑mutated acute myeloid leukemia: a systematic review and meta‑analysis. J Hematol Oncol . 2023 Mar 6;16(1):19. doi: 10.1186/s13045-023-01417-5.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言