Nature子刊:中山大学赵绮毅/苏士成/廖建友发现机械转导信号调节癌症干细胞的新机理
2023-01-19 iNature iNature 发表于威斯康星
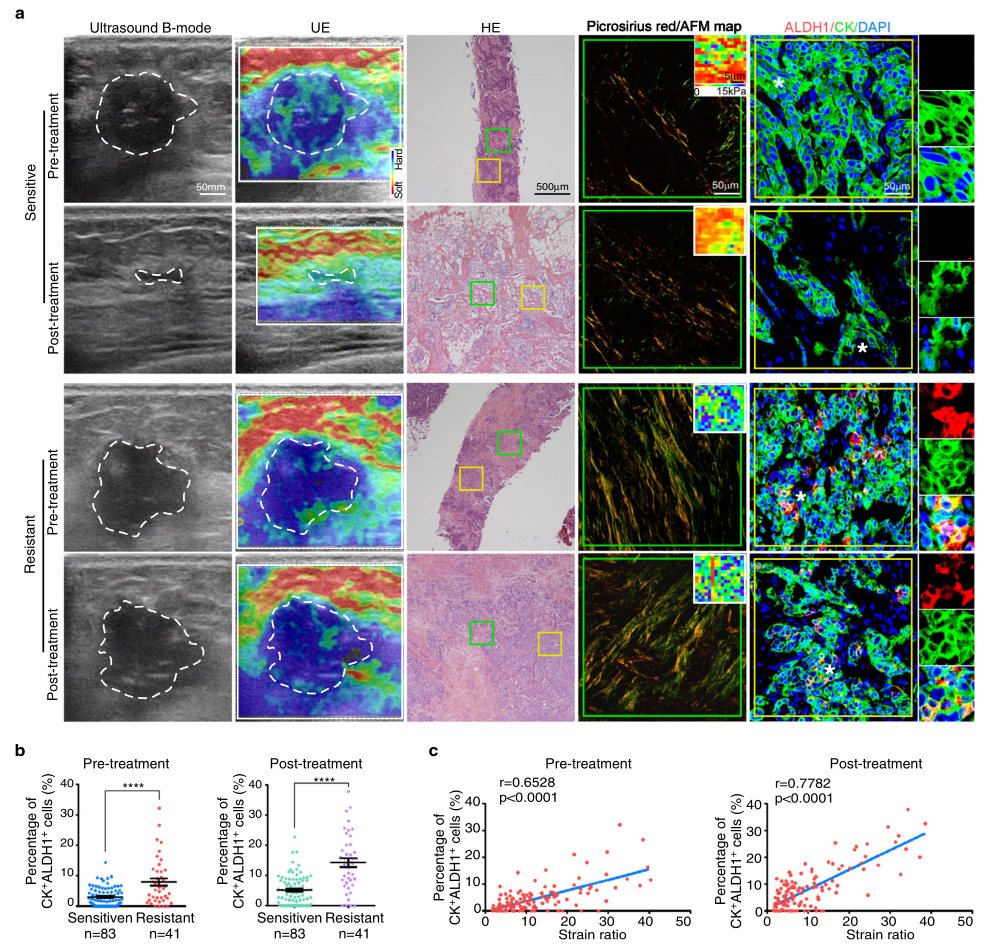
该研究表明生态位刚度通过TAZ和NANOG相分离维持癌症干性。通过对患者病变的临床超声弹性成像和对手术样本的原子力显微镜,作者揭示了基质刚度的增加与乳腺癌患者对新辅助化疗反应差、预后差和CSC丰富有关
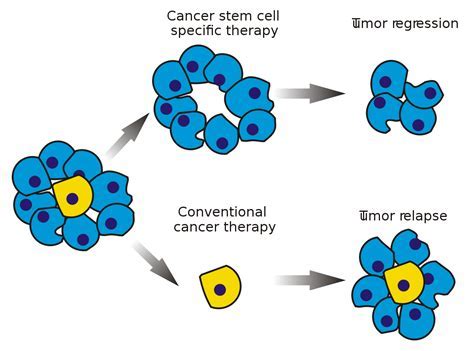
新出现的证据表明,需要生物力学环境来支持癌症干细胞(CSCs),这些干细胞在耐药性中起着至关重要的作用。然而,机械转导信号如何调节CSCs及其临床意义尚不清楚。
2023年1月16日,中山大学赵绮毅、苏士成及廖建友共同通讯在Nature Communications 在线发表题为“Niche stiffness sustains cancer stemness via TAZ and NANOG phase separation”的研究论文,该研究表明生态位刚度通过TAZ和NANOG相分离维持癌症干性。通过对患者病变的临床超声弹性成像和对手术样本的原子力显微镜,作者揭示了基质刚度的增加与乳腺癌患者对新辅助化疗反应差、预后差和CSC丰富有关。
机制上,生物力学激活的TAZ通过与NANOG相分离增强CSC性能。TAZ-NANOG相分离依赖于NANOG N端激活域的酸性残基,促进SOX2和OCT4的转录。在治疗上,靶向NANOG或TAZ可减少CSCs并增强体内的化学敏感性。总的来说,这项研究证明了多能性转录因子的相分离将生态位中的机械线索与CSCs的命运联系起来。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











博士生患癌。
1