颈动脉内膜切除术的麻醉管理要点
2023-05-11 张子银 麻醉MedicalGroup 发表于上海
本文总结归纳一下此种手术在麻醉方面需注意的方面,对于提高麻醉管理水平有些许的帮助。
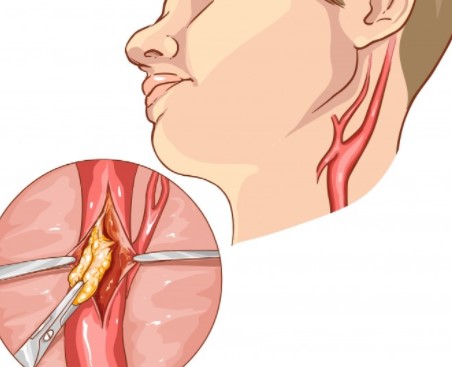
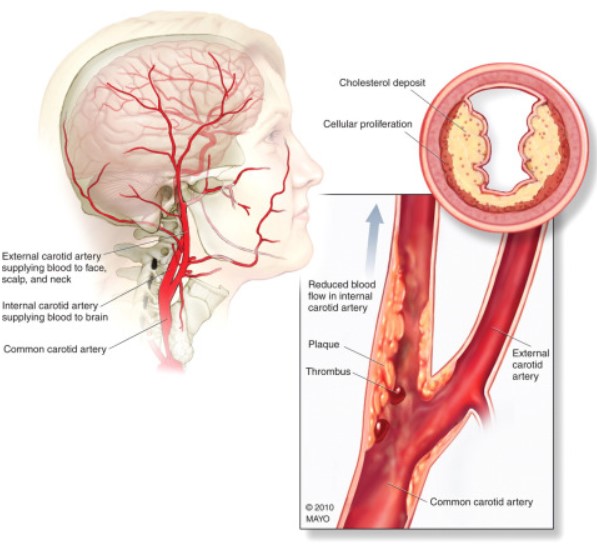
颈动脉粥样硬化是脑卒中的常见原因。常用血运重建方法包括颈动脉内膜切除术(carotid endarterectomy, CEA)和颈动脉支架术(carotid artery stenting, CAS),即经皮CAS和经颈动脉血运重建(transcarotid artery revascularization, TCAR)。下面总结归纳一下此种手术在麻醉方面需注意的方面,对于提高麻醉管理水平有些许的帮助。
术中管理的一般注意事项
麻醉目标 — 无论采用哪种血运重建方法(CEA、经皮CAS、TCAR)和麻醉方法(全身麻醉、局部/区域麻醉),麻醉目标都是:
确保患者在手术结束时能够迅速苏醒并充分配合神经系统检查,以及早发现脑卒中,采用局部/区域麻醉时,患者需能配合术中检查。
避免血压和/或心率在整个手术过程中和术后即刻出现大幅波动。
血流动力学监测 — 由于基线颈动脉压力感受器的功能发生改变和术中操作这些压力感受器,患者的血压和/或心率可能会在CEA、经皮CAS或TCAR的围术期极不稳定。因此,与其他血管外科手术相似,需通过直接动脉血压监测来快速发现并治疗低血压或高血压。动脉内导管还可以指导血管活性药物治疗(即血管加压药和血管扩张药),并在必要时用于血气分析。我们在麻醉诱导前进行动脉置管。进行右侧CEA时,通常选择左侧桡动脉置管,因为手术可能会干扰右侧桡动脉脉搏。
血流动力学管理
药物的准备和使用 — 有必要在整个围术期控制患者的血压。药物治疗包括准备好拟交感神经药、血管扩张药和短效β受体阻滞剂,以快速治疗低血压、高血压、快速性心律失常或缓慢性心律失常。需准备好推注以下药物:
血管加压药和正性肌力药–去氧肾上腺素、麻黄碱、血管加压素
降压药和/或治疗心动过速的药物–尼卡地平、拉贝洛尔、艾司洛尔
治疗或预防心动过缓的药物–阿托品、格隆溴铵
还需准备去氧肾上腺素和硝酸甘油的输注溶液,以便随时取用。
虽然补液可能有助于恢复正常的血容量和血压,但颈动脉手术通常不会引起过多失血、体液丢失或液体外渗。因此,CEA或CAS期间很少需要使用大量液体进行容量复苏。
CEA期间的血流动力学管理 — 无论采用何种颈动脉血运重建技术,全身麻醉的诱导期和苏醒期都有可能出现血流动力学不稳定。在CEA期间,患者最容易出现血流动力学不稳定和/或心肌或脑缺血的时期包括:
对颈动脉窦和颈动脉进行手术操作–在切开颈动脉和对颈动脉窦进行手术操作时,交感神经刺激可能导致心动过速和高血压,或可能增加副交感神经传出而导致心动过缓和低血压。可以将局麻药注入颈动脉体或颈动脉窦周围的外膜周围,以尽量减轻颈动脉操作引起的反射性心动过缓和血流动力学不稳定。但暂无充分数据支持常规使用这种方法。
横断钳闭及松开颈动脉–为了在横断钳闭颈动脉时优化侧支脑灌注,通常会通过连续输注去氧肾上腺素来控制患者的收缩压,使其维持在基线至基线水平的120%(。有些中心会为此监测并维持较高的平均动脉压,而不是处理收缩压。松开颈动脉后,血压可回到基线水平。然而,松开钳闭后的再灌注期可能并发低血压,需予以治疗以维持基线血压。
CEA的麻醉管理
麻醉诱导–与其他心血管疾病患者相似,为削弱喉镜和插管引起的交感神经反应,麻醉诱导时通常联用短效催眠药(如依托咪酯或逐步调整的小剂量丙泊酚)与小剂量阿片类药物(如芬太尼或瑞芬太尼)和/或利多卡因50-100mg。麻醉诱导时常用神经肌肉阻断剂辅助插管。手术过程中不一定要维持肌肉阻断,选用全凭静脉麻醉(total intravenous anesthesia, TIVA)技术时尤其如此,其中的瑞芬太尼足以使患者运动不能。
需注意,麻醉诱导药物可通过以下途径引起低血压:消除交感神经张力、直接降低体循环血管阻力、直接抑制心肌、减少静脉回流或诱发心动过缓。随后的气管插管可能引起交感神经刺激,导致心动过速和高血压。这些血流动力学异常可通过血管活性药物及加深或减少麻醉深度来控制。
麻醉维持–挥发性麻醉和/或TIVA均可用于麻醉维持
挥发性麻醉–若使用挥发性麻醉药进行颈动脉血运重建,建议选择地氟烷或七氟烷,因为手术过程较短时,这些溶解度低于异氟烷的药物有助于患者快速苏醒。如果采用神经监测,通常以≤0.5-1个最低肺泡有效浓度(MAC)的剂量给予挥发性麻醉药,以避免可能会干扰脑缺血检测的信号抑制,应维持这种低浓度麻醉,无需重大调整。
TIVA–颈动脉血运重建期间,也可使用TIVA(如丙泊酚联合瑞芬太尼)来维持全身麻醉。如果采用神经监测,监测团队可能会要求在TIVA期间对挥发性吸入麻醉药的浓度或剂量设限。
苏醒–应避免拔管时刺激气管引起的咳嗽。联用丙泊酚和瑞芬太尼进行TIVA的一大优点在于,其通常能使患者平稳苏醒,几乎不出现咳嗽。也可在麻醉气体清除时给予小剂量瑞芬太尼,或在患者即将苏醒时经静脉给予利多卡因来减轻咳嗽。此外,刺激气管引起的交感神经刺激可能会导致严重高血压,可通过降压药和/或心动过速药物(如尼卡地平、拉贝洛尔、艾司洛尔来治疗。
气道管理 — 全身麻醉下接受CEA的患者通常要气管插管,因为术中的气道管理受限。但我们通常对全身麻醉下接受CAS的患者使用喉罩。
气管内导管(endotracheal tube, ETT)可以开放气道,并在整个手术过程中实现可靠的控制机械通气。然而,放置ETT以及在术中对插管患者进行头部操作可能会诱发交感神经刺激,引起心动过速和高血压,高危患者还可能出现心肌缺血[7]。此外,在麻醉苏醒和气管拔管过程中,咳嗽和高血压可能会导致CEA术后缝线断裂、颈动脉血肿和危及生命的气道受压,或经皮CAS后的股动脉血肿[45]。麻醉苏醒期的血流动力学不稳定可通过以下方式减轻:深度麻醉下拔管,继以苏醒期间进行温和的面罩通气,并持续至患者完全恢复意识和自主通气。
喉罩也可用于CEA的气道管理。喉罩位于声门上,可最大限度减轻气道刺激,因此与气管插管相比,该法在麻醉诱导和苏醒期间引起血流动力学不稳定的可能性更小。但与使用ETT相比,CEA期间喉罩移位的可能性更大。
CEA期间脑缺血的预防
管理血压–颈动脉横断钳闭会减少颈动脉血流,有可能导致同侧脑缺血。在此期间,我们通常会连续输注去氧肾上腺素,以将收缩压维持在基线水平至基线的120%,从而优化侧支脑灌注。即使放置了转流管,该操作也不能省略。发现脑缺血时,可进一步升高血压。有些中心会监测并维持平均动脉压高于基线水平,而不是处理收缩压。
松开颈动脉后,血压可回到基线水平。但松开钳闭后的再灌注期可能并发低血压,需予以治疗以维持基线血压。
颈动脉转流–CEA期间发现脑缺血的外科处理包括放置颈动脉转流管,或评估使用中的颈动脉转流管是否完好。
CEA期间的抗凝 — 推荐在CEA期间抗凝,即在钳闭颈动脉之前静脉推注肝素。肝素的给药策略通常取决于活化凝血时间(activated clotting time, ACT),目标ACT为200-250秒。但很少有资料说明CEA或其他大型血管手术的具体ACT目标,并且颈动脉钳闭的时间一般较短,所以一般不要求麻醉科医师监测ACT。完成CEA操作后,外科医生根据出血风险决定是否使用鱼精蛋白逆转肝素。若需逆转,麻醉科医师必须缓慢给药并监测有无不良反应,如组胺诱发血管扩张引起的低血压或更严重的全身性过敏反应。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言