JCO:新型抗体药物偶联物Dato-DXd在晚期或转移性HR+/HER2-和三阴性乳腺癌患者中的初步疗效及安全性研究
2024-05-09 daikun MedSci原创 发表于上海
该研究旨在评估Dato-DXd在先前治疗的晚期或转移性HR+/HER2-乳腺癌和三阴性乳腺癌患者中的安全性和有效性,Dato-DXd显示出显著的抗肿瘤活性且安全可控。
HR+/HER2-乳腺癌和三阴性乳腺癌是乳腺癌的主要亚型,共占美国乳腺癌病例的80%,尽管近年来治疗方法有所进步,但转移性HR+/HER2-乳腺癌和三阴性乳腺癌的5年生存率仍然较低,对于转移性HR+/HER2-乳腺癌,标准治疗为内分泌治疗联合CDK4/6抑制剂,然而,约10%的患者对CDK4/6抑制剂耐药,大多数患者最终会发展耐药,对于三阴性乳腺癌,化疗仍是标准治疗,但治疗选择有限,针对这两种乳腺癌亚型的治疗需求,抗体药物偶联物(ADCs)作为一种新兴治疗方法,具有提高响应率并降低系统毒性的潜力,因此,Dato-DXd作为一种靶向TROP2的ADC,被用于评估其在先前治疗的晚期或转移性HR+/HER2-乳腺癌和三阴性乳腺癌患者中的安全性和有效性。

方法
该研究是一项I期临床试验:包括剂量爬坡和剂量扩展两部分。纳入了18岁及以上,先前治疗失败的HR+/HER2-乳腺癌或三阴性乳腺癌患者,患者静脉注射Dato-DXd,每21天为一个周期,确定6mg/kg每3周一次为推荐扩展剂量,主要研究终点为Dato-DXd的安全性、耐受性,次要研究终点为Dato-DXd的药代动力学特征、抗肿瘤活性、抗药物抗体发生率等,研究直至不可接受的毒性、疾病进展或患者退出。
研究结果
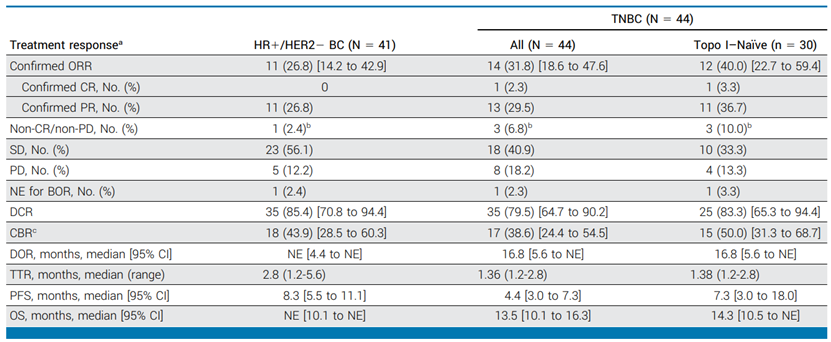
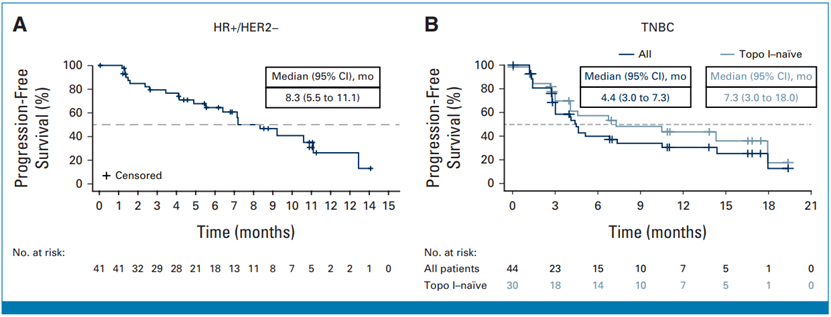
该研究共有85例患者入组,其中HR+/HER2-乳腺癌41例,三阴性乳腺癌44例,患者都接受了6mg/kg每3周一次的Dato-DXd治疗,2例患者接受8mg/kg每3周一次的Dato-DXd治疗。HR+/HER2-乳腺癌:客观响应率26.8%,中位无进展生存期8.3个月;三阴性乳腺癌:客观响应率31.8%,中位无进展生存期4.4个月,在TROP2抑制剂初治的三阴性乳腺癌患者亚组中,客观响应率更高,为40%。所有患者均出现治疗相关不良事件,最常见为口腔炎,严重不良事件发生率较低,最严重为1例三度间质性肺病,物相关不良事件发生率较高,但大多数为轻度至中度。

结论
Dato-DXd显示出显著的抗肿瘤活性,其中HR+/HER2-乳腺癌的客观响应率为26.8%,三阴性乳腺癌的客观响应率为31.8%,在TROP2抑制剂初治的三阴性乳腺癌患者中,Dato-DXd显示出更高的客观响应率,达到40%,Dato-DXd的安全性良好,最常见的不良事件为口腔炎,严重不良事件发生率较低,仅出现1例三度间质性肺病,综上所述,Dato-DXd在晚期HR+/HER2-乳腺癌和三阴性乳腺癌的治疗中具有潜力,目前正在进行III期临床试验进一步评估其效果。
原始出处
Bardia A, et al. 2024. Datopotamab Deruxtecan in Advanced or Metastatic HR+/HER2– and Triple-Negative Breast Cancer: Results From the Phase I TROPION-PanTumor01 Study. Journal of Clinical Oncology:JCO.23.01909.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#三阴性乳腺癌# #抗体药物偶联物# #HR+/HER2-乳腺癌#
7