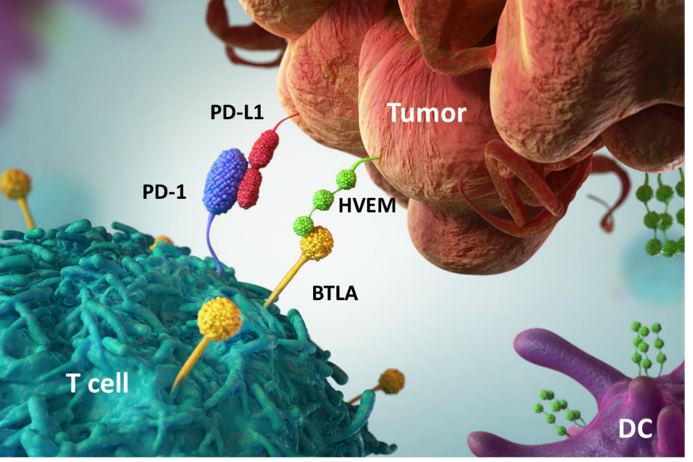
Blood:BV和PD-1的出现改善了R/R cHL自体移植后的结局!
2023-03-06 聊聊血液 网络 发表于上海
自体HCT前含PD-1抑制剂的挽救治疗方案可改善无进展生存期。
大多数经典霍奇金淋巴瘤 (cHL) 患者可通过一线化疗治愈,但有约10-20%会复发,而另外5-10%为原发难治性疾病。对于适合移植的复发或难治性 (R/R) cHL 患者,标准治疗为挽救治疗后自体造血细胞移植 (AHCT),与单独化疗相比AHCT可治愈超过一半的患者,且无进展生存期 (PFS) 更优。AHCT 前通过PET扫描达到代谢完全缓解 (CR) 是与5年 PFS 更好相关的关键预后因素(5年PFS为75%),而残留 PET 阳性患者为31%
近十年该领域的重大变革包括维布妥昔单抗和两个PD-1抑制剂(纳武利尤单抗和帕博利珠单抗)获批治疗R/R cHL,后续也有研究在早期治疗线中评估它们的疗效和安全性,包括AHCT后维持治疗、AHCT前的首次挽救治疗甚至一线治疗等,均证实了三个新药极为重要的地位。
鉴于过去十年的显著发展,斯坦福大学Sally Arai教授牵头评估了该中心共342例接受 AHCT 的 R/R cHL 患者,分为2011-2020年(n=159)与2001-2010年(n=183),两个时期的结局和实践模式的变化,以反映当代新药的使用增加情况。作者还评估了两个时期 PFS 和 OS 的预后因素。文章近日发表于《Blood》。

•在维布妥昔单抗和PD-1抑制剂获批后,复发/难治性霍奇金淋巴瘤自体HCT后的总生存期有所改善
•在多变量分析中,自体HCT前含PD-1抑制剂的挽救治疗方案可改善无进展生存期

纳入2001年9月至2020年12月在斯坦福医院接受AHCT的所有连续R/R cHL患者,使用吉西他滨、长春瑞滨、卡莫司汀(BCNU)、依托泊苷和环磷酰胺(GN-BVC)的统一预处理方案。队列分为两个治疗时期:2001-2010年和2011-2020年,后一个时期(以下简称当代)新药的使用越来越多。研究终点包括OS、PFS以及累积复发率和累积非复发死亡率 (NRM),包括整个队列和不同时期的对比。
患者特征
基线患者特征见表1。
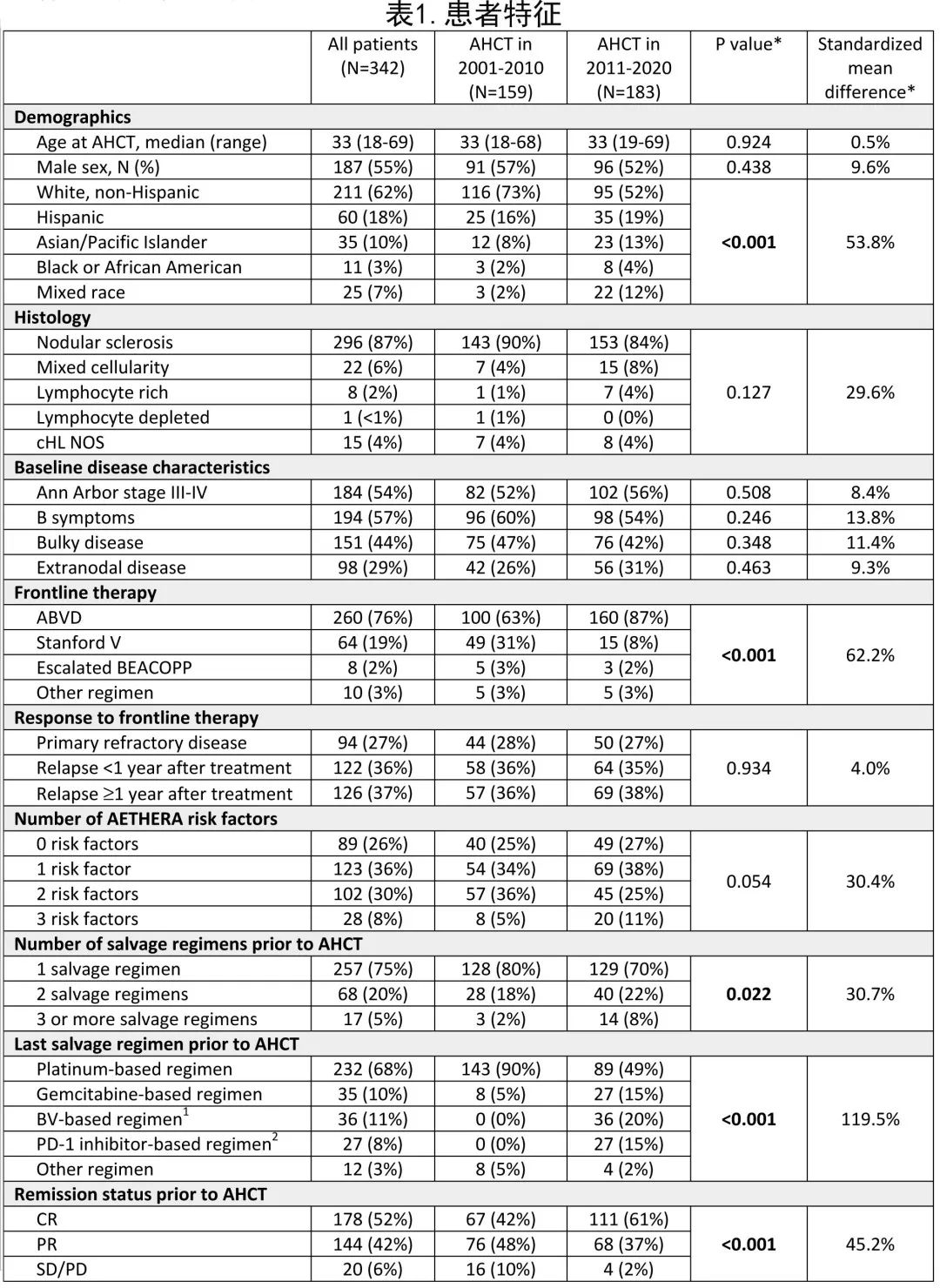
共有342例患者接受了AHCT,包括2001-2010年移植的159例患者和2011-2020年移植的183例患者。AHCT 时的中位年龄为33岁,55%为男性,62%为非西班牙裔白人。人种和种族因时期而异,当代非西班牙裔白人患者接受 AHCT 的比例降低,而亚洲/太平洋岛民和混血儿患者接受 AHCT 的比例增加 (p<0.001)。初诊时两个时期的大多数患者均为晚期疾病和 B 症状。整体队列中大包块病变和结外受累分别占44%和29%。在当代 ABVD 方案使用有所增加,而Stanford V 方案使用减少,一线治疗在不同时期存在差异 (p<0.001)。
74%的患者存在一种或多种AETHERA不良风险因素(原发难治性疾病、CR1持续时间<1年或复发时存在结外病变)。患者在 AHCT 前接受了中位2次全身治疗,25%的患者在 AHCT 前接受了多种挽救治疗方案,且当代有更多的移植患者在 AHCT 前接受了≥2种挽救治疗方案 (p=0.022)。挽救治疗的选择因时期而异,铂类药物化疗的使用显著减少,而BV和/或 PD-1 抑制剂联合治疗方案的使用增加 (p<0.001)。52%的患者在 AHCT 时处于代谢CR,当代 CR 移植的患者百分比较高 (p<0.001)。
不同时期的新药、放疗和alloHCT使用情况
不同时期新药和放疗的使用存在显著差异(表2)。
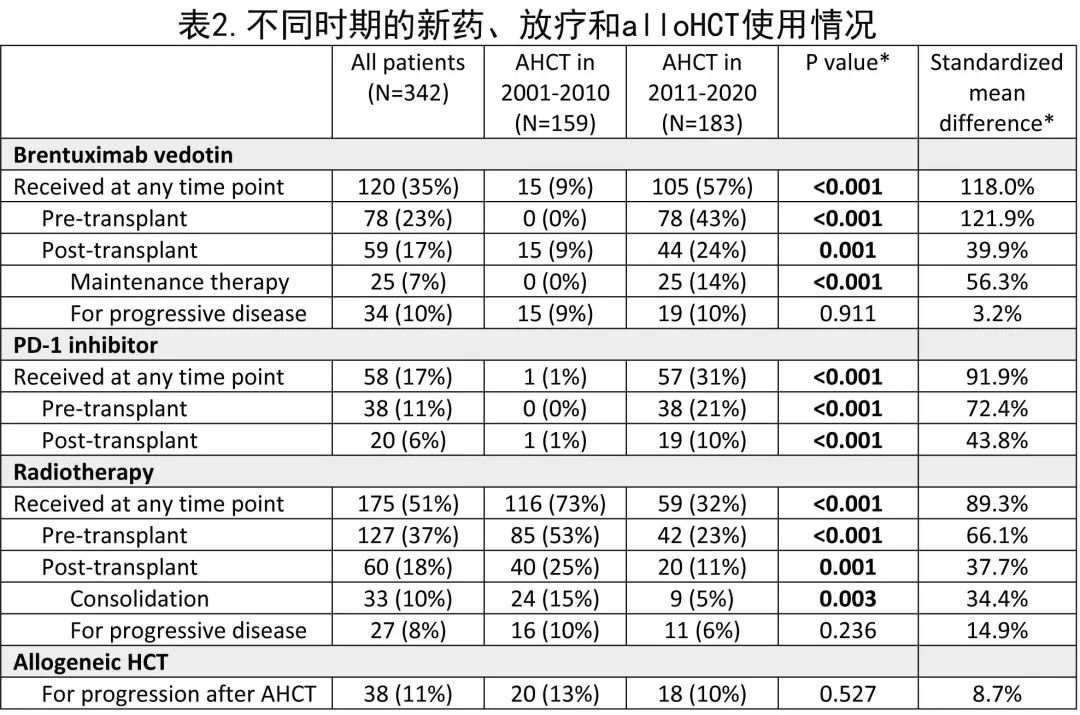
对于当代移植的患者,57%在任何时间点接受BV,而2001-2010年移植的患者仅有9% (p<0.001)。当代移植的患者中有31%接受了 PD-1 抑制剂,而2001-2010年移植的患者中仅有1% (p<0.001);且PD-1抑制剂更常用作 AHCT 前挽救治疗的组成部分。放疗的使用率从73%降至32% (p<0.001),包括移植前放疗和移植后巩固治疗均下降。在2014年采用从累及野放疗 (IFRT) 过渡到累及部位放疗 (ISRT) 后,放疗野尺寸有所减小;不同时期的放疗剂量也从中位数 36 Gy 降至30 Gy。38例患者 (11%) 在 AHCT 后接受了非清髓性alloHCT 治疗PD。此外不同时期的alloHCT 使用无差异 (p = 0.53)。
不同时期的生存、复发和NRM
按不同时期分层的患者结局见图1。

整个队列的中位随访时间为5.9年(2001-2010年移植患者为11.6年,2011-2020年为4.0年),其中当代移植患者的OS更优(4年OS 89.1% vs 79.0%,HR=0.53,95%CI 0.33-0.85,p=0.011),但PFS无统计学显著差异(4年PFS 73.1% vs 63.3%,HR=0.75,95%CI 0.53-1.07,p=0.11)。考虑到当代 CR 时移植患者的百分比较高,因此分别评估了AHCT前CR和PR患者的结局,结果不同时期 CR 时移植患者的 OS 和 PFS 无差异,但 PR 时移植患者中当代的 OS 更优(4年OS 88.2% vs 74.6%,HR=0.47,95%CI 0.24-0.92,p=0.042)。在这两个时期,大多数 PR 移植患者在 AHCT 后转化为CR (2011-2020年和2001-2010年分别为60.3%和52.6%)。不同时期的累积复发率无差异(4年估计值23.9% vs 30.5%,p=0.39),早期 NRM 也相似(1年估计值2.5% vs 2.8%),但当代的移植后2年 NRM 有降低趋势(4年估计值3.6% vs 7.0%,p=0.082)
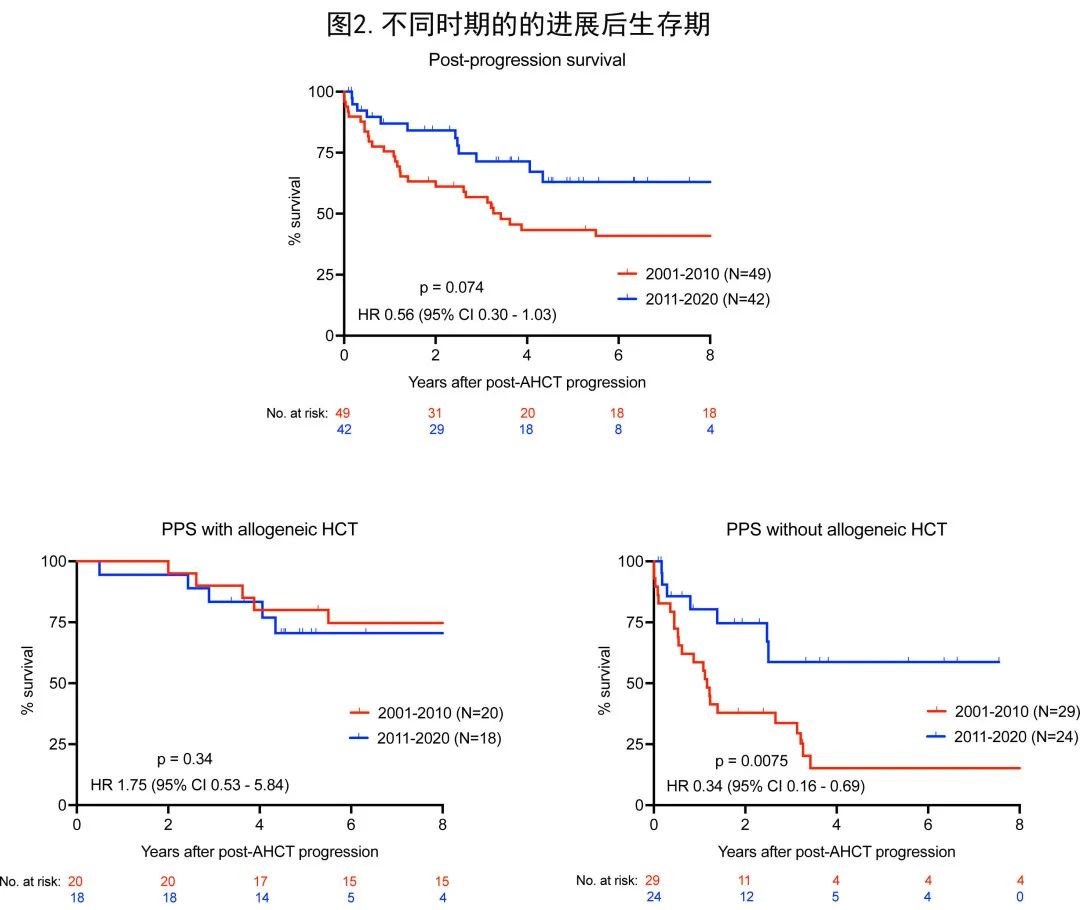
不同时期的进展后生存期
2001-2010年队列中49例患者 (31%) 在 AHCT 后进展,2011-2020年队列中42例患者 (23%) 进展。当代更多的移植患者接受了 BV (45% vs 31%) 和 PD-1 抑制剂 (45% vs 4%) 用于治疗 AHCT 后复发,而不同时期接受后续alloHCT 的比例相似 (43% vs 41%)。在 AHCT 后进展的患者中,当代的 PPS 有延长的趋势(4年PPS 71.4% vs 43.3%,HR=0.56,95%CI 0.30-1.03,p=0.074)(图2)。对于接受后续alloHCT 的患者,不同时期的 PPS 也相似(4年 PPS 为83.3% vs. 80.0%,p=0.20);但在未接受alloHCT 的患者中,当代的 PPS 更优(4年PPS 58.8% vs 15.2%,HR=0.34,95%CI 0.16-0.69,p=0.0075)。
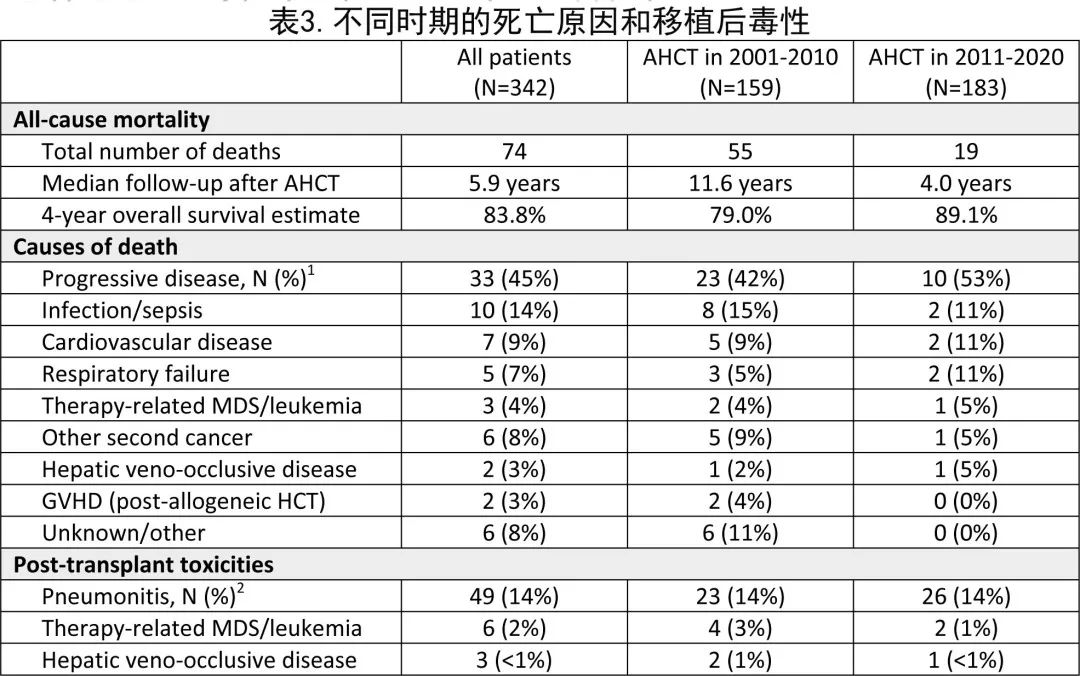
死亡原因和治疗相关毒性
死亡原因和显著的治疗相关毒性总结见表3。两个时期中大多数患者死于PD。NRM 的主要原因包括感染/败血症、心血管疾病和第二肿瘤。19例患者 (5.6%) 发生第二肿瘤,最常见的第二肿瘤包括治疗相关 MDS 或急性白血病以及骨或软组织肉瘤,分别发生在1.8%和0.9%的患者中。14%的患者在 AHCT 后100天内发生需要皮质类固醇治疗的肺炎,大多数归因于BCNU。在 AHCT 前接受基于 PD-1 抑制剂的挽救治疗方案的27例患者中,5例患者 (19%) 发生移植后肺炎。其他具有临床意义的免疫相关不良事件包括需要甲状腺激素替代治疗的甲状腺炎 (N=4)、炎性关节炎 (N=3)、新发1型糖尿病 (N=2) 和炎性结肠炎 (N=2)。肝脏 VOD 罕见(<1%)。
PFS和OS的预后因素
在单变量分析中,初始的无病间期、AHCT前的缓解状态、AETHERA风险因素数量和 AHCT 前的挽救治疗类型是 PFS 的预后因素(图3)。
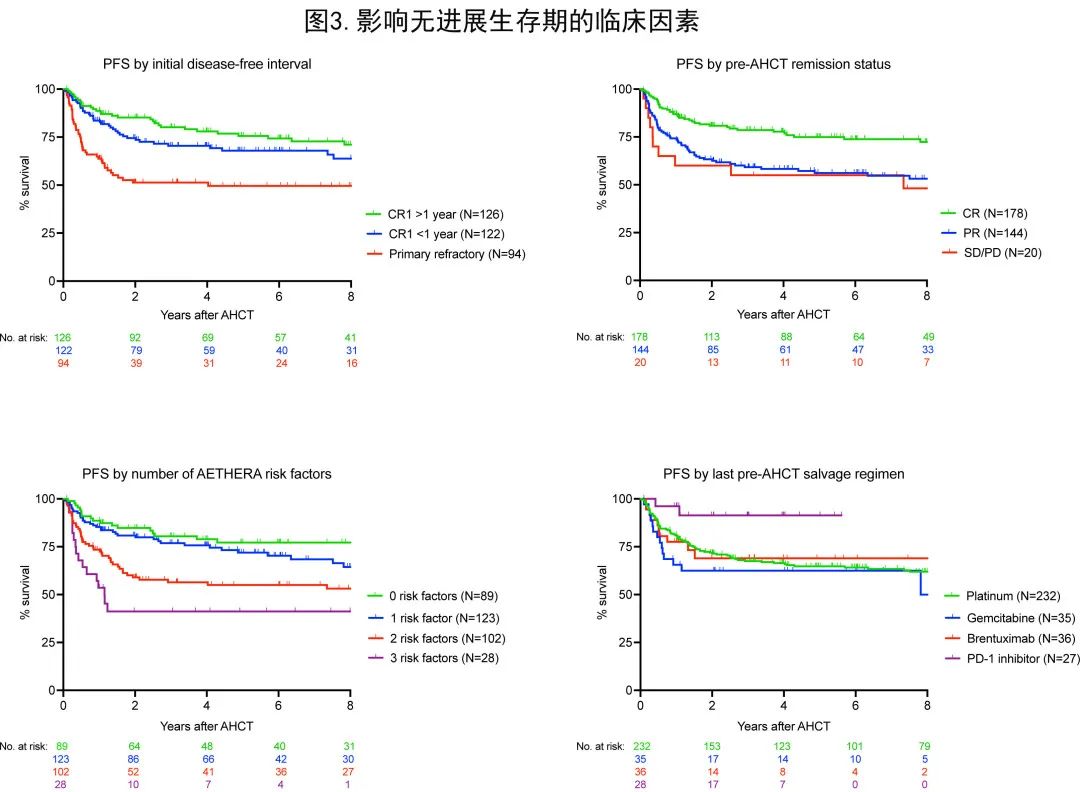
对于CR1 > 1年、CR1 < 1年和原发难治性疾病患者,4年 PFS 估计值分别为78.0%、70.5%和51.3% (p=0.0002)。对于 AHCT 前达到CR、PR或疾病稳定 (SD)/PD 的患者,4年 PFS 估计值分别为77.7%、58.3%和55.0% (p=0.0008)。AETHERA 风险因素(0、1、2或3)的数量也具有很强的预后性,4年 PFS 估计值分别为78.9%、75.8%、55.0%和41.2% (p<0.0001)。根据 AHCT 前即刻给予的挽救治疗方案类型比较结局,包括铂类、吉西他滨、BV和含PD-1 抑制剂方案:接受含 PD-1 抑制剂方案的患者的 PFS 显著高于接受含铂类药物化疗的患者(4年PFS率91.3% vs 66.4%,p=0.026),而接受吉西他滨或 BV 方案的患者的 PFS 与接受铂类化疗的患者相似。
在2001-2010年移植患者的多变量分析中,对 PFS 有显著影响的变量包括原发难治性疾病 (HR=0.97,95%CI 1.35-6.54,p=0.0068) 和接受≥2种挽救治疗方案 (HR=4.55,95%CI 2.10-9.89,p=0.00013);而年龄≥45岁与 OS 较差相关 (HR=2.06,95%CI 1.16-3.65,p=0.013)。在当代移植患者的多变量分析中有4个变量对 PFS 有显著影响:年龄≥45岁 (HR=1.96,95%CI 1.01-3.84,p=0.049)、原发难治性疾病 (HR=2.58,95%CI 1.44-4.63,p=0.0014)、AHCT前未达到CR(HR=1.93,95%CI 1.06-3.50,p=0.031)、AHCT 前接受含 PD-1 抑制剂的治疗方案 (HR=0.21,95%CI 0.05-0.80,p=0.030)(表4)。在当代,复发时有结外病变与 OS 较差相关 (HR=3.12,95%CI 1.25-7.77,p=0.014)。


在 BV 和 PD-1 抑制剂获批后,过去十年中R/R cHL的治疗现状发生了显著变化,目前在 AHCT 前有许多挽救治疗选择,且移植后巩固治疗和复发的治疗也有新的有效选择。本研究为当代移植的 R/R cHL 患者的结局提供了一个新的基准, 4年 PFS 和 OS 估计值分别达到惊人的73%和89%。本研究证明,在过去十年中,使用相同的预处理方案进行 AHCT 后的OS较先前也有显著改善,其中的因素包括: (1) 更有效的挽救治疗方案,尤其是结合免疫治疗(PD-1抑制剂)的方案,可以在 AHCT 前更好地控制疾病,(2) 治疗移植后复发更有效,(3) 移植后2年以上 NRM 有降低的趋势。
参考文献
Michael A Spinner,et al. Improved outcomes for relapsed/refractory Hodgkin lymphoma after autologous transplantation in the era of novel agents. Blood . 2023 Mar 1;blood.2022018827. doi: 10.1182/blood.2022018827.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言