首次发现人肺细胞中形成的“杂交”病毒!更易感且可逃避免疫系统
2022-11-08 生物探索 生物探索
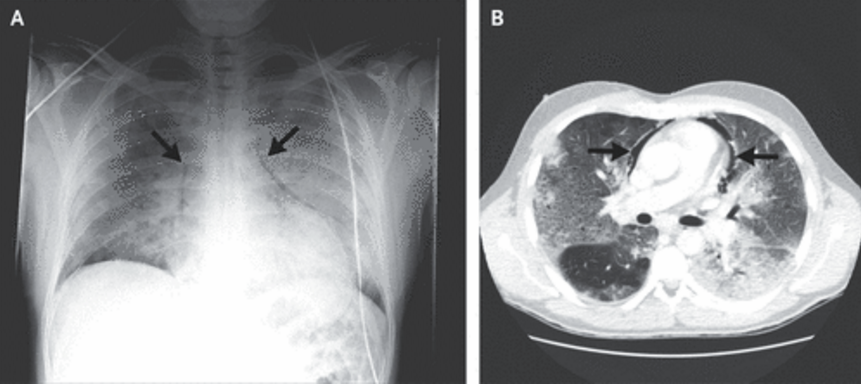
一个人同时感染两种病毒,也即合并感染,占所有呼吸道病毒感染的10-30%,且在儿童中尤为常见。但病毒合并感染会产生怎样的临床结果,目前仍不清楚。
导语:呼吸道病毒之间的相互作用会影响病毒的传播以及临床结果。为了在细胞水平上识别和表征病毒之间的相互作用,研究人员将人类肺细胞与甲型流感病毒(IAV)和呼吸道合胞病毒(RSV)共感染,发现混合病毒颗粒(HVP)含有IVA和RSV的表面糖蛋白和核糖核蛋白,表明以上两种病毒“杂交”形成了一种新型病毒病原体。这一“杂交”病毒不仅可逃避免疫系统,而且更易感染人类。
一个人同时感染两种病毒,也即合并感染,占所有呼吸道病毒感染的10-30%,且在儿童中尤为常见。但病毒合并感染会产生怎样的临床结果,目前仍不清楚。共感染细胞内病毒之间的相互作用可能会导致其病毒后代发生变化,包括但不限于假型或基因组重排,可能会产生具有大流行潜力的新毒株例如SARS-CoV-2和大流行性甲型流感病毒。
每年全球约有500人因IAV住院,而RSV是5岁以下儿童急性下呼吸道感染的主要原因,并可能导致部分儿童出现严重性疾病。为了研究共感染期间病毒的相互作用,在最近一项研究中,研究人员用两种常见呼吸道病毒IAV和RSV的混合接种物感染了人类肺细胞。研究发现,这两种病毒并没有像其他一些已知病毒那样互相竞争,而是相互融合形成了一种圈子内的混合病毒。合并感染后形成的杂交病毒是棕榈树状的,RSV形成了新病毒的树干,IAV形成了新病毒的叶子。相关研究结果以“Coinfection by influenza A virus and respiratory syncytial virus produces hybrid virus particles”为题,发表在Nature Microbiology上。
 研究人员发现,在两种病毒共感染期间存在具有IAV和RSV糖蛋白的出芽病毒细丝。为了确定这一丝状结构的具体细节,研究人员进行了低温电子断层扫描,并观察到与含有IAV和RSV元素的混合病毒颗粒一致的结构。
研究人员发现,在两种病毒共感染期间存在具有IAV和RSV糖蛋白的出芽病毒细丝。为了确定这一丝状结构的具体细节,研究人员进行了低温电子断层扫描,并观察到与含有IAV和RSV元素的混合病毒颗粒一致的结构。
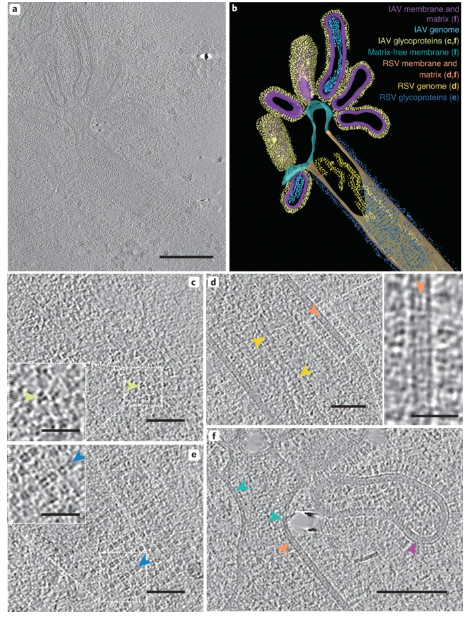 图2 混合病毒颗粒包含IAV和RSV样结构区域(图源:[1])
图2 混合病毒颗粒包含IAV和RSV样结构区域(图源:[1])
通过对混合病毒颗粒进行观察鉴定,研究人员发现,病毒共感染可导致形成在结构上与任一亲本病毒类型不同的两类杂合病毒颗粒。
由于表面糖蛋白决定抗原性和趋向性,假设混合病毒颗粒会显示出抗原性的改变。为了测试这一点,研究人员首先比较了抗IAV HA抗体对从从单独感染IAV或同时感染IAV和RSV的细胞中收集的病毒的中和效率。与从单一IAV感染细胞中收集的病毒相比,从共感染细胞中收集的病毒显示出IAV中和减少。中和效率的下降在共感染细胞中尤为显著,其中只有33%IAV被中和,表明该部分中三分之二的IAV能够逃避抗体介导的中和。比较抗 RSV F 抗体对从单独感染 RSV 或合并感染的细胞中收集的病毒的中和效率,发现单一感染和混合感染细胞中的RSV被有效中和。这表明,与IAV相比,RSV不能利用IAV糖蛋白来促进病毒进入。此外,在传染性方面,研究人员发现混合病毒可以介导IAV在难治性细胞群中的传播。
接着,研究人员用这两种病毒共感染了分化的原代人支气管上皮细胞,以检查IAV和RSV在原代人支气管上皮细胞中的传播,对单个共感染细胞的分析显示,IAV和RSV抗原在共感染细胞顶端表面和细胞质内均呈双重染色,为IAV和RSV之间的相互作用和混合病毒颗粒的形成提供了机会。
综上,这项研究表征了IAV和RSV两种病毒在细胞间的相互作用,在病毒共感染中可以产生由两种亲本病毒的结构、基因组和功能成分组成的传染性混合病毒颗粒。并且,合并感染产生的病毒具有改变的抗原性和扩大的嗜性。
研究人员还发现,RSV F介导混合病毒颗粒的进入,表明在合并感染的情况下,IAV可以借助于不相关病毒的糖蛋白作为其功能性包膜蛋白,这一特性可能会促进宿主内传播到呼吸道区域,进而可能会影响到发病机制和疾病结果。比如,混合病毒颗粒可以使IAV在扩散到下呼吸道的同时逃脱粘膜抗体,随后可能出现并发症,包括病毒性肺炎。
研究人员认为,混合病毒颗粒的形成在多轮感染中得以维持,并且其反过来也促进了IAV在难治性细胞群中的传播。IAV在共感染过程中不仅感染能力增强,其还可以借助于RSV逃避免疫系统,增加感染可能性。利兹大学的病毒学家斯蒂芬格里芬博士表示,这可能会增加流感引发严重甚至致命的病毒性肺炎的机会。
这种研究发现在一定程度上可能有助于解释病毒混合感染为什么会导致更严重,甚至是致命的病毒性肺炎和难治性肺炎。下一步研究工作是确认混合病毒是否可以在合并感染的患者体内形成,并确定这些病毒的具体种类。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言