Sunvozertinib 在 EGFR 外显子 20 突变的 NSCLC 中展示了早期安全性和有效性
2022-10-30 网络 网络
约2%的非小细胞肺癌(NSCLC)患者中检测到表皮生长因子受体外显子20插入突变(EGFR exon20ins)。由于缺乏有效的治疗,这些患者的预后很差。Sunvozertinib(DZD9008)是
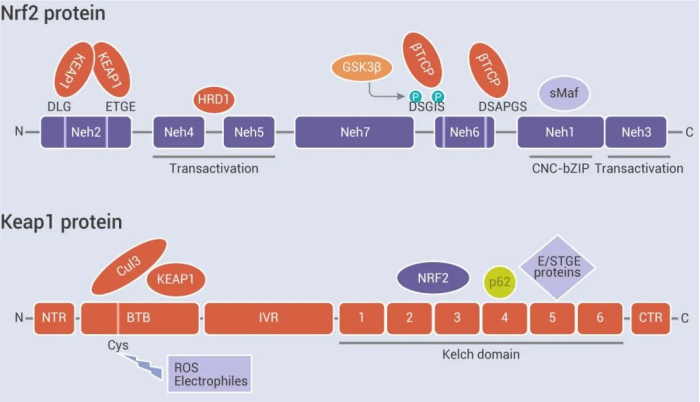
约2%的非小细胞肺癌(NSCLC)患者中检测到表皮生长因子受体外显子20插入突变(EGFR exon20ins)。由于缺乏有效的治疗,这些患者的预后很差。Sunvozertinib(DZD9008)是一种口服、高效、不可逆的选择性EGFR酪氨酸激酶抑制剂,是针对EGFR/HER2 20号外显子插入突变设计的全球首创小分子化合物,对EGFR 20号外显子插入突变在内的多种EGFR突变和HER2 20号外显子插入突变都有较强活性。
在细胞系和异种移植模型中,Sunvozertinib显示出强大的抗肿瘤活性。在两项正在进行的1期临床研究中,Sunvozertinib人体最大耐受剂量是400 mg,每日一次。最常见的药物相关不良反应是腹泻和皮疹。在治疗剂量 ≥100 mg时,显示出对各种EGFR exon20ins突变亚型的患者有效,并在Amivantamab治疗后及基线有脑转移的患者中均显示疗效。中位反应持续时间(DoR)尚未达到。
据医学博士 D. Ross Camidge 称,Sunvozertinib (DZD9008) 作为二线或后线治疗对携带 EGFR 外显子 20 插入突变的非小细胞肺癌 (NSCLC) 患者产生了有希望的反应,他补充说,进一步需要进行调查以探索该药剂的长期益处、其中枢神经系统 (CNS) 活动以及它在西方人群中的表现。
DZD9008正在进行两项 I 期临床研究(WU-KONG1和WU-KONG2)。WU-KONG1正在美国、澳大利亚、韩国和中国台湾进行,WU-KONG2正在中国内地进行。WU-KONG6数据在ESMO上提交。
如果患者患有带有EGFR或HER2突变(包括EGFR 20ins)的局部晚期或转移性非小细胞肺癌,并且在之前的标准治疗中复发,且疾病可通过放射学测量,则符合研究条件。由于这两项研究的关键研究设计相似,研究人员进行了合并分析,以评估安全性、药代动力学和抗肿瘤疗效。
2019年7月9日至2021年4月3日,102例EGFR或HER2突变NSCLC患者接受了DZD9008治疗,其中54例和48例患者分别来自WU-KONG1和WU-KONG2研究。43例、54例和5例患者分别被纳入剂量递增组、剂量扩展组和食物效应组。102例患者中62例(60.8%)携带EGFR 20ins。
截至2021年4月3日,剂量递增队列的注册已完成,食物效应和剂量扩展队列仍在开放中。在剂量递增队列中,探索了DZD9008的五个剂量水平:50、100、200、300和 400 mg,每日一次。基于剂量递增队列中的安全性、耐受性、药代动力学和疗效信号,选择三个剂量水平(200、300和400 mg)进行扩展。在数据截止日期,剂量递增、剂量扩展或食物效应队列中分别有 6、28和3例患者仍在接受DZD9008治疗。
入组患者的人群特征包括:中位年龄为59岁,102例患者中有57例(55.9%)为女性,101例患者(99%)的ECOG评分≤1。先前治疗的中位线为3,93例患者(91.2%)至少接受过一线化疗。102例患者的突变类型包括EGFR 20ins(61%)、EGFR致敏突变(4%)、EGFR T790M(1%)、EGFR致敏/T790M双突变(6% )、EGFR罕见点突变(1%)和HER2 20ins(28%)。
在56例可评估疗效的EGFR 20 ins患者中,在剂量≥100 mg时观察到部分缓解(PR)。在所有剂量水平下,客观缓解率(ORR)为37.5%;部分缓解(PR)率为37.5%,疾病稳定(SD)率为48.2%,疾病进展(PD)率为14.3%。疾病控制(DCR)率为85.7%。
当推荐的II期剂量(PR2D)为200mg(n=11)和300mg(n=31)时,ORR分别为45.5%和41.9%;PR分别为45.5%和41.9%,SD分别为36.4%和48.4%,PD分别为18.2%和9.7%。DCR分别为81.8%和90.3%。
当剂量为400mg时,ORR为22.2%;PR为22.2%,SD为55.5%,PD为22.2%。DCR为77.7%。
在 2022 年 ESMO 大会上提交的 2 期 WU-KONG6 试验 (CTR20211009) 的数据显示,每天接受 300 mg sunvozertinib (n = 97) 的患者的总体缓解率 (ORR) 为 59.8%。在经预处理的基线 CNS 转移患者 (n = 31) 中,使用该药物达到的 ORR 为 48.4%。
Camidge 补充说,必须在未经治疗的脑转移患者中评估 sunvozertinib,以充分了解其 CNS 活性。由于最长的反应持续时间(DOR)超过 9.7 个月,并且未达到中位 DOR,他补充说,需要进一步的随访来评估药物的持久性。
Camidge认为sunvozertinib 在携带 EGFR 外显子 20 插入突变的 NSCLC 患者中的潜在效用、使用该药物观察到的疗效和安全性数据以及未来的研究方向。
国内其它EGFR 外显子 20 插入突变的药物:
 图注:EGFR 20 ins突变靶向药物临床数据
图注:EGFR 20 ins突变靶向药物临床数据
原始出处:
Wang M, Yang JC-H, Mitchell P, et al. Sunvozertinib for NSCLC patients with EGFR exon 20 insertion mutations: Preliminary analysis of WU-KONG6, the first pivotal study. Ann Oncol. 2022;33(suppl 7):S1003-S1004. doi:10.1016/j.annonc.2022.07.1114
https://www.sohu.com/a/567489188_100199817
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言