J Clin Invest:全新研究找到HIV“隐藏蓄水池”的秘密,或能将HIV一网打尽!
2018-01-24 佚名 来宝网
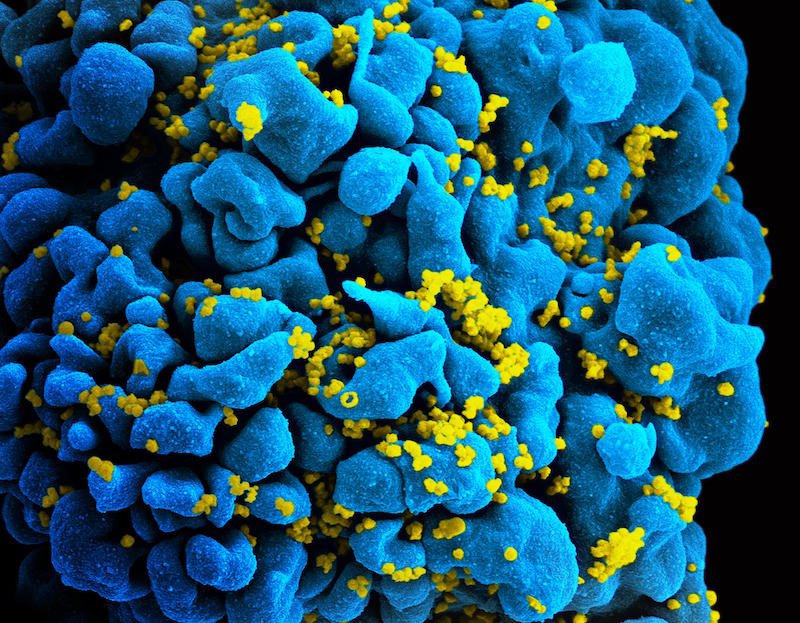
最近一项旨在消除艾滋病病毒的“踢杀”研究揭示了寻找治疗方法的潜在障碍。乔治华盛顿大学的研究人员最近的一项研究发现,潜伏的HIV蓄水池对CD8 T细胞有抵抗力,CD8 T细胞是一种白细胞,其主要功能是杀死受感染的细胞。
“我们已经发现了一个障碍,现在很难理解这个障碍的本质。我们用我们最强大的组合来对付这些细胞,当尘埃落定时,我们发现病毒的存在水平和最初的水平一样高。”
艾滋病治疗目前包括终身抗逆转录病毒治疗,而寻求治疗的工作仍在继续。这种病毒的持久性、潜伏性蓄积使其难以治愈感染。为了根除这些HIV蓄积物,研究人员必须找到一种方法来消除具有整合HIV供应的细胞的持久性种群。“踢杀”模式的目的是将延迟逆转剂与免疫效应结合起来,唤醒病毒并杀死重新激活的细胞。
这项发表在《临床研究杂志》上的研究发现,潜伏的HIV蓄水池对CD8-T细胞表现出内在的抵抗力。与其他使用工程细胞的HIV模型的研究不同,GW的研究小组使用HIV感染者的CD8 T细胞,结合LRAs攻击,并杀死受感染的细胞。
结果表明,受复制能力强的HIV感染的细胞对T细胞具有内在的抵抗力,这是治疗HIV的障碍。然而,研究人员对艾滋病研究的未来持乐观态度,并相信这项研究的结果将有助于提高研究人员对如何处理艾滋病病毒的理解。
研究人员说:“虽然结果肯定不是我们所希望的,但我们已经确定了在杀死感染艾滋病毒的细胞方面可能存在一个重要障碍,既然我们有了研究它的方法,就有理由认为我们可能会比以前的研究取得更大的成功。”
他的团队将继续努力,希望能够理解对CD8-T细胞的抗药性的原因。他们还将研究不同的联合疗法,观察那些可能对减少HIV感染细胞有效的其他情况下使用的疗法。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#EST#
33