Sci Adv:突破!无创MRIgFUS挽救阿尔茨海默病有绝招
2022-12-17 brainnew神内神外 brainnew神内神外 发表于安徽省
基于聚焦超声运载的选择性TrkA 激动剂挽救AD胆碱能功能
胆碱能神经元退化是阿尔茨海默病(Alzheimer’s Disease, AD)的重要病理特征。在动物损伤和衰老模型中,神经生长因子(nerve growth factor, NGF)通过绑定原肌球蛋白受体酶A(tropomyosin receptor kinase A, TrkA)和神经营养蛋白受体(p75 neurotrophin receptor, p75NTR)增强胆碱能细胞的存活、生长及突触可塑性,从而参与记忆的提升。但是在AD病理状态下,NGF相关疗法尚未达到胆碱能神经元再生潜力。多伦多大学I.Aubert团队在Science Advances发文表明,刺激TrkA受体并无p75NTR受体激活,是NGF疗法起效的关键。

(一)在AD最早期, NGF的表达和运输、受体表达、及下游信号成份的激活等变化导致胆碱能神经传递受损,继而造成AD晚期神经元变性。6、8月NGF和TrkA缺乏的TgCRND8小鼠中,内侧隔/Broca斜角带 (medial septum/diagonal band of Broca ,MS/DBB)及meynert基底核(nucleus basalis of Meynert,NBM)NGF蛋白水平下降。选择性TrkA激动剂D3处理的小鼠能够挽救NGF信号传导,而与TrkA和p75NTR相互作用的NGF则不能。(图1 )
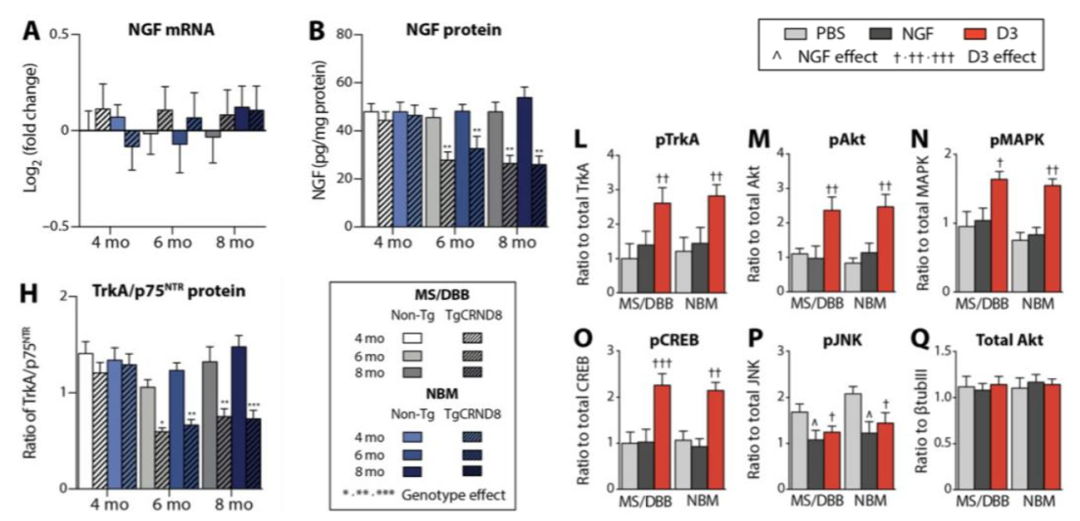
图1. D3提高随年龄增加而下降的NGF/TrkA 信号表达
(二)利用核磁共振导航的聚焦超声 (magnetic resonance imaging-guided focused ultrasound, MRIgFUS) 能够调节基底前脑血脑屏障(BBB)渗透性,超声90分钟后,处理区域没有发现明显的红细胞外溢或神经元死亡,证明此方法安全性。
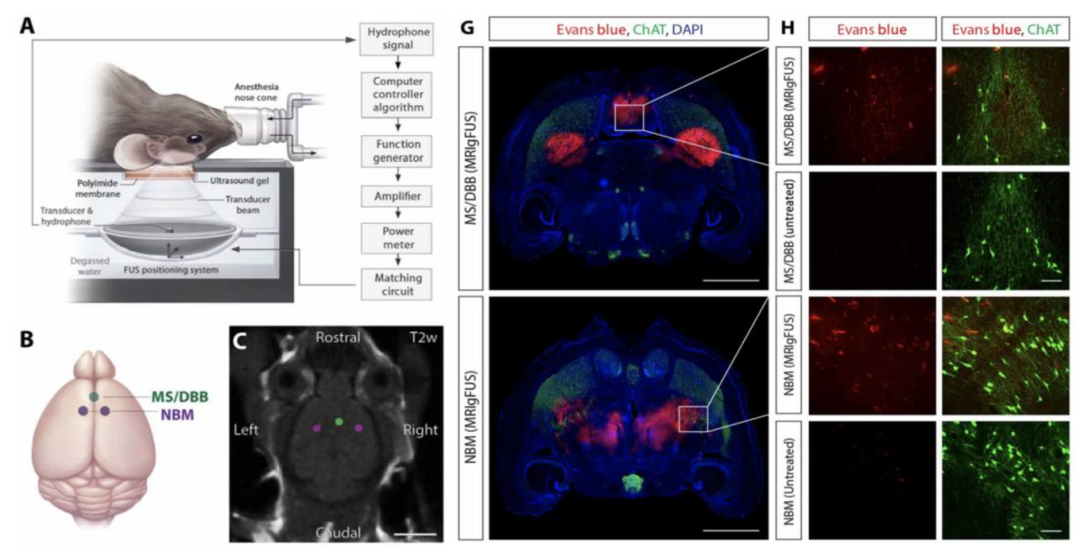
图2. 无创MRIgFUS调节基底前脑BBB渗透性
(三)MRIgFUS 开放BBB使得基底前脑D3运输加强,增加NGF蛋白水平及TrkA依赖的信号传导,且D3平均浓度、NGF蛋白水平和MRI T1相对对比度增强呈正相关。该模型证明在Aβ病理存在的情况下,选择性地TrkA受体可调节关键的细胞内信号级联转导进而促进胆碱能神经元的功能。

图3. D3增加NGF蛋白水平及TrkA依赖的信号传导
(四)总结
AD是一种以进展性认知减退为特征性改变的神经退行性障碍,很大程度上由基底前脑胆碱能神经元(brain forebrain cholinergic neurons, BFCN)变性导致。NGF的疗效受其半衰期短、与p75NTR激活相关的有害作用、以及无法通过BBB的限制,使得将其转化为治疗AD的策略成为一项重大挑战。该研究利用一种安全、可行的MRIgFUS方法,通过调节BBB渗透性,将选择性TrkA激动剂D3传输到基底前脑,激活TrkA相关的信号级联反应并增强胆碱能神经传递,促进内源性大脑可塑性和修复,最终达到有效治疗AD的目的。本研究提示,未来利用无创MRIgFUS方法调节BBB,开发靶向TrkA的神经保护剂,为阻抗AD神经变性提供极有前途的策略。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言